Nắm kỹ propan công thức và tính chất quan trọng trong hóa học
Propan công thức C3H8 là một hydrocacbon no thuộc dãy đồng đẳng của metan. Chất khí này có vai trò quan trọng trong đời sống với nhiều ứng dụng thiết thực. Propan tồn tại phổ biến trong khí tự nhiên và dầu mỏ. Các phản ứng hóa học đặc trưng của propan tạo nên nhiều sản phẩm công nghiệp giá trị.
Propan công thức và cấu tạo phân tử
Propan là một hydrocacbon no thuộc dãy đồng đẳng ankan. Tôi sẽ giúp các em hiểu rõ về công thức và cấu tạo của nó.
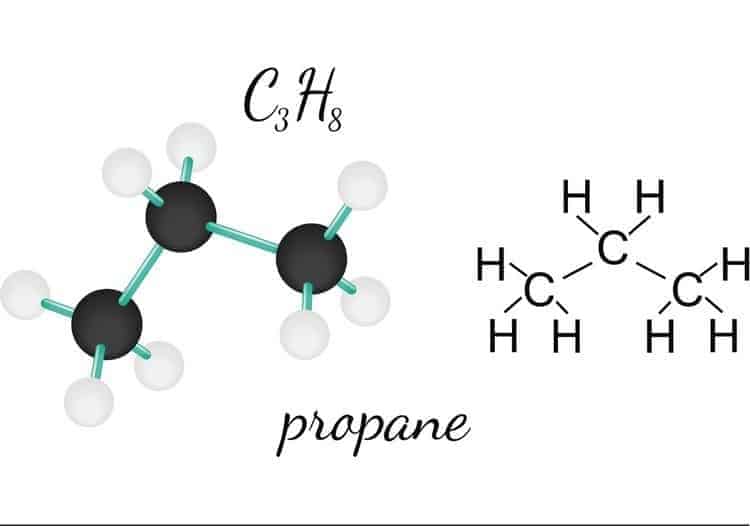
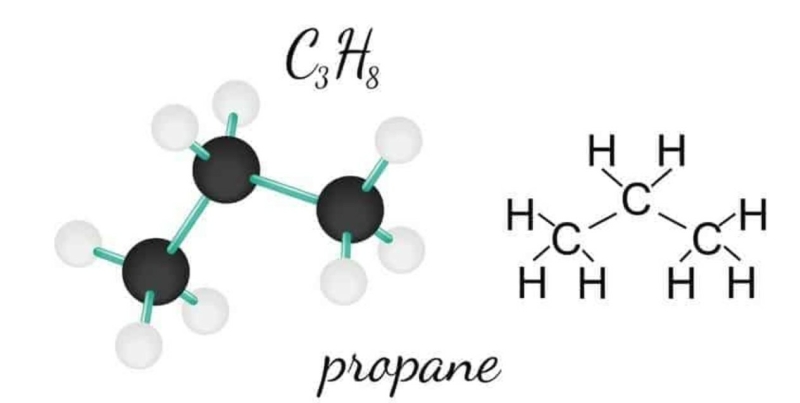
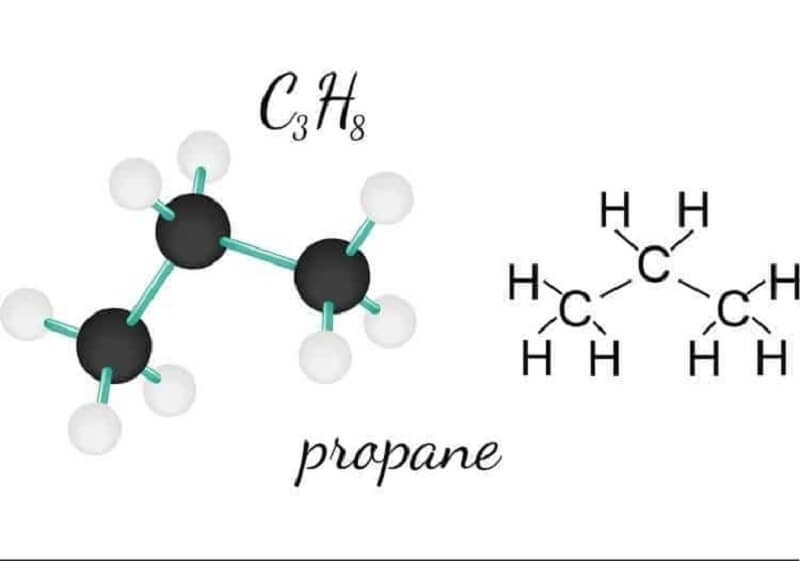
Propan công thức phân tử là C3H8. Đây là một phân tử gồm 3 nguyên tử cacbon và 8 nguyên tử hydro. Trong quá trình giảng dạy, tôi thường nhắc học sinh nhớ số nguyên tử H bằng cách áp dụng công thức CnH2n+2 với n=3.
Về cấu tạo, propan cấu tạo gồm 3 nguyên tử C liên kết với nhau tạo thành mạch thẳng. Mỗi nguyên tử C đầu mạch liên kết với 3 nguyên tử H, nguyên tử C giữa liên kết với 2 nguyên tử H. Cấu trúc này tạo nên độ bền vững cho phân tử.
Propan có mối liên hệ chặt chẽ với các đồng đẳng khác như công thức của propen và propin công thức. Sự khác biệt nằm ở loại liên kết giữa các nguyên tử C.
Khi vẽ công thức cấu tạo, tôi thường hướng dẫn học sinh viết theo thứ tự: vẽ khung C trước, sau đó thêm các liên kết H. Cách này giúp tránh nhầm lẫn số lượng liên kết.
Tính chất vật lý và hóa học của propan
Propan là một hydrocacbon no thuộc dãy đồng đẳng của metan với công thức phân tử C3H8. Chất này có vai trò quan trọng trong đời sống và công nghiệp.
Tính chất vật lý đặc trưng của propan
Ở điều kiện thường, propan tính chất vật lý nổi bật là khí không màu, không mùi và nặng hơn không khí. Nhiệt độ sôi của propan là -42°C nên dễ dàng hóa lỏng dưới áp suất.
Trong quá trình giảng dạy, tôi thường ví von propan như một “chú cá voi” trong gia đình hydrocacbon – to lớn và nặng nề hơn các “anh em” metan, etan. Điều này giúp học sinh dễ nhớ tính chất của nó.
Các phản ứng hóa học quan trọng của propan
Propan phản ứng theo 3 hướng chính: cháy, thế và cracking. Mỗi phản ứng có điều kiện và sản phẩm khác nhau, tương tự như công thức butan.
Phản ứng cháy
Khi cháy trong không khí, propan tạo ra CO2 và H2O theo phương trình:
C3H8 + 5O2 → 3CO2 + 4H2O + Q
Phản ứng này tỏa nhiều nhiệt nên được ứng dụng làm nhiên liệu đun nấu và sưởi ấm trong gia đình.
Phản ứng thế
Propan hóa học tham gia phản ứng thế với halogen (Cl2, Br2) khi có ánh sáng hoặc nhiệt độ cao. Sản phẩm tạo thành là hỗn hợp dẫn xuất halogen của propan.
Kinh nghiệm của tôi khi giảng dạy là vẽ sơ đồ phản ứng thế từng bước, giúp học sinh hiểu rõ cơ chế thay thế hydro bằng halogen.
Phản ứng cracking
Ở nhiệt độ cao (500-600°C), propan bị cracking tạo thành propylene công thức và các sản phẩm khác:
C3H8 → C3H6 + H2
Phản ứng này có ý nghĩa quan trọng trong công nghiệp hóa dầu để sản xuất các olefin.
Phương pháp điều chế và sản xuất propan công nghiệp
Propan là một hydrocacbon mạch thẳng có nhiều ứng dụng quan trọng trong đời sống và công nghiệp. Việc điều chế và sản xuất propan công nghiệp đòi hỏi các phương pháp khác nhau tùy theo quy mô và mục đích sử dụng.
Điều chế propan trong phòng thí nghiệm
Trong phòng thí nghiệm, propan có thể được điều chế bằng phản ứng Wurtz từ 1-bromopropan với natri kim loại. Phương pháp này tương tự như cách tổng hợp Fomon công thức nhưng đơn giản hơn.
Phản ứng xảy ra theo phương trình:
2CH3CH2CH2Br + 2Na → CH3CH2CH2-CH2CH2CH3 + 2NaBr
Một phương pháp khác là thủy phân muối propyl halogenua với kiềm. Phương pháp này cho hiệu suất cao hơn và dễ kiểm soát điều kiện phản ứng.
Sản xuất propan trong công nghiệp
Trong công nghiệp, propan được sản xuất chủ yếu từ quá trình chưng cất phân đoạn dầu mỏ. Quy trình này tương tự như sản xuất phân lân công thức nhưng phức tạp hơn.
Dầu thô được đun nóng đến nhiệt độ khoảng 400°C trong tháp chưng cất. Các hydrocacbon nhẹ như propan sẽ bay hơi trước và được thu hồi ở phần trên của tháp.
Ngoài ra, propan còn được tách ra từ khí tự nhiên thông qua quá trình làm lạnh và nén. Phương pháp này cho sản phẩm có độ tinh khiết cao, phù hợp làm nhiên liệu và nguyên liệu hóa dầu.
Ứng dụng của propan trong đời sống và công nghiệp
Propan là một trong những hydrocacbon đơn giản nhưng có vai trò quan trọng trong cuộc sống. Với công thức phân tử C3H8, propan tồn tại ở dạng khí ở điều kiện thường và dễ dàng hóa lỏng dưới áp suất.
Tôi sẽ phân tích chi tiết các ứng dụng chính của propan trong 3 lĩnh vực: nhiên liệu, công nghiệp hóa chất và sinh hoạt hàng ngày.
Ứng dụng làm nhiên liệu
Propan khí được sử dụng rộng rãi làm nhiên liệu trong các động cơ đốt trong. Khi đốt cháy, propan tỏa nhiệt lượng lớn và ít gây ô nhiễm môi trường.
Theo số liệu từ Hiệp hội Khí đốt Thế giới, propan chiếm khoảng 3% tổng lượng nhiên liệu sử dụng trong giao thông vận tải toàn cầu. Đặc biệt tại các nước châu Âu, xe chạy bằng propan ngày càng phổ biến.
Ứng dụng trong công nghiệp hóa chất
Propan là nguyên liệu quan trọng trong sản xuất nhiều sản phẩm hóa chất. Qua quá trình cracking, propan tạo thành propen – tiền chất để sản xuất nhựa PP là gì.

Ngoài ra, propan còn được dùng làm nguyên liệu sản xuất tơ capron là gì và Tơ lapsan công thức. Các sản phẩm này có độ bền cao và được ứng dụng rộng rãi trong công nghiệp dệt may.
Ứng dụng trong sinh hoạt
Trong sinh hoạt, propan được sử dụng phổ biến nhất dưới dạng gas đun nấu. Propan ứng dụng trong lĩnh vực này có nhiều ưu điểm:
- Nhiệt lượng tỏa ra lớn, giúp nấu ăn nhanh chóng
- An toàn khi sử dụng đúng cách
- Giá thành hợp lý
- Dễ dàng vận chuyển và bảo quản
Ngoài ra, propan còn được dùng làm nhiên liệu sưởi ấm trong mùa đông tại nhiều quốc gia. Khí propan khi đốt cháy cho ngọn lửa xanh, nhiệt độ cao và ít khói.
FAQ: Câu hỏi thường gặp về propan
Propan là một trong những khí đốt phổ biến nhất được sử dụng trong đời sống. Tôi thường nhận được nhiều câu hỏi từ học sinh về đặc tính của propan và các ứng dụng của nó.
Propan có độc không?
Propan không gây độc khi tiếp xúc trực tiếp với da hoặc niêm mạc. Tuy nhiên, khi nồng độ propan trong không khí quá cao sẽ gây thiếu oxy và ngạt thở.
Trong quá trình giảng dạy, tôi luôn nhấn mạnh với học sinh cần thận trọng khi sử dụng propan. Cần đảm bảo thông thoáng khi dùng bếp gas và kiểm tra rò rỉ thường xuyên.
Propan có thể hóa lỏng không?
Propan dễ dàng hóa lỏng dưới áp suất thấp ở nhiệt độ thường. Đây là tính chất quan trọng giúp propan được đóng chai và vận chuyển thuận tiện.
Khi giảng bài về isopentan là gì, tôi thường so sánh với propan để học sinh hiểu rõ hơn về nhiệt độ sôi của hydrocarbon.
Propan và LPG có giống nhau không?
LPG (khí gas hóa l�ng) là hỗn hợp của propan và butan. Tỷ lệ propan trong LPG thường dao động từ 30-40%.
Propan có nhiệt trị cao hơn butan nên thường được ưu tiên sử dụng trong mùa lạnh. Còn butan phù hợp hơn cho mùa nóng do áp suất hơi thấp hơn.
Kiến thức về propan công thức giúp người học nắm vững cấu trúc phân tử, tính chất và phản ứng của hợp chất quan trọng này. Propan đóng vai trò thiết yếu trong đời sống với ứng dụng làm nhiên liệu và nguyên liệu công nghiệp. Việc nắm chắc các phương pháp điều chế, tính chất đặc trưng và phản ứng hóa học của propan tạo nền tảng cho học sinh tiếp cận các kiến thức hóa học nâng cao.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

