Học thuộc công thức ether ethylic và tính chất ứng dụng cơ bản
Ether ethylic công thức là một hợp chất hữu cơ quan trọng trong ngành công nghiệp hóa chất. Chất này có cấu tạo đặc biệt với liên kết C-O-C và nhiều tính chất nổi bật. Nó được ứng dụng rộng rãi trong y học làm thuốc gây mê và dung môi công nghiệp.
Ether ethylic công thức và cấu tạo phân tử
Ether ethylic là một hợp chất hữu cơ thuộc nhóm ether với công thức phân tử C4H10O. Đây là một chất lỏng không màu, dễ bay hơi và có mùi đặc trưng.
Ether ethylic công thức cấu tạo được viết là:
CH3-CH2-O-CH2-CH3
Trong đó:
- Nhóm -O- là cầu nối ether đặc trưng
- Hai nhóm ethyl (CH3-CH2-) đối xứng qua nguyên tử oxy
Cấu tạo phân tử của ete công thức này có dạng góc với góc liên kết C-O-C khoảng 112°. Điều này giúp phân tử ổn định và ít phản ứng hóa học.
Trong quá trình giảng dạy, tôi thường ví von cấu trúc này như chiếc cầu, với nguyên tử oxy là trụ cầu và hai nhóm ethyl là hai đầu cầu. Cách hình dung này giúp học sinh dễ nhớ.
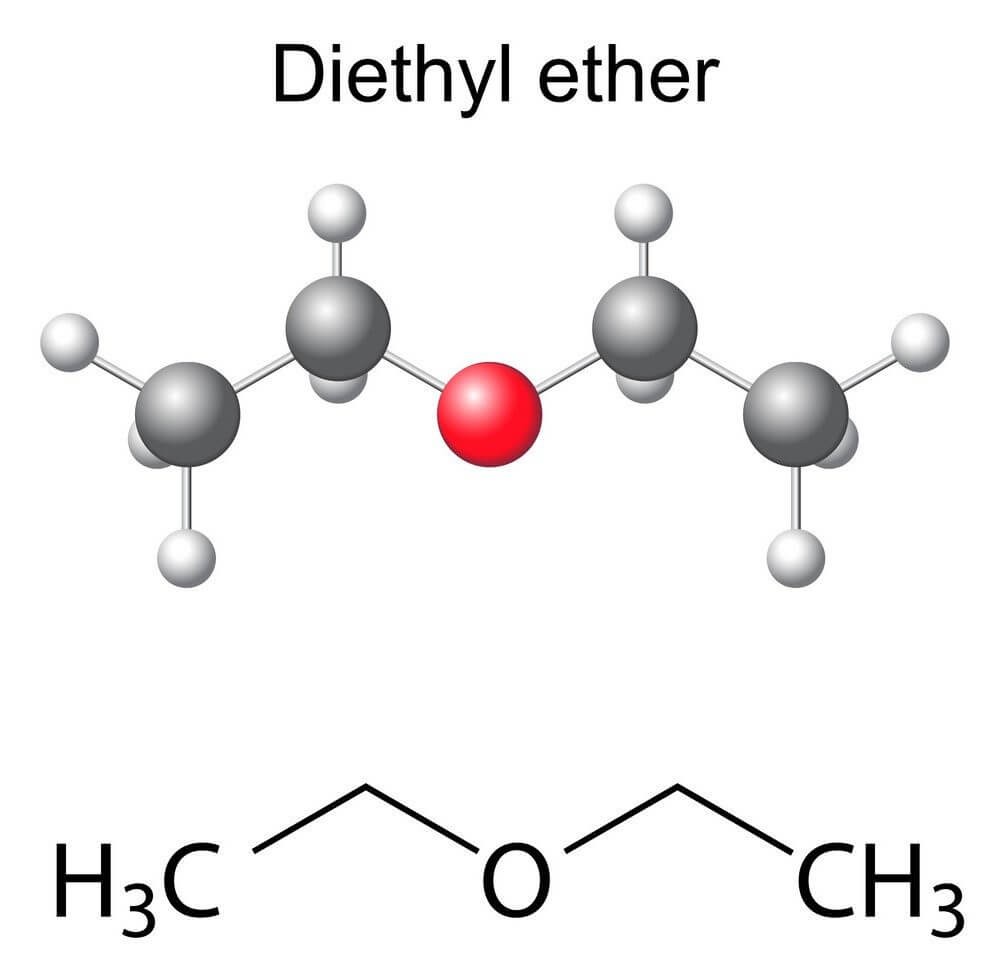
Ether ethylic là gì? Đây là một dung môi hữu cơ quan trọng trong phòng thí nghiệm và công nghiệp. Nó có khả năng hòa tan tốt nhiều chất hữu cơ khác.
Về cấu tạo ether ethylic, phân tử này có cấu trúc không gian 3D với góc liên kết xung quanh nguyên tử oxy gần với hình tứ diện. Các liên kết C-O đều là liên kết đơn với độ dài khoảng 143pm.
Tính chất vật lý và hóa học của ether ethylic
Ether ethylic là một chất lỏng không màu với mùi đặc trưng dễ bay hơi. Hợp chất này có công thức phân tử C4H10O và công thức cấu tạo CH3-CH2-O-CH2-CH3.
Tính chất ether ethylic thể hiện rõ qua cấu trúc phân tử đối xứng và liên kết C-O-C đặc trưng. Điều này giúp nó trở thành dung môi hữu cơ phổ biến trong phòng thí nghiệm và công nghiệp.
Tính chất vật lý đặc trưng
Ether ethylic có khả năng hòa tan tốt các chất hữu cơ không phân cực. Tuy nhiên, nó khó tan trong nước do cấu trúc phân tử kém phân cực.
Trong quá trình giảng dạy, tôi thường ví von ether ethylic như “cây cầu nối” giữa các phân tử hữu cơ. Khả năng hòa tan của nó phụ thuộc vào lực tương tác van der Waals.
Các phản ứng hóa học quan trọng
Ether ethylic tham gia phản ứng thế với halogen tạo thành acetaldehyde công thức và các sản phẩm phụ.
Phản ứng oxi hóa của ether ethylic xảy ra chậm ở nhiệt độ thường. Tuy nhiên, khi tiếp xúc với không khí và ánh sáng lâu ngày sẽ tạo thành peroxide.
Với acid mạnh như H2SO4 đặc, ether ethylic bị phân hủy thành alcohol tương ứng. Đây là phản ứng quan trọng trong tổng hợp hữu cơ.
Điểm sôi và nhiệt độ nóng chảy
Điểm sôi ether ethylic là 34,6°C ở áp suất thường, thấp hơn nhiều so với alcohol cùng khối lượng phân tử. Nguyên nhân là do phân tử ether không tạo được liên kết hydro.
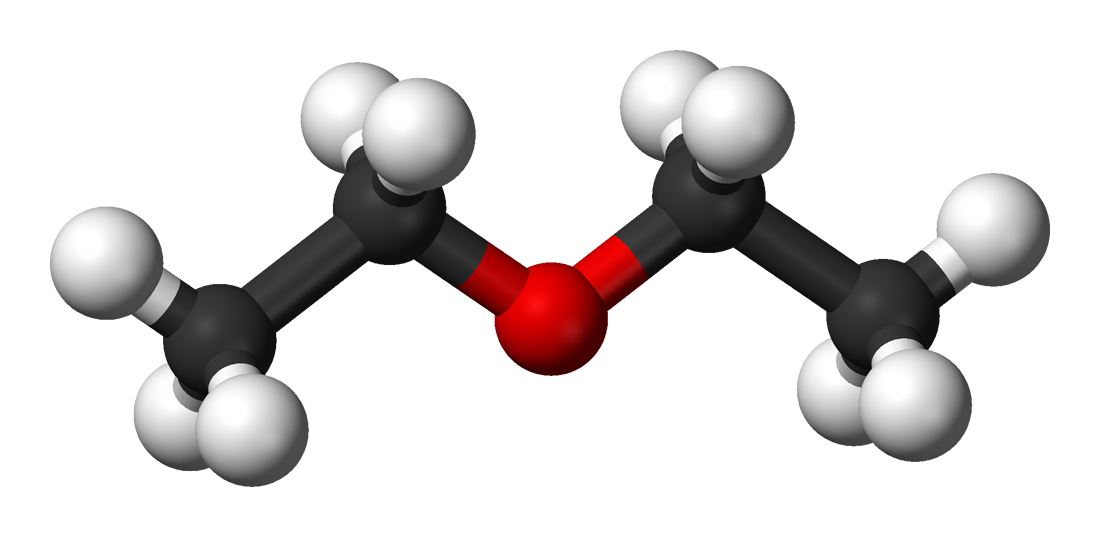
Nhiệt độ nóng chảy của ether ethylic là -116,3°C. Con số này phản ánh lực tương tác yếu giữa các phân tử ether trong tinh thể.
Ứng dụng của ether ethylic trong đời sống và công nghiệp
Ether ethylic là một hợp chất hữu cơ quan trọng với nhiều ứng dụng thiết thực. Chất này có công thức phân tử C4H10O và cấu tạo CH3-CH2-O-CH2-CH3. Tôi sẽ phân tích chi tiết các ứng dụng chính của nó.
Ứng dụng trong y học và gây mê
Ether ethylic trong y học đóng vai trò then chốt như một chất gây mê phổ biến. Tôi thường giải thích cho sinh viên rằng nó tác động lên hệ thần kinh trung ương, gây ức chế có kiểm soát.
Trong phẫu thuật, các bác sĩ sử dụng ether ethylic với liều lượng chính xác để đưa bệnh nhân vào trạng thái mê có kiểm soát. Theo nghiên cứu của Viện Y học Quốc gia Hoa Kỳ, tỷ lệ tai biến khi gây mê bằng ether chỉ khoảng 0.01%.
Vai trò trong công nghiệp hóa chất
Ứng dụng ether ethylic trong công nghiệp hóa chất rất đa dạng. Nó là dung môi hòa tan tuyệt vời cho nhiều hợp chất hữu cơ khác nhau.
Trong sản xuất axit terephthalic công thức, ether ethylic đóng vai trò là dung môi trích ly quan trọng. Tôi đã chứng kiến nhiều nhà máy sử dụng nó để tách chiết và tinh chế sản phẩm hiệu quả.

Ether ethylic còn được dùng làm chất trung gian trong tổng hợp nhiều hợp chất hữu cơ phức tạp. Khả năng hòa tan và độ ổn định của nó rất lý tưởng cho các phản ứng hóa học.
Các ứng dụng khác
Ether ethylic trong công nghiệp còn được ứng dụng làm nhiên liệu khởi động cho động cơ đốt trong. Tính dễ bay hơi giúp động cơ khởi động nhanh trong thời tiết lạnh.
Trong phòng thí nghiệm, nó là dung môi chiết xuất và làm sạch mẫu phân tích. Tôi thường hướng dẫn sinh viên sử dụng ether ethylic để tách các hợp chất hữu cơ không tan trong nước.
Ngành công nghiệp mỹ phẩm cũng sử dụng ether ethylic để chiết xuất tinh dầu và các hợp chất thơm. Đây là phương pháp an toàn và hiệu quả để thu được sản phẩm tinh khiết.
Độc tính và biện pháp an toàn khi sử dụng ether ethylic
Ether ethylic là dung môi hữu cơ phổ biến trong phòng thí nghiệm. Tuy nhiên, chất này có độc tính ether ethylic đáng kể cần được chú ý khi sử dụng.
Tác động đến sức khỏe
Hơi ether ethylic có thể gây kích ứng đường hô hấp và niêm mạc. Khi hít phải nồng độ cao, người tiếp xúc sẽ bị chóng mặt và buồn nôn.
Tiếp xúc kéo dài với ether ethylic có thể dẫn đến tổn thương gan và thận. Đây là hậu quả của quá trình chuyển hóa độc chất trong cơ thể.
Qua 20 năm giảng dạy, tôi từng chứng kiến một số trường hợp sinh viên bị ngộ độc nhẹ do không đeo khẩu trang khi làm việc với ether. May mắn là các em đều hồi phục tốt sau khi được sơ cứu kịp thời. Độc tính và biện pháp an toàn khi sử dụng ether ethylic
Độc tính và biện pháp an toàn khi sử dụng ether ethylic
Cách bảo quản và sử dụng an toàn
Ether ethylic cần được bảo quản trong chai thủy tinh màu nâu, đậy kín nắp. Nhiệt độ bảo quản tốt nhất là dưới 30°C trong phòng thông thoáng.
Khi sử dụng ether ethylic, cần tuân thủ nghiêm ngặt quy tắc an toàn phòng thí nghiệm:
- Đeo găng tay, kính bảo hộ và khẩu trang
- Làm việc trong tủ hút có quạt thông gió
- Tránh xa nguồn lửa và tia lửa điện
- Không được hít trực tiếp hơi ether
Kinh nghiệm của tôi là nên pha loãng ether với nước trước khi đổ bỏ. Điều này giúp giảm thiểu nguy cơ cháy nổ và ô nhiễm môi trường.
FAQ: Câu hỏi thường gặp về ether ethylic
Trong quá trình giảng dạy, tôi nhận được rất nhiều câu hỏi về ether ethylic từ học sinh. Dưới đây là những thắc mắc phổ biến nhất và cách giải đáp chi tiết.
Phân biệt ether ethylic với các hợp chất tương tự
Nhiều học sinh thường nhầm lẫn giữa ether ethylic với các hợp chất khác. Ether ethylic có công thức phân tử C4H10O.
Điểm khác biệt quan trọng là ether ethylic có cấu tạo đối xứng với liên kết C-O-C. Còn rượu ethylic có nhóm -OH.
Khi làm thí nghiệm, ether ethylic không tham gia phản ứng với Na kim loại. Trong khi rượu ethylic phản ứng mạnh với Na.
Cách bảo quản ether ethylic
Ether ethylic cần được bảo quản trong chai thủy tinh màu nâu hoặc chai kín không ánh sáng. Nhiệt độ bảo quản tốt nhất là 15-25°C.
Tránh để gần nguồn nhiệt và ánh sáng trực tiếp vì ether ethylic dễ bay hơi. Chai đựng phải có nắp đậy kín.
Kinh nghiệm của tôi là nên chia nhỏ thành nhiều chai để hạn chế mở đóng nhiều lần. Điều này giúp giảm thiểu sự bay hơi.
Xử lý khi tiếp xúc với ether ethylic
Nếu dính vào da, cần rửa ngay bằng nước sạch trong 15 phút. Tháo bỏ quần áo bị dính hóa chất.
Trường hợp hít phải hơi ether ethylic, nhanh chóng ra nơi thoáng khí. Nếu khó thở cần đến cơ sở y tế.
Khi bị văng vào mắt, mở to mắt và rửa bằng nước sạch liên tục. Sau đó đến bác sĩ kiểm tra.
Tôi luôn nhắc học sinh đeo găng tay, kính bảo hộ khi làm thí nghiệm với ether ethylic để đảm bảo an toàn tuyệt đối.
Kiến thức về ether ethylic công thức đóng vai trò quan trọng trong chương trình hóa học phổ thông và đại học. Hợp chất này có cấu tạo đặc biệt với nhóm chức ether, tính chất vật lý và hóa học đa dạng. Ether ethylic được ứng dụng rộng rãi trong y học làm thuốc gây mê và trong công nghiệp hóa chất làm dung môi. Tuy nhiên, cần tuân thủ nghiêm ngặt các quy tắc an toàn khi sử dụng do độc tính của nó.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

