Công thức tính nguyên tử khối dễ hiểu và bài tập minh họa
Nguyên tử khối là một trong những kiến thức nền tảng của hóa học, đóng vai trò quan trọng trong việc xác định đặc tính của các nguyên tố và hợp chất. Để hiểu rõ hơn về nguyên tử khối, bài viết này sẽ giới thiệu công thức tính nguyên tử khối một cách dễ hiểu, kèm theo các bài tập minh họa để giúp các em áp dụng kiến thức vào thực tế và củng cố quá trình học tập.
Nguyên tử khối là gì? Công thức tính nguyên tử khối
Nguyên tử khối là khối lượng tương đối của nguyên tử. Nguyên tử khối của một nguyên tử cho biết khối lượng của nguyên tử đó nặng gấp bao nhiêu lần đơn vị khối lượng nguyên tử.
Cách xác định nguyên tử khối:
Khối lượng của các loại hạt cấu tạo nên nguyên tử:
- Khối lượng của một electron: me = 9,1094.10-31 kg.
- Khối lượng của một proton: mp = 1,6726.10-27 kg.
- Khối lượng của một nơtron: mn = 1,6748.10-27 kg.
Proton và nơtron có khối lượng xấp xỉ nhau, khối lượng electron bé hơn nhiều so với khối lượng proton.
Coi như nguyên tử khối xấp xỉ số khối hạt nhân. Do vậy công thức tính số khối như sau:
Số khối (A) = tổng số proton (Z) + tổng số nơtron (N)
Khối lượng nguyên tử được tính bằng tổng khối lượng các hạt trong nguyên tử:
mnguyên tử = ∑mp + ∑mn + ∑me
Đơn vị khối lượng nguyên tử là u.
1u = 1,6605.10-27 kg = 1,6605.10-24 g.
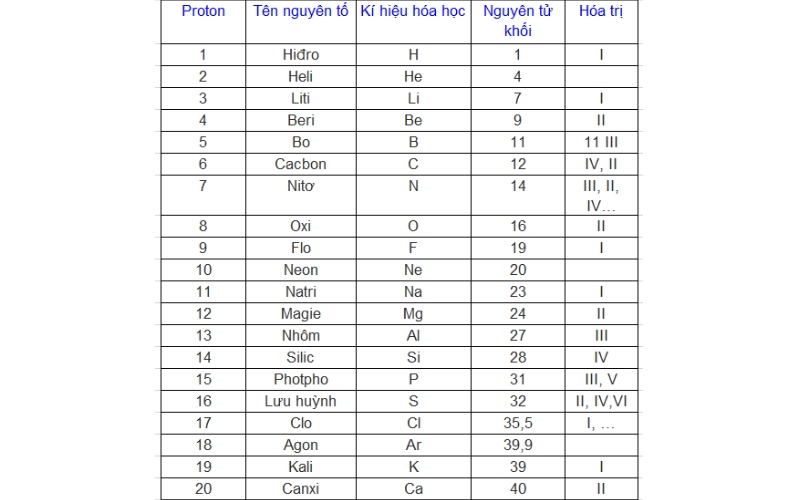
Nguyên tử khối của một số nguyên tố hay gặp
Dưới đây là danh sách nguyên tử khối của một số nguyên tố hay gặp được chúng tôi tổng hợp giúp các bạn học sinh tham khảo
Các dạng bài tập về nguyên tử khối
Dưới đây là những dạng bài tập thường gặp về nguyên tử khối, giúp học sinh củng cố lý thuyết và nắm vững cách giải bài một cách hiệu quả.
Bài tập tính khối lượng nguyên tử
Tính toán khối lượng của một nguyên tử dựa trên nguyên tử khối và đơn vị khối lượng nguyên tử (amu).
Ví dụ: Tính khối lượng của một nguyên tử oxy, biết nguyên tử khối của oxy là 16 đvC.
Bài tập về đồng vị
Đồng vị là các biến thể của cùng một nguyên tố, khác nhau về số neutron. Bài toán thường yêu cầu xác định tỉ lệ phần trăm của các đồng vị dựa trên nguyên tử khối trung bình.
Ví dụ: Trong tự nhiên, chlorine tồn tại dưới hai đồng vị Cl-35 và Cl-37 với tỉ lệ phần trăm lần lượt là 75,76% và 24,24%. Hãy tính nguyên tử khối trung bình của chlorine.
Bài tập xác định thành phần nguyên tử
Xác định số proton, neutron và electron trong một nguyên tử dựa trên số khối và số hiệu nguyên tử.
Ví dụ: Tìm số proton, neutron và electron của nguyên tử natri có số khối là 23 và số hiệu nguyên tử là 11.
Bài tập về cấu hình electron
Viết cấu hình electron cho các nguyên tử và ion dựa trên quy tắc cấu hình electron.
Ví dụ: Viết cấu hình electron cho nguyên tử sắt (Fe) có số hiệu nguyên tử là 26.
Bài tập trắc nghiệm về khối lượng nguyên tử
Các câu hỏi trắc nghiệm liên quan đến tính toán và kiến thức về khối lượng nguyên tử.
Ví dụ: Tính khối lượng của một nguyên tử Magie, biết nguyên tử khối của Magie là 24 đvC.
Bài tập về tính nguyên tử khối kèm đáp án
Dưới đây là một số bài tập kèm đáp án chi tiết về nguyên tử khối
Bài 1
Một hợp chất gồm 1 nguyên tử X liên kết 2 nguyên tử Oxi và nặng hơn phân tử hiđro 22 lần.
a/ Tính phân tử khối hợp chất.
b/ Tính NTK X , cho biết tên và KHHH
Hướng dẫn
Phân tử hidro (2H) => PTK = 2 . 1 = 2
Hợp chất nặng hơn phân tử hidro 22 lần => PTK của hợp chất: 2.22 = 44
1 nguyên tử X liên kết 2 nguyên tử O => hợp chất (1X; 2O) => PTK = X + 2.16 = X + 32
=> X + 32 = 2 . 22 = 44
=> X = 44 – 32 = 12
Vậy X là nguyên tố cacbon, KHHH là C.

Bài 2
Biết nguyên tố X có nguyên tử khối bằng 3,5 lần nguyên tử khối của oxi. Xác định tên và KHHH của nguyên tố X.
Hướng dẫn:
Diễn đạt X có nguyên tử khối bằng 3,5 lần NTK của oxi là: X = 3,5.O
NTK của O đã biết → tìm được NTK của X → dò bảng xác định được tên nguyên tố X → KHHH
X = 3,5 . O = 3,5 . 16 = 56
=> X là nguyên tố sắt, KHHH Fe.
Bài 3
Tính phân tử khối của H2SO4
Hướng dẫn
Phân tử khối của H2SO4 là: MH2SO4 = 2×1 + 32 + 4×16 = 98 đvC.
Bài 4
Tổng số hạt proton, nơtron, electron trong hai nguyên tử kim loại A và B là 142, trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 42. Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 12. Xác định 2 kim loại A và B.
Hướng dẫn
Gọi tổng số hạt proton, nơtron và electron của nguyên tử A là : pA, nA, eA và B là pB, nB, eB.
Ta có pA = eA và pB = eB.
Theo bài : Tổng số các loại hạt proton, nơtron và electron của hai nguyên tử A và B là 142 nên: pA + nA + eA + pB + nB + eB = 142 2pA + 2pB + nA + nB = 142 (1)
Tổng số hạt mang điện nhiều hơn số hạt không mang điện là 42 nên:
pA + eA + pB + eB – nA – nB = 42 2pA + 2pB – nA – nB = 42 (2)
Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 12 nên:
pB + eB – pA – eA = 12 2pB – 2pA = 12 pB – pA = 6 (3)
Từ (1), (2), (3) ta có : pA = 20 (Ca) và pB = 26 (Fe).
Bài 5
Tổng số hạt cơ bản trong phân tử X có công thức là M2O là 140, trong phân tử X thì tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44. Vậy X là
Hướng dẫn
Trong X có 2 nguyên tử M và 1 nguyên tử O.
Nên ta có : 2.ZM + 8 = (140 + 44) : 4 = 46 => Z =19 => K => X là K2O
Bài 6
M và X là hai nguyên tử kim loại, tổng số hạt cơ bản của cả nguyên tử M và X là 142, trong đó tổng số hạt mang điện nhiều hơn không mang điện là 42. Số hạt mang điện trong nguyên tử M nhiều hơn trong nguyên tử X là 12. Tìm M và X
Hướng dẫn
Ta có: ZM + ZX = (142 : 42) : 4 = 46.
2ZM – 2ZX = 12 (tổng số hạt mang điện là 2Z)
Dễ dàng tìm được ZM = 26, ZX = 20. Vậy M là Fe, X là Ca.
Lời kết
Các công thức tính nguyên tử khối và bài tập luyện tập không chỉ giúp học sinh hiểu sâu hơn về những khái niệm nền tảng trong hóa học, mà còn mở ra cơ hội rèn luyện tư duy logic để chinh phục những bài toán phức tạp. Thông qua quá trình luyện tập, học sinh không chỉ củng cố kiến thức, mà còn xây dựng sự tự tin vững vàng, chuẩn bị tốt nhất cho những kỳ thi phía trước.
Bài viết liên quan
Tổng quan công thức Faraday hóa và ứng dụng trong điện phân
Tìm hiểu chi tiết về công thức Faraday hóa học trong điện phân, cách áp dụng định luật và giải bài tập với phương pháp đơn giản. Hướng dẫn tính toán khối lượng chất điện phân chuẩn xác.

Thông tin chi tiết về công thức tỉ khối và cách áp dụng trong hóa học
Tìm hiểu công thức tỉ khối và cách áp dụng trong hóa học. Bài viết giải thích chi tiết các loại tỉ khối, phương pháp xác định và bài tập thực hành cho học sinh dễ hiểu.

Tổng quan công thức tính nồng độ đương lượng và cách áp dụng
Tìm hiểu chi tiết công thức tính nồng độ đương lượng, cách xác định đương lượng gam và giải bài tập với phương pháp đơn giản. Bao gồm công thức, ví dụ và bài tập mẫu có lời giải.
Tổng quan công thức tính số liên kết hóa trị và cách áp dụng chuẩn xác
Hướng dẫn công thức tính số liên kết hóa trị và phương pháp xác định chính xác các loại liên kết trong phân tử hữu cơ. Giải thích chi tiết cách tính liên kết σ, π kèm bài tập minh họa.
Phân tích công thức tính liên kết hidro và ứng dụng trong hóa học
Tìm hiểu công thức tính liên kết hidro và cách áp dụng trong các phân tử, gen, protein. Giải thích chi tiết bản chất, vai trò quan trọng trong nước, rượu và axit nucleic.

Công thức tính đồng phân và cách xác định nhanh các dạng đồng phân hóa học
Tìm hiểu công thức tính đồng phân và phương pháp xác định nhanh số đồng phân trong hóa học. Hướng dẫn chi tiết cách tính đồng phân ankan, ancol kèm bài tập và mẹo giải nhanh cho học sinh.

