Nghiên cứu công thức phân tử của etylamin và tính chất hóa học cơ bản
Công thức phân tử của etylamin là nền tảng để hiểu về nhóm amin bậc một. Chất này có cấu trúc đơn giản nhưng đóng vai trò quan trọng trong tổng hợp hữu cơ. Etylamin thể hiện tính bazơ mạnh và tham gia nhiều phản ứng hóa học đặc trưng.
Công thức phân tử của etylamin
Etylamin là một amin bậc 1 có công thức phân tử của etylamin là C2H5NH2. Đây là một hợp chất hữu cơ chứa nhóm amino (-NH2) gắn với gốc etyl (C2H5-).
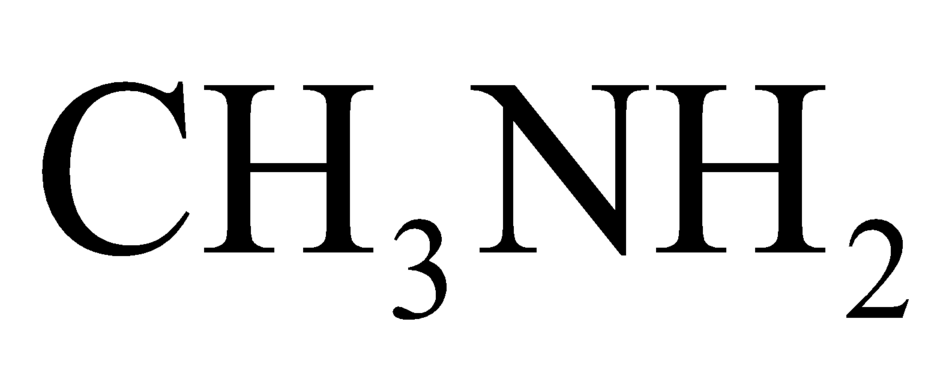
Cấu tạo phân tử của công thức etylamin có thể được phân tích chi tiết như sau:
- C2H5: Gốc etyl, gồm 2 nguyên tử cacbon và 5 nguyên tử hydro
- NH2: Nhóm amino, gồm 1 nguyên tử nitơ và 2 nguyên tử hydro
Trong quá trình giảng dạy, tôi thường giúp học sinh ghi nhớ công thức này bằng cách chia thành 2 phần: phần gốc hydrocarbon C2H5- và phần nhóm chức -NH2. Điều này giúp các em dễ dàng nhận biết và viết đúng công thức khi làm bài tập.
Một cách đơn giản để nhớ cấu tạo của etylamin là tưởng tượng nó như một phân tử ethan (C2H6) với một nguyên tử H được thay thế bằng nhóm NH2. Phương pháp này đã giúp nhiều học sinh yếu hóa học của tôi tiến bộ rõ rệt.
Cấu tạo và đặc điểm phân tử etylamin
Phân tử etylamin có cấu tạo khá đơn giản nhưng đóng vai trò quan trọng trong nhiều phản ứng hóa học. Nó thuộc nhóm amin bậc một với công thức phân tử là C2H5NH2. Tương tự như công thức cấu tạo của etilen glicol, cấu trúc của etylamin cũng có sự liên kết giữa các nguyên tử cacbon.
Cấu trúc phân tử của etylamin
Phân tử etylamin có cấu trúc gồm một mạch cacbon thẳng chứa 2 nguyên tử C. Nguyên tử N mang một cặp electron tự do và liên kết với 2 nguyên tử H. Góc liên kết H-N-H xấp xỉ 107°, gần với góc tứ diện 109.5°.
Trong quá trình giảng dạy, tôi thường ví von cấu trúc này như một cái “dù” với N ở giữa và các nguyên tử H như những thanh dù xòe ra. Cách hình dung này giúp học sinh dễ nhớ hơn về hình học không gian của phân tử.
Liên kết trong phân tử etylamin
Các liên kết trong phân tử cấu tạo etylamin đều là liên kết cộng hóa trị. Liên kết C-C và C-H là liên kết không phân cực. Liên kết N-H có tính phân cực do độ âm điện của N lớn hơn H.
Đặc biệt, cặp electron tự do trên nguyên tử N tạo ra khả năng liên kết hydro với các phân tử khác. Điều này giải thích nhiệt độ sôi của etylamin cao hơn hydrocarbon có khối lượng phân tử tương đương.
Các nhóm chức đặc trưng
Nhóm chức quan trọng nhất trong phân tử là nhóm amino (-NH2). Nhóm này quyết định tính bazơ và khả năng phản ứng của etylamin. Nhóm etyl (-C2H5) đóng vai trò gốc hydrocarbon.

Khi giảng dạy, tôi thường nhấn mạnh với học sinh rằng nhóm -NH2 giống như “trung tâm hoạt động” của phân tử. Nó tham gia vào hầu hết các phản ứng hóa học quan trọng của etylamin.
Tính chất hóa học của etylamin
Etylamin là một amin bậc 1 có công thức phân tử C2H5NH2. Hợp chất này thể hiện nhiều tính chất etylamin đặc trưng của nhóm amin no, đơn chức, mạch hở.
Tôi thường ví von etylamin như một “anh chàng” hoạt động sôi nổi trong các phản ứng hóa học. Sau hơn 20 năm giảng dạy, tôi nhận thấy học sinh dễ nhớ tính chất của nó qua 4 nhóm phản ứng chính.
Tính bazơ của etylamin
Etylamin tính bazơ mạnh hơn amoniac do hiệu ứng đẩy electron của nhóm etyl. Phân tử etylamin có cặp electron tự do trên nguyên tử N.
Trong dung dịch nước, etylamin phản ứng với nước theo phương trình:
C2H5NH2 + H2O ⇌ C2H5NH3+ + OH-
Tôi thường nhắc học sinh rằng etylamin có thể làm đổi màu quỳ tím thành xanh và có thể tạo muối với các axit. Giống như công thức của trimetylamin, etylamin cũng là một bazơ yếu.
Phản ứng với axit
Etylamin tham gia phản ứng trung hòa với axit tạo thành muối. Đây là phản ứng đặc trưng của amin.
Phương trình phản ứng tổng quát:
C2H5NH2 + HX → C2H5NH3+X-
(X là gốc axit như Cl-, NO3-, SO42-)
Ví dụ phản ứng với axit clohidric:
C2H5NH2 + HCl → C2H5NH3+Cl-
Phản ứng thế
Etylamin có khả năng tham gia phản ứng thế H trong nhóm NH2 bằng các gốc hiđrocacbon.
Phản ứng với ankyl halogenua:
C2H5NH2 + CH3I → C2H5NHCH3 + HI
C2H5NHCH3 + CH3I → C2H5N(CH3)2 + HI
Các phản ứng thế này giúp tổng hợp các amin bậc cao hơn từ etylamin.
Phản ứng với halogen
Etylamin phản ứng với halogen (Cl2, Br2) trong môi trường kiềm tạo thành các sản phẩm thế.
Phương trình phản ứng:
C2H5NH2 + 3Cl2 + 3NaOH → C2H5NCl2 + 3NaCl + 3H2O
Đây là phản ứng quan trọng trong công nghiệp để điều chế các dẫn xuất halogen của amin.
Ứng dụng và vai trò của etylamin trong hóa học
Etylamin là một amin bậc một có công thức phân tử C2H5NH2, được ứng dụng rộng rãi trong nhiều lĩnh vực. Hợp chất này có vai trò quan trọng trong công nghiệp hóa chất và tổng hợp hữu cơ. Ngoài ra, etylamin còn được sử dụng làm nguyên liệu sản xuất thuốc trong ngành dược phẩm.
Ứng dụng trong công nghiệp
Trong công nghiệp, etylamin được sử dụng làm chất trung gian để sản xuất thuốc trừ sâu và phân bón. Hợp chất này tham gia vào quá trình tổng hợp các chất hoạt động bề mặt và chất tẩy rửa công nghiệp.
Theo nghiên cứu của Viện Hóa học Công nghiệp Việt Nam, etylamin còn được dùng làm chất xúc tác trong sản xuất cao su tổng hợp. Đặc biệt, hợp chất này có khả năng tăng độ bền và độ đàn hồi của sản phẩm cao su.
Vai trò trong tổng hợp hữu cơ
Trong phòng thí nghiệm, etylamin hóa học 11 đóng vai trò là tác nhân ankyl hóa quan trọng. Hợp chất này tham gia phản ứng với nhiều nhóm chức khác nhau để tạo ra các dẫn xuất mới.
Etylamin còn được sử dụng để tổng hợp công thức hoá học của ketamin và các hợp chất dược phẩm khác. Phản ứng giữa etylamin với các acid carboxylic tạo ra các amid có hoạt tính sinh học cao.
Ứng dụng trong y dược
Trong ngành dược phẩm, etylamin là nguyên liệu quan trọng để tổng hợp nhiều loại thuốc. Hợp chất này tham gia vào quá trình sản xuất thuốc kháng histamin và thuốc giảm đau.
Các nhà khoa học tại Viện Kiểm nghiệm thuốc Trung ương đã nghiên cứu thành công việc sử dụng etylamin để tổng hợp một số dẫn xuất mới có tác dụng điều trị. Kết quả cho thấy các hợp chất này có hoạt tính kháng viêm và kháng khuẩn tốt.
Etylamin còn được dùng làm chất bảo quản trong các chế phẩm dược phẩm. Tính bazơ của nó giúp ổn định pH và kéo dài thời hạn sử dụng của thuốc.
FAQ: Câu hỏi thường gặp về etylamin
Etylamin là hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Các câu hỏi thường gặp về etylamin giúp hiểu rõ hơn về tính chất và ứng dụng của nó.
Etylamin thuộc nhóm amin bậc mấy?
Etylamin là một etylamin amin bậc 1 điển hình với công thức phân tử C2H5NH2. Cấu tạo phân tử gồm một nhóm etyl (C2H5-) liên kết với nhóm -NH2.
Tôi thường giải thích cho học sinh rằng amin bậc 1 giống như một “ngôi nhà” chỉ có một “cửa ra vào” là nguyên tử H. Điều này giúp phân biệt với tính chất etyl propionat và các hợp chất khác.
Cách nhận biết etylamin trong phòng thí nghiệm
Etylamin có mùi khai đặc trưng giống mùi cá ươn. Trong phòng thí nghiệm, có thể nhận biết bằng giấy quỳ tím ẩm.
Khi cho etylamin tác dụng với dung dịch HCl, sẽ tạo thành muối etylamin hydroclorua kết tinh trắng. Phản ứng này tương tự như công thức phân tử của axit gluconic.
Qua 20 năm giảng dạy, tôi luôn nhắc học sinh phải cẩn thận khi làm thí nghiệm với etylamin vì tính bay hơi cao của nó.
Độc tính và cách bảo quản etylamin
Etylamin là chất độc, có thể gây kích ứng mạnh đường hô hấp và mắt. Cần bảo quản trong bình kín, tránh ánh sáng trực tiếp.
Nhiệt độ bảo quản tối ưu là dưới 25°C, tương tự như công thức phân tử của cao su thiên nhiên. Phòng chứa cần được thông gió tốt.
Khi tiếp xúc với etylamin, phải mang đầy đủ thiết bị bảo hộ như kính, găng tay và khẩu trang. Tránh xa nguồn lửa vì etylamin dễ cháy.
Kiến thức về công thức phân tử của etylamin giúp các em nắm vững cấu trúc phân tử, liên kết hóa học và tính chất đặc trưng của hợp chất amin bậc 1 này. Etylamin có vai trò quan trọng trong công nghiệp hóa chất, tổng hợp hữu cơ và ngành dược phẩm. Các phản ứng hóa học cơ bản của etylamin thể hiện rõ tính bazơ và khả năng phản ứng đa dạng với nhiều chất khác nhau.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

