Công thức hóa học của giấy và thông tin cấu tạo phân tử cellulose
Công thức hóa học của giấy bắt nguồn từ cellulose với cấu trúc phân tử phức tạp. Cellulose tạo nên khung sườn chính của tờ giấy thông qua các liên kết hóa học đặc biệt. Quá trình sản xuất giấy là chuỗi phản ứng hóa học biến đổi nguyên liệu thô thành sản phẩm cuối cùng.
Công thức hóa học của giấy
Giấy được tạo thành từ cellulose – một hợp chất hữu cơ phức tạp. Công thức hóa học của giấy chính là công thức của cellulose: (C6H10O5)n.
Trong đó:
- C6H10O5 là đơn vị lặp lại cơ bản của cellulose
- n là số lần lặp lại, thường từ 300-3000 đơn vị
Cellulose có cấu trúc mạch thẳng dài với các nhóm hydroxyl (-OH) xen kẽ. Các nhóm -OH này tạo liên kết hydrogen giữa các mạch cellulose với nhau.
Khi tôi giảng dạy về cellulose, tôi thường ví von nó như một chuỗi xích dài. Mỗi mắt xích là một đơn vị C6H10O5, chúng nối với nhau tạo thành sợi dài.
Quá trình sản xuất giấy sẽ biến đổi cellulose từ gỗ thành bột giấy. Các sợi cellulose được tách ra và sắp xếp lại thành tấm mỏng.
Theo nghiên cứu của Viện Khoa học và Công nghệ Việt Nam, cellulose chiếm khoảng 40-50% khối lượng của giấy thành phẩm, phần còn lại là các chất phụ gia khác.
Kinh nghiệm giảng dạy cho thấy học sinh dễ nhớ công thức này khi liên hệ với các vật dụng quen thuộc. Giấy vở, khăn giấy hay giấy báo đều có cùng thành phần cellulose cơ bản.
Thành phần và cấu tạo hóa học của giấy
Giấy là sản phẩm được tạo thành từ các sợi cellulose đan xen và liên kết với nhau. Thành phần hóa học của giấy bao gồm cellulose và một số chất phụ gia khác.
Các sợi cellulose trong giấy có nguồn gốc chủ yếu từ gỗ. Theo công thức hóa học của gỗ, cellulose chiếm khoảng 40-50% thành phần của gỗ.
Cấu tạo phân tử giấy được hình thành từ mạng lưới các sợi cellulose đan xen phức tạp. Các sợi này liên kết với nhau nhờ các liên kết hydro và van der Waals.
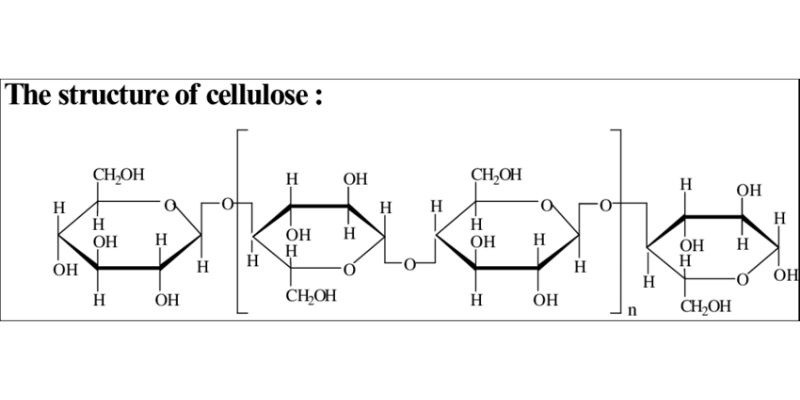
Cellulose – thành phần chính của giấy
Cellulose là một polysaccharide có công thức cellulose trong giấy là (C6H10O5)n. Trong đó n là số đơn vị glucose liên kết với nhau, thường từ 300-3000.
Mỗi đơn vị glucose trong cellulose có 3 nhóm hydroxyl (-OH). Các nhóm này tạo liên kết hydro với các phân tử cellulose khác.
Cấu trúc mạch thẳng của cellulose giúp các phân tử sắp xếp song song và tạo vùng tinh thể. Điều này làm cho giấy có độ bền cơ học cao.
Các thành phần phụ trong giấy
Ngoài cellulose, giấy còn chứa các chất phụ gia để cải thiện tính chất:
- Chất độn vô cơ (kaolin, CaCO3): Tăng độ trắng và mịn
- Chất kết dính (tinh bột, nhựa): Tăng độ bền
- Phẩm màu: Tạo màu sắc cho giấy
- Chất chống thấm: Giúp giấy không thấm nước
Các thành phần phụ chiếm khoảng 10-20% khối lượng giấy.
Liên kết hóa học trong phân tử cellulose
Trong phân tử cellulose tồn tại hai loại liên kết chính:
Liên kết β-1,4-glycoside nối các đơn vị glucose tạo thành mạch chính. Đây là liên kết cộng hóa trị bền vững.
Liên kết hydro giữa các nhóm -OH của các mạch cellulose. Loại liên kết này tạo ra cấu trúc sợi bền chắc.
Các liên kết van der Waals yếu cũng góp phần tạo nên độ bền của cấu trúc cellulose trong giấy.
Quy trình tạo thành giấy từ góc độ hóa học
Quá trình sản xuất giấy là chuỗi các phản ứng hóa học phức tạp. Tôi sẽ phân tích chi tiết từng công đoạn để các em dễ hiểu hơn về quy trình này.
Nguyên liệu thô và xử lý ban đầu
Nguyên liệu làm giấy chủ yếu là gỗ và các loại sợi thực vật. Gỗ được cắt nhỏ thành dăm rồi nghiền nát với nước tạo bột giấy thô.
Bột giấy thô sau đó được xử lý với dung dịch kiềm NaOH và Na2S ở nhiệt độ cao. Quá trình này giúp tách lignin ra khỏi cellulose – thành phần chính tạo nên sợi giấy.
Trong quá trình xử lý, người ta thường dùng công thức sắt 3 clorua làm chất xúc tác để tăng tốc độ phản ứng phân hủy lignin.
Các phản ứng hóa học chính trong quá trình sản xuất
Phản ứng hóa học tạo giấy bao gồm nhiều giai đoạn. Đầu tiên là phản ứng thủy phân lignin trong môi trường kiềm:
C9H10O2 + 2NaOH → C9H9O2Na + H2O + NaOH
Tiếp theo là phản ứng tẩy trắng bột giấy bằng H2O2 hoặc NaClO:
Cellulose-CHO + H2O2 → Cellulose-COOH + H2O
Các phản ứng này giúp loại bỏ tạp chất và tạo màu trắng cho giấy.
Công đoạn tạo thành giấy
Cách tạo thành giấy là công đoạn cuối cùng của quy trình. Bột giấy được pha loãng với nước tạo hỗn hợp đồng nhất.
Hỗn hợp được đưa qua máy xeo giấy, tạo thành màng mỏng trên lưới kim loại. Nước được loại bỏ bằng các con lăn ép và sấy khô.
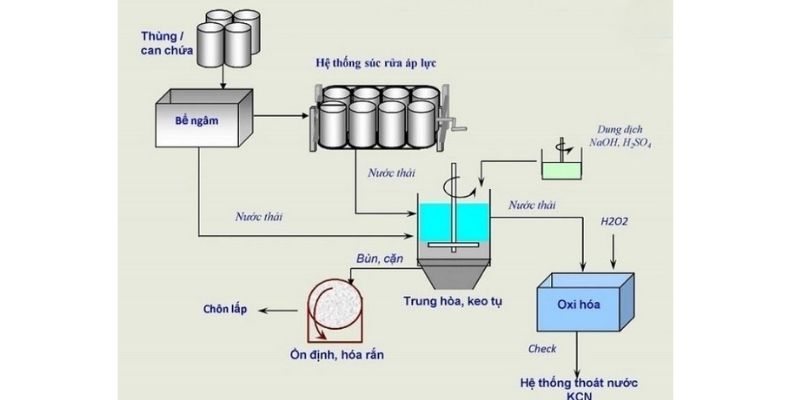
Cuối cùng, giấy được phủ thêm các chất như bột đá CaCO3, tinh bột để tăng độ trắng và độ mịn của bề mặt.
Cấu trúc phân tử và tính chất của cellulose trong giấy
Cellulose là thành phần chính tạo nên giấy, chiếm tới 90% khối lượng. Cấu trúc và tính chất của nó quyết định chất lượng giấy.
Giống như Công thức hóa học của cát, hóa học giấy cơ bản cần hiểu rõ về cấu trúc phân tử để ứng dụng hiệu quả.
Cấu trúc mạch phân tử cellulose
Cellulose có cấu trúc mạch thẳng dài, gồm các đơn vị glucose liên kết β-1,4-glycoside. Mỗi đơn vị glucose có công thức phân tử C6H10O5.
Thành phần cellulose trong giấy được tạo từ hàng nghìn đơn vị glucose xếp song song. Điều này tạo nên độ bền cơ học cao cho sợi giấy.
Tương tự như Công thức hóa học của kẽm, liên kết trong cellulose rất bền vững nhờ lực hydrogen giữa các mạch.
Các nhóm chức quan trọng
Cellulose chứa nhiều nhóm hydroxyl (-OH) trên mỗi đơn vị glucose. Các nhóm này tạo liên kết hydrogen giữa các mạch.
Nhóm acetal (-O-) liên kết các đơn vị glucose tạo thành mạch chính. Nhóm này bền trong môi trường kiềm nhưng dễ bị thủy phân trong axit.
Các nhóm chức này quyết định khả năng tương tác của cellulose với nước và các chất khác trong quá trình sản xuất giấy.
Tính chất hóa học đặc trưng
Cấu trúc phân tử cellulose giấy cho phép nó tham gia nhiều phản ứng hóa học quan trọng. Cellulose không tan trong nước nhưng có khả năng trương nở.
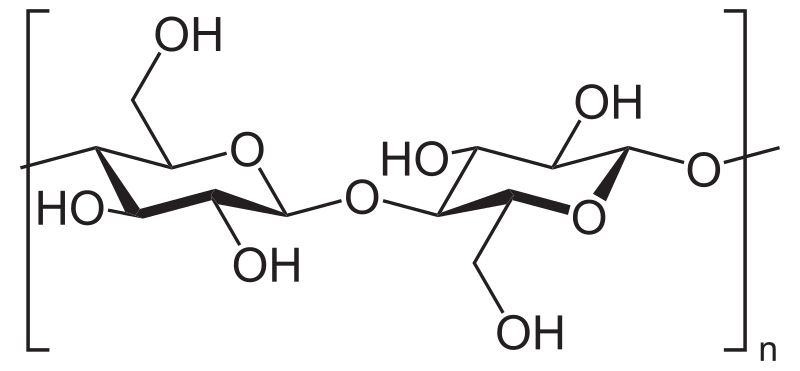
Phản ứng thủy phân cellulose xảy ra trong môi trường axit mạnh. Quá trình này phá vỡ liên kết glycoside tạo thành glucose.
Cellulose có khả năng tạo este với axit. Phản ứng này được ứng dụng để sản xuất giấy chống thấm và các loại giấy đặc biệt khác.
FAQ: Câu hỏi thường gặp về công thức hóa học của giấy
Giấy là vật liệu quen thuộc trong cuộc sống. Công thức hóa học của giấy chủ yếu là cellulose (C6H10O5)n và một số thành phần phụ gia khác.
Cellulose là một polymer tự nhiên được tạo thành từ các đơn vị glucose. Nó tạo nên cấu trúc sợi chắc chắn của giấy, tương tự như trong công thức hóa học của cơm.
Giấy tái chế có cấu tạo hóa học khác gì so với giấy thường?
Giấy tái chế vẫn giữ nguyên thành phần cellulose cơ bản. Tuy nhiên, quá trình tái chế làm đứt gãy một số liên kết polymer.
Sợi cellulose trong giấy tái chế ngắn hơn giấy nguyên sinh. Điều này khiến giấy tái chế có độ bền kém hơn, tương tự như công thức đá phấn khi bị nghiền nhỏ.
Tại sao giấy bị vàng khi để lâu?
Hiện tượng giấy ngả vàng xảy ra do phản ứng oxy hóa cellulose. Quá trình này tương tự như vàng có tính chất hóa học gì khi tiếp xúc với không khí.
Ánh sáng và độ ẩm cao thúc đẩy phản ứng oxy hóa. Các nhóm hydroxyl (-OH) trong cellulose bị oxy hóa tạo thành nhóm carbonyl (C=O) có màu vàng.
Làm thế nào để bảo quản giấy tốt nhất?
Giấy cần được bảo quản ở nơi khô ráo, thoáng mát. Nhiệt độ lý tưởng là 20-25°C và độ ẩm 45-55%.
Tránh ánh nắng trực tiếp chiếu vào giấy. Nên đặt giấy trong hộp kín hoặc túi nilon để hạn chế tiếp xúc với không khí.
Kinh nghiệm của tôi là thêm một vài gói hút ẩm silica gel vào hộp đựng giấy. Điều này giúp duy trì độ ẩm ổn định và kéo dài tuổi thọ của giấy.
Việc nghiên cứu công thức hóa học của giấy giúp chúng ta hiểu rõ bản chất của loại vật liệu quan trọng này. Cellulose với cấu trúc mạch dài và các liên kết đặc trưng tạo nên tính chất cơ bản của giấy. Quá trình sản xuất giấy là chuỗi phản ứng hóa học phức tạp từ nguyên liệu thô đến sản phẩm cuối cùng. Các kiến thức về cấu tạo và tính chất hóa học của giấy có ý nghĩa thiết thực trong việc sản xuất và bảo quản giấy tốt hơn.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

