Tìm hiểu công thức của thạch cao sống và ứng dụng trong thực tiễn
Công thức của thạch cao sống là kiến thức quan trọng trong hóa học vô cơ. Thạch cao sống có cấu trúc phân tử đặc biệt với nước kết tinh. Quá trình chuyển hóa giữa thạch cao sống và thạch cao khan diễn ra theo quy luật. Các phương pháp điều chế thạch cao sống đòi hỏi kỹ thuật chính xác.
Công thức của thạch cao sống
Thạch cao sống có công thức hóa học là CaSO4.1/2H2O. Đây là một hợp chất vô cơ phổ biến trong tự nhiên và công nghiệp.
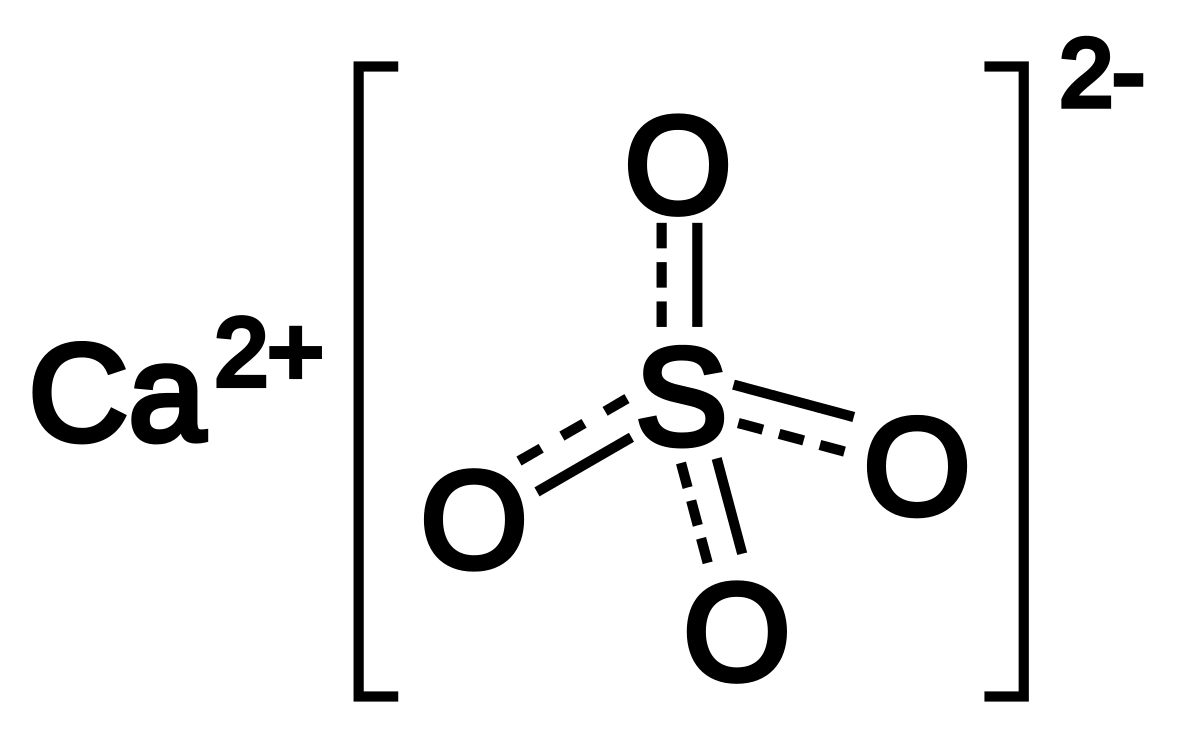
Công thức của thạch cao sống bao gồm các thành phần:
– Ca: Canxi
– SO4: Gốc sunfat
– 1/2H2O: Nửa phân tử nước kết tinh
Trong quá trình giảng dạy, tôi thường giúp học sinh ghi nhớ công thức này bằng cách liên tưởng đến “nửa ly nước”. Thạch cao sống có công thức là CaSO4 kết hợp với 1/2 phân tử nước, giống như một ly nước uống dở.
Khi nung nóng thạch cao sống ở 650°C, nó sẽ mất hoàn toàn nước kết tinh và chuyển thành CaSO4 khan. Ngược lại, khi thêm nước vào thạch cao khan, nó sẽ kết hợp với nước tạo thành thạch cao sống CaSO4.1/2H2O.
Một mẹo nhỏ để phân biệt: Thạch cao sống chỉ chứa 1/2 phân tử nước, trong khi thạch cao thường (CaSO4.2H2O) chứa 2 phân tử nước kết tinh. Điều này giúp học sinh dễ dàng phân biệt hai dạng thạch cao phổ biến.
Cấu tạo và thành phần hóa học của thạch cao sống CaSO4.2H2O
Thạch cao sống CaSO4.2H2O là một khoáng chất phổ biến trong tự nhiên. Nó có cấu trúc tinh thể đặc trưng với các lớp ion Ca2+ và SO42- xen kẽ nhau.
Cấu trúc này tạo nên một mạng tinh thể ba chiều phức tạp. Các phân tử nước kết tinh nằm giữa các lớp ion, đóng vai trò quan trọng trong việc ổn định cấu trúc.
Tương tự như công thức đá vôi, thạch cao sống có cấu tạo vững chắc. Điều này giúp nó trở thành nguyên liệu quan trọng trong công nghiệp xây dựng.
Phân tử thạch cao sống gồm những thành phần nào
Thạch cao sống có công thức phân tử là CaSO4.2H2O, bao gồm:
– Ion canxi (Ca2+): Tạo nên khung cấu trúc chính
– Ion sulfat (SO42-): Liên kết với ion canxi tạo thành mạng tinh thể
– Phân tử nước (H2O): Có 2 phân tử nước kết tinh trong mỗi đơn vị công thức
Các thành phần này kết hợp với tỉ lệ mol 1:1:2 tạo nên cấu trúc ổn định của thạch cao sống.
Liên kết hóa học trong thạch cao sống
Trong thạch cao sống tồn tại hai loại liên kết chính. Liên kết ion mạnh mẽ giữa Ca2+ và SO42- tạo nên khung cấu trúc vững chắc.
Liên kết hydro giữa các phân tử nước và ion sulfat đóng vai trò ổn định cấu trúc. Chúng tạo thành một mạng lưới liên kết ba chiều.
Sự kết hợp của hai loại liên kết này mang lại độ bền cao cho tinh thể thạch cao sống. Đây là cơ sở cho các ứng dụng của nó trong thực tế.
Vai trò của nước kết tinh trong thạch cao sống
Nước kết tinh đóng vai trò then chốt trong cấu trúc thạch cao sống. Nó tạo ra các cầu nối hydro giữa các ion, làm tăng độ bền của tinh thể.
Khi nung nóng và mất nước kết tinh, cấu trúc tinh thể bị phá vỡ. Quá trình này tạo ra thạch cao khan CaSO4 với tính chất hoàn toàn khác.
Trong quá trình 20 năm giảng dạy, tôi thường ví von nước kết tinh như xi măng. Nó gắn kết các thành phần lại với nhau tạo nên một khối thống nhất.
Quá trình chuyển hóa giữa thạch cao sống và thạch cao khan
Thạch cao sống và thạch cao khan có mối quan hệ chuyển hóa qua lại thông qua phản ứng thuận nghịch với nước. Quá trình này diễn ra dưới tác động của nhiệt độ và áp suất khác nhau.
Khi nung nóng thạch cao sống ở 120-180°C, nó sẽ mất một phần nước và chuyển thành thạch cao khan. Đây là phản ứng có thể đảo ngược khi thêm nước vào thạch cao khan.
Theo công thức của thạch cao nung, phản ứng chuyển hóa được biểu diễn:
CaSO4.2H2O ⇌ CaSO4.1/2H2O + 3/2H2O
Phản ứng mất nước của thạch cao sống
Phản ứng mất nước xảy ra theo hai giai đoạn chính. Giai đoạn đầu diễn ra ở 120°C, thạch cao sống mất 75% lượng nước kết tinh.
Giai đoạn thứ hai xảy ra ở 180°C, phần nước còn lại tiếp tục tách ra. Quá trình này tạo thành thạch cao khan có công thức CaSO4.
Nhiệt độ là yếu tố quyết định tốc độ phản ứng. Ở nhiệt độ càng cao, phản ứng mất nước diễn ra càng nhanh.

Sự khác biệt về cấu trúc và tính chất
Thạch cao sống có cấu trúc tinh thể monoclinic, chứa hai phân tử nước trong mạng tinh thể. Các phân tử nước liên kết chặt chẽ với ion Ca2+ và SO42-.
Thạch cao khan có cấu trúc tinh thể orthorhombic, chỉ chứa nửa phân tử nước. Điều này làm cho nó có khả năng hút ẩm mạnh hơn thạch cao sống.
Ứng dụng trong thực tế
Trong xây dựng, thạch cao khan được sử dụng làm vật liệu trát tường và trang trí nội thất. Khi trộn với nước, nó đông cứng nhanh và tạo bề mặt nhẵn mịn.
Trong y tế, thạch cao khan dùng làm băng bó cố định xương gãy. Tính chất đông cứng nhanh giúp cố định vị trí xương hiệu quả.
Trong công nghiệp, thạch cao khan được dùng làm chất độn trong sản xuất giấy và nhựa. Nó cải thiện độ bền và tính chất cơ học của sản phẩm.
Phương pháp điều chế và sản xuất thạch cao sống
Thạch cao sống được điều chế từ quá trình nung nóng thạch cao tự nhiên ở nhiệt độ thích hợp. Công thức của thạch cao sống là CaSO4.2H2O → CaSO4.1/2H2O + 3/2H2O.
Quá trình thạch cao sống nung diễn ra ở nhiệt độ 120-180°C, tạo thành sản phẩm bán hydrat. Phản ứng này có thể kết hợp với nước vôi trong công thức để tạo ra vữa xây dựng.
Trong phòng thí nghiệm, việc điều chế thạch cao sống được thực hiện bằng cách nung thạch cao dihydrat trong bình sấy. Quá trình này cần kiểm soát chặt chẽ nhiệt độ và thời gian.
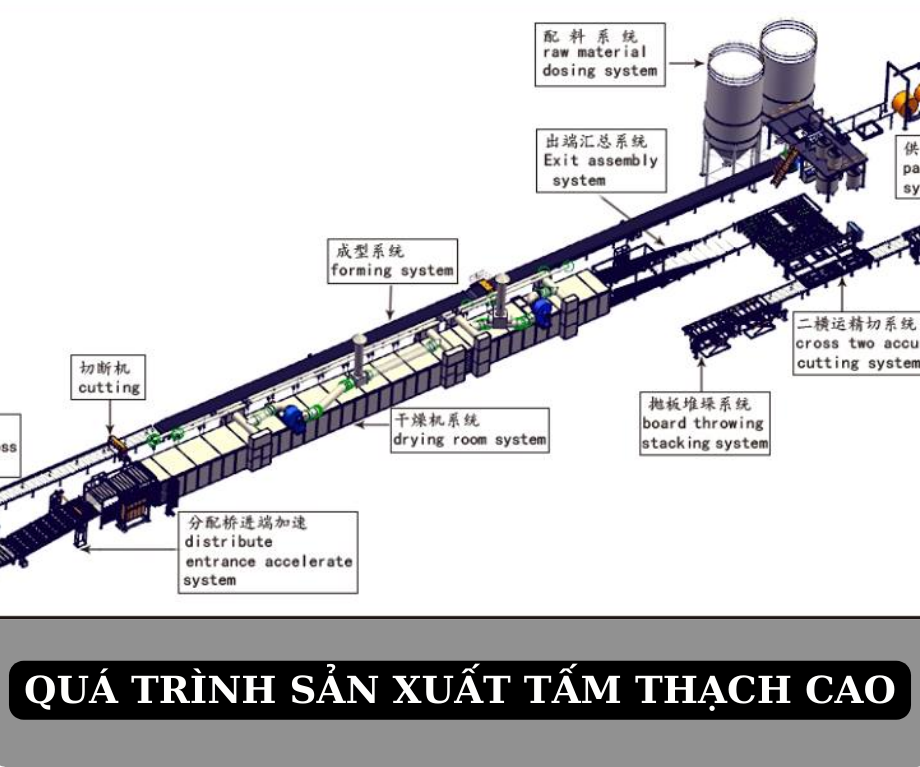
Quy trình sản xuất công nghiệp
Quy trình sản xuất thạch cao sống công nghiệp bắt đầu từ khâu nghiền nhỏ đá thạch cao tự nhiên. Kích thước hạt càng nhỏ, hiệu suất phản ứng càng cao.
Sau đó, nguyên liệu được đưa vào lò nung quay hoặc lò tĩnh. Nhiệt độ nung được kiểm soát tự động bằng các cảm biến nhiệt.
Sản phẩm sau nung được làm nguội nhanh và nghiền mịn. Quá trình này giúp tạo ra bột thạch cao sống có độ mịn và chất lượng đồng đều.
Các yếu tố ảnh hưởng đến chất lượng sản phẩm
Nhiệt độ nung là yếu tố quan trọng nhất quyết định chất lượng thạch cao sống. Nhiệt độ quá cao sẽ tạo thành thạch cao khan không có khả năng đông kết.
Độ ẩm của nguyên liệu ban đầu cũng ảnh hưởng lớn đến quá trình nung. Nguyên liệu càng khô, năng lượng tiêu tốn càng ít và hiệu suất càng cao.
Thời gian nung và tốc độ làm nguội cũng cần được kiểm soát chặt chẽ. Quá trình làm nguội nhanh giúp sản phẩm có cấu trúc vi mô tốt hơn.
Kích thước hạt của sản phẩm cuối cùng ảnh hưởng trực tiếp đến khả năng đông kết. Độ mịn càng cao, tốc độ đông kết càng nhanh và độ bền càng tốt.
FAQ: Câu hỏi thường gặp về thạch cao sống
Thạch cao sống là một vật liệu phổ biến trong xây dựng và công nghiệp. Tôi sẽ giải đáp những thắc mắc thường gặp về loại vật liệu này.
Thạch cao sống có độc không?
Thạch cao sống không độc hại với con người khi tiếp xúc thông thường. Tuy nhiên, bụi thạch cao có thể gây kích ứng đường hô hấp nếu hít phải nhiều.
Khi làm việc với thạch cao, cần đeo khẩu trang và găng tay bảo hộ. Điều này giúp tránh các vấn đề về hô hấp và da.
Thạch cao sống có thể tái sử dụng không?
Thạch cao sống sau khi đã đông cứng không thể tái sử dụng trực tiếp. Quá trình hydrat hóa là không thể đảo ngược.
Tuy nhiên, thạch cao thải có thể được tái chế thành nguyên liệu mới. Các nhà máy sẽ nghiền và nung lại thành thạch cao ban đầu.
Cách bảo quản thạch cao sống đúng cách
Thạch cao cần được bảo quản trong môi trường khô ráo, thoáng mát. Nhiệt độ lý tưởng là 20-25°C.
Đóng gói thạch cao trong bao bì kín, tránh tiếp xúc với không khí ẩm. Độ ẩm cao sẽ làm thạch cao đông cứng trước khi sử dụng.
Nên đặt thạch cao trên kệ cao, tránh tiếp xúc trực tiếp với nền nhà. Điều này ngăn ẩm từ mặt đất thấm vào vật liệu.
Việc nắm vững công thức của thạch cao sống giúp người học hiểu rõ bản chất hóa học của vật liệu quan trọng này. Thạch cao sống CaSO4.2H2O có cấu trúc tinh thể đặc biệt với sự tham gia của phân tử nước. Quá trình chuyển hóa giữa thạch cao sống và thạch cao khan diễn ra theo quy luật nhiệt động học rõ ràng. Các phương pháp điều chế và sản xuất thạch cao sống đã được tối ưu hóa trong công nghiệp hiện đại.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

