Phân tích công thức của propen và các tính chất hóa học cơ bản
Công thức của propen là nền tảng để hiểu về hydrocacbon không no. Propen có cấu trúc đơn giản với liên kết đôi C=C đặc trưng. Chất này đóng vai trò quan trọng trong công nghiệp hóa dầu và sản xuất polymer. Các phản ứng hóa học của propen minh họa rõ tính chất của anken.
Công thức của propen
Propen là một hydrocacbon không no thuộc dãy ankene có 3 nguyên tử cacbon. Công thức của propen là C3H6 hay CH3-CH=CH2.
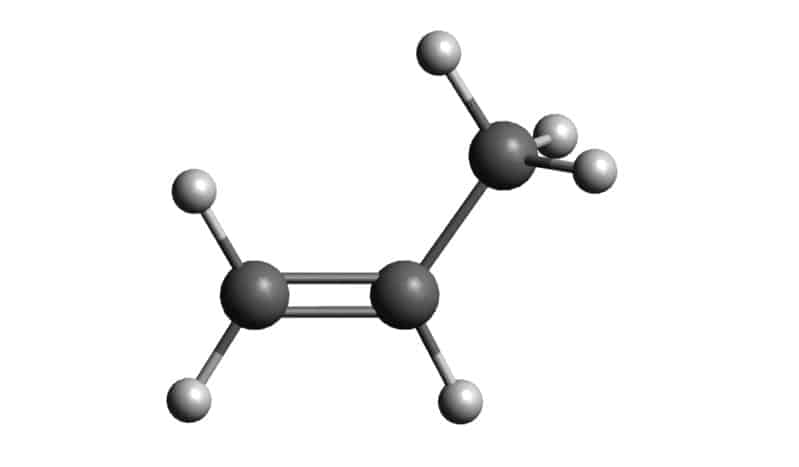
Trong cấu trúc phân tử propen, các nguyên tử được liên kết với nhau theo thứ tự:
- Một nhóm metyl (CH3-)
- Một liên kết đôi (-CH=CH2)
Công thức propen là gì? Đây là một câu hỏi thường gặp của học sinh khi học về ankene. Propen có công thức phân tử C3H6 và công thức cấu tạo CH3-CH=CH2.
Tôi thường giúp học sinh ghi nhớ công thức này bằng cách phân tích:
- C3: có 3 nguyên tử cacbon
- H6: có 6 nguyên tử hydro
- Liên kết đôi ở vị trí số 2
Propen là một chất khí không màu ở điều kiện thường, có mùi đặc trưng. Nó được sử dụng rộng rãi trong công nghiệp hóa chất để sản xuất polypropylene và nhiều hợp chất hữu cơ khác.
Khi giải các bài tập về propen, học sinh cần chú ý:
- Số liên kết đôi: 1
- Số liên kết đơn: 7
- Góc liên kết tại cacbon số 2: xấp xỉ 120°
Cấu tạo phân tử và đặc điểm của propen
Propen là một hydrocacbon không no thuộc dãy olefin với liên kết đôi C=C. Cấu trúc phân tử propen có nhiều điểm đặc biệt cần tìm hiểu kỹ.
Tôi sẽ phân tích chi tiết về công thức phân tử, cấu tạo và cấu trúc không gian của propen. Đây là những kiến thức nền tảng giúp hiểu rõ tính chất của hợp chất này.
Công thức phân tử của propen
Công thức phân tử của propen là C3H6. Propen có cấu tạo tương tự như propan công thức nhưng ít hơn 2 nguyên tử H.
So với propan (C3H8), propen mất đi 2 nguyên tử H do có liên kết đôi C=C. Điều này làm cho propen có tính chất hóa học khác biệt.
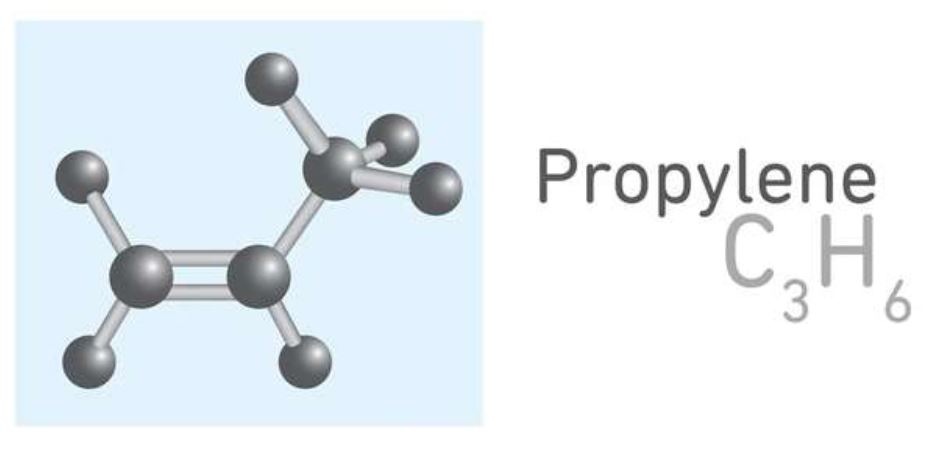
Công thức cấu tạo của propen
Công thức cấu tạo của propen hay còn gọi là propylene công thức được viết là CH3-CH=CH2.
Trong phân tử có một liên kết đôi C=C ở vị trí carbon số 2. Nhóm methyl (-CH3) gắn vào carbon đầu tiên.
Các electron π trong liên kết đôi C=C làm cho propen có khả năng tham gia phản ứng cộng. Đây là đặc điểm quan trọng của hợp chất này.
Cấu trúc không gian của phân tử propen
Phân tử propen có dạng phẳng ở vùng liên kết đôi C=C. Các nguyên tử carbon và hydro nằm trên cùng một mặt phẳng.
Góc liên kết giữa các nguyên tử carbon là 120°. Điều này phù hợp với lai hóa sp2 của carbon trong liên kết đôi.
Nhóm methyl (-CH3) có thể xoay tự do quanh trục liên kết đơn C-C. Tuy nhiên liên kết đôi C=C không thể xoay được.
Tính chất vật lý và ứng dụng của propen
Propen là một hydrocacbon không no thuộc dãy olefin, có công thức phân tử C3H6. Nó là một chất khí không màu ở điều kiện thường và có mùi đặc trưng. Cấu trúc phân tử của propen tương tự như propin công thức nhưng có liên kết đôi thay vì liên kết ba.
Các tính chất vật lý cơ bản
Propen tồn tại ở dạng khí không màu ở nhiệt độ và áp suất thường. Nhiệt độ sôi của propen là -47,6°C, thấp hơn so với các hợp chất tương tự như công thức của isopren.
Khối lượng riêng của propen ở điều kiện chuẩn là 1,915 kg/m3, nặng hơn không khí. Điều này khiến propen thường tích tụ ở các vùng thấp khi rò rỉ.
Propen có độ tan trong nước rất thấp, chỉ khoảng 200mg/L ở 20°C. Tuy nhiên, nó tan tốt trong các dung môi hữu cơ như benzen, cloroform và etanol.
Ứng dụng trong công nghiệp và đời sống
Propen là một trong những nguyên liệu quan trọng nhất của ngành công nghiệp hóa dầu. Nó được sử dụng để sản xuất polypropylene – một loại nhựa phổ biến dùng làm bao bì, đồ gia dụng.

Trong công nghiệp hóa chất, propen là nguyên liệu để tổng hợp nhiều hợp chất quan trọng như propylene oxide, acrylonitrile và isopropanol. Các sản phẩm này được dùng để sản xuất chất tẩy rửa, sợi tổng hợp.
Propen còn được sử dụng làm nhiên liệu trong một số động cơ đặc biệt. Khi trộn với propan, nó tạo thành hỗn hợp LPG thương mại dùng trong đun nấu và sưởi ấm.
Phản ứng hóa học đặc trưng của propen
Công thức của propen CH3-CH=CH2 là một anken không no với liên kết đôi C=C. Đây là một chất khí không màu ở điều kiện thường, dễ dàng tham gia các phản ứng cộng và oxi hóa.
Tương tự như cấu tạo benzen, cấu tạo propen có tính chất đặc trưng của hợp chất không no. Propen có thể tham gia nhiều loại phản ứng hóa học quan trọng.
Phản ứng cộng
Propen dễ dàng tham gia phản ứng cộng với các chất như H2, Br2, HCl theo quy tắc Markovnikov. Phản ứng này xảy ra do liên kết đôi C=C bị bẻ gãy.
Ví dụ phản ứng cộng HCl vào propen:
CH3-CH=CH2 + HCl → CH3-CHCl-CH3
Tôi thường giải thích cho học sinh bằng cách so sánh liên kết đôi như một chiếc cầu có thể bị phá vỡ để tạo ra sản phẩm mới.
Phản ứng oxi hóa
Propen có thể bị oxi hóa bởi KMnO4 hoặc O2 tạo thành nhiều sản phẩm khác nhau. Với KMnO4 loãng, lạnh sẽ tạo ra diol:
CH3-CH=CH2 + [O] + H2O → CH3-CHOH-CH2OH
Khi oxi hóa mạnh bằng KMnO4 đặc, nóng, liên kết đôi bị phá vỡ tạo thành axit cacboxylic và CO2:
CH3-CH=CH2 + [O] → CH3COOH + CO2 + H2O
Phản ứng trùng hợp
Propen có thể tham gia phản ứng trùng hợp tạo polypropylene – một loại nhựa quan trọng, tương tự như công thức phân tử của phenol có thể tạo nhựa phenol formaldehyde.
nCH3-CH=CH2 → [-CH2-CH(CH3)-]n
Phản ứng trùng hợp xảy ra khi có xúc tác và áp suất cao. Sản phẩm polypropylene được ứng dụng rộng rãi trong sản xuất bao bì, đồ gia dụng.
Trong quá trình giảng dạy, tôi thường lấy ví dụ về các sản phẩm nhựa quen thuộc để học sinh dễ hình dung về ứng dụng của phản ứng này.
FAQ: Câu hỏi thường gặp về propen
Propen là một hydrocacbon không no thuộc nhóm olefin. Tôi sẽ giải đáp một số thắc mắc phổ biến về hợp chất này.
Propen có độc không?
Propen có độc tính thấp nhưng không được coi là vô hại. Khi tiếp xúc ở nồng độ cao, khí này có thể gây ngạt thở do thiếu oxy.
Theo nghiên cứu của Viện An toàn và Sức khỏe Nghề nghiệp Mỹ (NIOSH), tiếp xúc với propen ở nồng độ trên 2000ppm có thể gây chóng mặt và buồn nôn. Tương tự như axit propionic có công thức là, propen cần được bảo quản và sử dụng cẩn thận.
Propen có thể tự bốc cháy không?
Không giống như công thức của etyl propionat, propen không tự bốc cháy ở điều kiện thường. Tuy nhiên, đây là chất dễ cháy và có thể phát nổ khi tiếp xúc với nguồn lửa.
Nhiệt độ tự bốc cháy của propen là 497°C. Điều này tương tự như công thức phèn nhôm khi bị nung nóng ở nhiệt độ cao.
Làm thế nào để bảo quản propen an toàn?
Propen cần được bảo quản trong bình chứa kín, tránh ánh nắng trực tiếp. Tương tự như freon là gì, khí này phải được lưu trữ ở nơi thoáng mát.
Nhiệt độ bảo quản tối ưu là dưới 50°C. Bình chứa cần được kiểm tra định kỳ về rò rỉ và tình trạng van khóa.
Khu vực lưu trữ phải được trang bị hệ thống phòng cháy chữa cháy và thiết bị phát hiện rò rỉ khí tự động.
Kiến thức về công thức của propen là nền tảng quan trọng trong chương trình hóa học hữu cơ. Propen với cấu trúc phân tử đơn giản C3H6 và liên kết đôi C=C đặc trưng tạo nên nhiều tính chất hóa học độc đáo. Các phản ứng cộng, oxi hóa và trùng hợp của propen đóng vai trò then chốt trong công nghiệp hóa chất. Việc nắm vững cấu tạo và tính chất của propen giúp học sinh dễ dàng tiếp cận các hợp chất hữu cơ phức tạp hơn.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

