Điểm qua công thức của methanol và các tính chất hóa học cơ bản
Công thức của methanol là nền tảng để hiểu về cấu trúc phân tử rượu đơn giản nhất. Methanol đóng vai trò quan trọng trong công nghiệp hóa chất và đời sống. Chất này có nhiều ứng dụng hữu ích nhưng cũng tiềm ẩn độc tính cao với cơ thể.
Công thức của methanol
Methanol là một hợp chất hữu cơ đơn giản nhất trong dãy ancol no, đơn chức, mạch hở. Công thức của methanol là CH3OH.
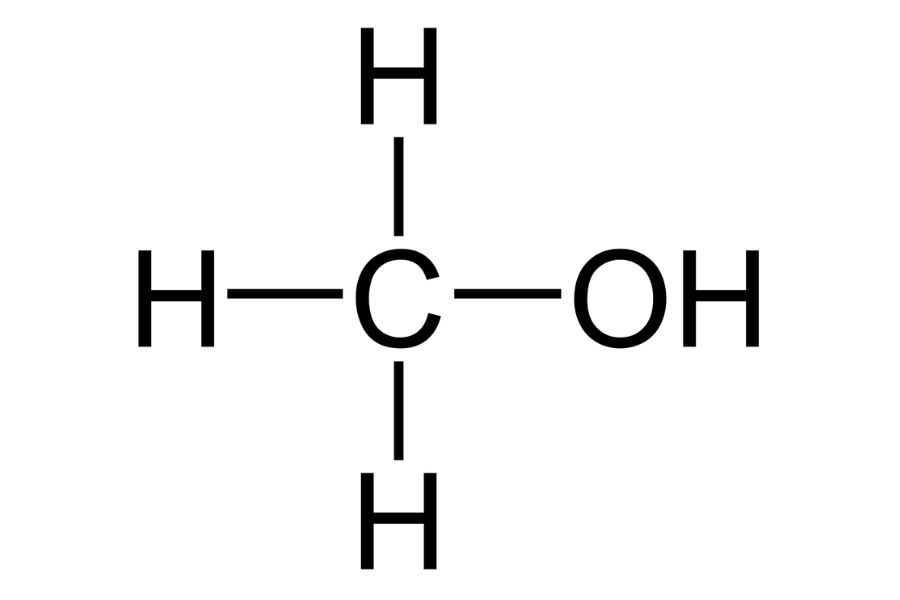
Công thức cấu tạo của methanol có thể viết như sau:
CH3-OH
Trong đó:
- C<h3>là gốc methyl</h3>- OH: là nhóm hydroxyl (nhóm chức)
Với kinh nghiệm 20 năm giảng dạy, tôi thường giúp học sinh ghi nhớ methanol công thức bằng cách liên tưởng đơn giản: Methanol chỉ có 1 nguyên tử carbon (CH3) gắn với 1 nhóm OH.
Ví dụ thực tế: Methanol thường được sử dụng làm dung môi trong công nghiệp. Tuy nhiên, đây là chất độc nguy hiểm, có thể gây mù mắt hoặc tử vong nếu uống phải.
Để phân biệt với ethanol (rượu uống), methanol có mùi cồn nhẹ hơn và không được phép sử dụng trong đồ uống. Khi làm bài tập, học sinh cần chú ý phân biệt rõ công thức của methanol (CH3OH) và ethanol (C2H5OH).
Cấu tạo và tính chất hóa học của methanol
Methanol là một hợp chất hữu cơ đơn giản nhất trong dãy ancol. Nó có vai trò quan trọng trong công nghiệp hóa chất và đời sống. Tôi sẽ phân tích chi tiết về cấu tạo và tính chất của methanol.

Công thức phân tử và cấu tạo của methanol
Công thức phân tử của methanol là CH3OH. Phân tử này có cấu trúc tương tự như công thức cấu tạo của metan nhưng một nguyên tử H được thay thế bằng nhóm OH.
Công thức cấu tạo của methanol thể hiện rõ sự sắp xếp không gian của các nguyên tử. Nguyên tử C ở trung tâm liên kết với 3 nguyên tử H và 1 nhóm OH.
Liên kết hóa học trong phân tử methanol
Trong phân tử methanol tồn tại hai loại liên kết chính. Liên kết C-H là liên kết cộng hóa trị không phân cực, bền vững với độ dài khoảng 0,109 nm.
Liên kết C-O và O-H có tính phân cực mạnh do độ âm điện của O lớn hơn C và H. Điều này tạo nên tính phân cực cho phân tử methanol.
Các tính chất vật lý đặc trưng
Methanol là chất lỏng không màu ở điều kiện thường. Nhiệt độ sôi của methanol là 64,7°C, thấp hơn nước do khối lượng phân tử nhỏ.
Do có nhóm OH phân cực, methanol tan vô hạn trong nước. Nó cũng là dung môi tốt cho nhiều chất hữu cơ.
Mật độ methanol là 0,792 g/mL ở 20°C, nhẹ hơn nước. Cấu tạo methanol quyết định các tính chất vật lý đặc trưng này.
Phản ứng hóa học cơ bản của methanol
Methanol tham gia phản ứng thế H trong nhóm OH tạo thành các este. Phản ứng này thường xảy ra khi có xúc tác axit.
Methanol cũng có thể bị oxi hóa thành formaldehyt CH2O. Phản ứng này xảy ra khi đun nóng với CuO hoặc không khí.
Trong điều kiện thích hợp, methanol có thể bị khử thành metan CH4. Đây là phản ứng quan trọng trong công nghiệp.
Ứng dụng và sản xuất methanol trong công nghiệp
Methanol là một hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Nó được sản xuất với quy mô lớn và có nhiều ứng dụng đa dạng. Tôi sẽ phân tích chi tiết về quy trình sản xuất và ứng dụng của methanol.
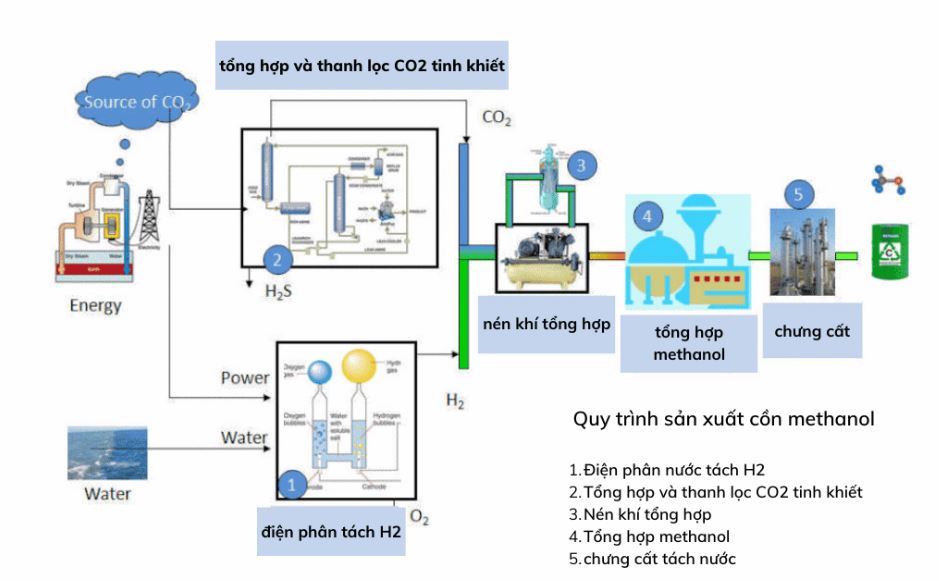
Quy trình sản xuất methanol
Methanol được sản xuất chủ yếu từ khí tổng hợp (CO và H2) qua phản ứng xúc tác:
CO + 2H2 → CH3OH
Quá trình này diễn ra ở nhiệt độ 250-300°C, áp suất 50-100 atm với xúc tác CuO-ZnO-Al2O3. Hiệu suất phản ứng đạt 99% nhờ kiểm soát chặt chẽ các thông số kỹ thuật.
Trong 20 năm giảng dạy, tôi thường ví von phản ứng này như “cuộc hẹn hò” giữa CO và H2 dưới sự mai mối của xúc tác để tạo thành methanol.
Các ứng dụng chính của methanol
Methanol là nguyên liệu quan trọng để tổng hợp nhiều hợp chất hữu cơ như công thức của metyl fomat và công thức của metyl metacrylat.
Nó còn được sử dụng làm dung môi trong công nghiệp sơn, keo dán và chất tẩy rửa. Methanol cũng là nhiên liệu sạch thay thế xăng dầu.
Trong ngành dược phẩm, methanol đóng vai trò dung môi chiết xuất và tinh chế các hoạt chất sinh học.
Lưu ý khi sử dụng methanol an toàn
Methanol có độc tính cao nên cần tuân thủ nghiêm ngặt quy tắc an toàn. Tránh tiếp xúc trực tiếp với da và hít phải hơi methanol.
Khi làm việc với methanol phải đeo găng tay, kính bảo hộ và khẩu trang. Nơi làm việc cần thông thoáng, tránh xa nguồn lửa.
Trong phòng thí nghiệm trường học, tôi luôn nhắc học sinh: “Methanol như con mèo xinh đẹp nhưng có móng vuốt sắc – phải biết cách vuốt ve đúng cách”.
Tác động của methanol đối với sức khỏe và môi trường
Methanol là một chất độc nguy hiểm có thể gây tổn thương nghiêm trọng cho cơ thể. Công thức của methanol CH3OH cho thấy đây là rượu đơn giản nhất trong dãy đồng đẳng. Tương tự như công thức của phenol, methanol có nhóm -OH nhưng độc tính cao hơn nhiều lần.

Độc tính của methanol
Methanol có thể gây ngộ độc qua đường hô hấp, tiêu hóa và da. Khi vào cơ thể, methanol bị chuyển hóa thành formaldehyde và axit formic gây tổn thương não.
Các triệu chứng ngộ độc methanol thường xuất hiện sau 12-24 giờ tiếp xúc. Người bệnh có thể bị đau đầu, chóng mặt, buồn nôn và rối loạn thị giác.
Trong trường hợp nặng, methanol có độc tính cao có thể dẫn đến mù lòa, hôn mê và tử vong nếu không được điều trị kịp thời.
Cách xử lý khi tiếp xúc với methanol
Khi da tiếp xúc với methanol, cần rửa ngay bằng nước sạch trong 15-20 phút. Tháo bỏ quần áo nhiễm methanol và đưa nạn nhân đến cơ sở y tế.
Nếu hít phải hơi methanol, nhanh chóng đưa nạn nhân ra khỏi khu vực nhiễm độc. Đặt nạn nhân nằm nghiêng một bên, giữ ấm và theo dõi hô hấp.
Trường hợp uống phải methanol là nguy hiểm nhất, cần gây nôn ngay và đưa đến bệnh viện càng sớm càng tốt.
Ảnh hưởng môi trường
Methanol có khả năng phân hủy sinh học cao trong môi trường. Tuy nhiên, nồng độ methanol cao có thể gây độc cho sinh vật thủy sinh.
Khi rò rỉ vào đất, methanol dễ dàng thấm xuống nước ngầm. Điều này có thể ảnh hưởng đến nguồn nước sinh hoạt của con người.
Methanol trong không khí sẽ phân hủy thành CO2 và H2O dưới tác dụng của ánh sáng mặt trời. Quá trình này góp phần làm tăng hiệu ứng nhà kính.
FAQ: Câu hỏi thường gặp về methanol
Methanol là hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Công thức methanol là CH3OH, một dạng cồn đơn giản nhất trong dãy đồng đẳng ancol. Tôi sẽ giải đáp một số thắc mắc phổ biến về hợp chất này.
Phân biệt methanol với ethanol
Methanol và ethanol có nhiều điểm khác biệt cơ bản. Công thức hóa học của methanol là CH3OH, trong khi ethanol có công thức C2H5OH. Methanol có độc tính cao hơn nhiều so với ethanol.
Về mặt tính chất vật lý, methanol có nhiệt độ sôi thấp hơn (64,7°C) so với ethanol (78,37°C). Điều này giúp phân biệt hai chất trong quá trình chưng cất phân đoạn.
Trong thực tế, methanol thường được sử dụng làm dung môi công nghiệp và nguyên liệu tổng hợp hóa chất như công thức của trimetylamin. Ethanol an toàn hơn và được dùng trong đồ uống, mỹ phẩm.
Cách bảo quản methanol đúng cách
Methanol cần được bảo quản trong bình kín, tránh ánh sáng trực tiếp và nhiệt độ cao. Nhiệt độ bảo quản lý tưởng là 15-25°C.
Không nên để methanol gần các chất oxy hóa mạnh như công thức của soda. Khi tiếp xúc với không khí, methanol có thể hấp thụ hơi nước và suy giảm nồng độ.
Bình chứa methanol phải được dán nhãn cảnh báo rõ ràng và để ở nơi khô ráo, thoáng mát. Tránh để gần nguồn lửa vì methanol dễ cháy.
Xử lý sự cố tràn đổ methanol
Khi methanol bị đổ, cần nhanh chóng thực hiện các biện pháp xử lý an toàn. Đầu tiên, di tản mọi người ra khỏi khu vực và thông gió.
Dùng cát hoặc vật liệu thấm hút để ngăn methanol lan rộng. Tuyệt đối không dùng nước để rửa trôi vì sẽ làm methanol phát tán.
Thu gom methanol đã thấm vào vật liệu và đựng trong thùng kín riêng biệt. Sau đó liên hệ đơn vị xử lý chất thải nguy hại để tiêu hủy đúng quy định.
Chất hữu cơ với công thức của methanol đóng vai trò quan trọng trong công nghiệp hóa chất và đời sống. Methanol có cấu tạo phân tử đơn giản nhưng tính chất hóa học đa dạng, ứng dụng rộng rãi trong sản xuất nhiên liệu và dung môi. Tuy nhiên, người sử dụng cần tuân thủ nghiêm ngặt các quy tắc an toàn do tính độc cao của methanol đối với cơ thể và môi trường.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

