Điểm qua công thức criolit và ứng dụng trong sản xuất nhôm công nghiệp
Công thức criolit đóng vai trò then chốt trong ngành luyện kim nhôm hiện đại. Criolit tồn tại dưới hai dạng tự nhiên và nhân tạo với những đặc tính riêng biệt. Chất này giúp hạ thấp nhiệt độ nóng chảy của quặng nhôm trong quá trình điện phân.
Công thức criolit là Na3AlF6
Criolit là một khoáng chất tự nhiên có công thức criolit là Na3AlF6. Đây là một hợp chất phức của natri, nhôm và flo.
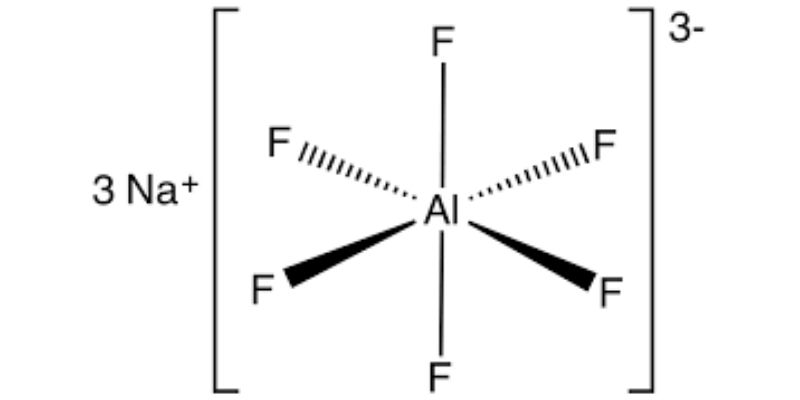 Công thức criolit là Na3AlF6
Công thức criolit là Na3AlF6Trong công thức Na3AlF6:
- Na: là nguyên tố Natri, hóa trị +1
- Al: là nguyên tố Nhôm, hóa trị +3
- F: là nguyên tố Flo, hóa trị -1
Công thức của criolit Na3AlF6 cho thấy trong 1 phân tử có:
- 3 nguyên tử Na+
- 1 nguyên tử Al3+
- 6 nguyên tử F-
Tôi thường giúp học sinh nhớ công thức này bằng cách phân tích cấu tạo: Na3[AlF6]. Trong đó [AlF6] là phức chất âm, mang điện tích -3, cần 3 ion Na+ để trung hòa.
Criolit có vai trò quan trọng trong công nghiệp luyện nhôm. Nó được dùng làm chất điện ly trong quá trình điện phân nhôm oxit để sản xuất nhôm kim loại.
Khi dạy về criolit, tôi thường nhấn mạnh với học sinh rằng đây là một trong những ví dụ điển hình về ứng dụng của hóa học trong công nghiệp khai thác kim loại.
Cấu tạo và tính chất của criolit trong tự nhiên
Criolit là gì? Criolit là một khoáng chất tự nhiên có công thức hóa học Na3AlF6, được tìm thấy chủ yếu ở Greenland. Khoáng chất này đóng vai trò quan trọng trong quá trình sản xuất nhôm công nghiệp.
Criolit thường xuất hiện cùng với các khoáng chất khác như công thức quặng apatit là gì trong tự nhiên. Sự kết hợp này tạo nên những mỏ khoáng sản có giá trị kinh tế cao.
Cấu trúc phân tử của criolit
Cấu tạo criolit gồm các ion Na+ và phức chất [AlF6]3-. Trong đó:
- Ion Na+ đóng vai trò cation, phân bố đều trong cấu trúc tinh thể
- Phức chất [AlF6]3- có dạng bát diện với Al3+ ở tâm
- 6 ion F- bao quanh tâm Al3+ theo hình học bát diện
Cấu trúc này tạo nên mạng tinh thể monoclinic đặc trưng của criolit.
Các tính chất vật lý đặc trưng của criolit
Criolit có màu trắng đục hoặc không màu khi tinh khiết. Độ cứng theo thang Mohs từ 2.5-3, thuộc nhóm khoáng vật mềm.
Tỷ trọng của criolit khoảng 2.95-3.0 g/cm3. Khoáng vật này có ánh thủy tinh đặc trưng và độ trong suốt từ trong suốt đến mờ đục.
Điểm nóng chảy và nhiệt độ phân hủy của criolit
Điểm nóng chảy criolit ở 1012°C, thấp hơn nhiều so với nhôm tinh khiết. Đặc tính này giúp criolit trở thành chất điện ly lý tưởng trong quá trình điện phân nhôm.

Khi nhiệt độ tăng cao trên 1100°C, criolit bắt đầu phân hủy thành NaF và AlF3. Quá trình này tạo ra hỗn hợp muối nóng chảy có tính dẫn điện tốt.
Phân loại và nguồn gốc của criolit trong công nghiệp
Criolit là một khoáng chất quan trọng trong công nghiệp luyện nhôm. Khoáng chất này tồn tại dưới hai dạng chính là criolit tự nhiên và criolit nhân tạo. Mỗi loại đều có những đặc điểm và ứng dụng riêng biệt trong sản xuất.
Tương tự như công thức dolomit là gì, criolit cũng là một khoáng chất có công thức hóa học Na3AlF6. Sự khác biệt về nguồn gốc hình thành tạo nên những tính chất đặc trưng cho từng loại.
Criolit tự nhiên và các mỏ khai thác
Criolit tự nhiên được hình thành trong các đá magma giàu kiềm. Quá trình kết tinh magma tạo nên các tinh thể criolit có cấu trúc đặc trưng.
Mỏ criolit tự nhiên lớn nhất thế giới nằm ở Ivigtut, Greenland. Mỏ này đã cung cấp phần lớn criolit cho công nghiệp luyện nhôm từ những năm 1850-1987.
Các mỏ nhỏ hơn được tìm thấy ở Colorado (Mỹ) và Siberia (Nga). Tuy nhiên trữ lượng không đáng kể so với nhu cầu sử dụng trong công nghiệp.
 Phân loại và nguồn gốc của criolit trong công nghiệp
Phân loại và nguồn gốc của criolit trong công nghiệpQuy trình sản xuất criolit nhân tạo
Criolit nhân tạo được sản xuất thông qua phản ứng giữa alumin hydroxit và natri florua. Quy trình này gồm các bước chính:
Bước 1: Pha chế dung dịch NaOH và Al(OH)3 theo tỷ lệ thích hợp
Bước 2: Cho HF vào hỗn hợp và khuấy đều
Bước 3: Kết tinh thu sản phẩm Na3AlF6
Bước 4: Sấy khô và nghiền mịn
Phương pháp này cho phép kiểm soát chất lượng và độ tinh khiết của sản phẩm tốt hơn criolit tự nhiên.
So sánh criolit tự nhiên và nhân tạo
Criolit tự nhiên có ưu điểm là giá thành thấp và không cần qua nhiều công đoạn chế biến. Tuy nhiên, hàm lượng tạp chất cao và nguồn cung không ổn định.
Criolit nhân tạo có độ tinh khiết cao, đáp ứng được các yêu cầu kỹ thuật khắt khe trong công nghiệp luyện nhôm. Chi phí sản xuất cao hơn nhưng chất lượng đồng đều và ổn định.
Hiện nay, hầu hết các nhà máy luyện nhôm đều sử dụng criolit nhân tạo do những ưu điểm vượt trội về chất lượng và tính ổn định của nguồn cung.
Vai trò của criolit trong sản xuất nhôm công nghiệp
Criolit đóng vai trò then chốt trong quá trình sản xuất nhôm công nghiệp. Hợp chất này có công thức hóa học Na3AlF6, được sử dụng làm chất điện ly trong quy trình điện phân nhôm oxit.
Tương tự như quặng photphorit là gì, criolit là một khoáng chất tự nhiên quan trọng trong công nghiệp. Tuy nhiên nguồn criolit tự nhiên rất hiếm nên phải tổng hợp nhân tạo để đáp ứng nhu cầu sản xuất.
 Vai trò của criolit trong sản xuất nhôm công nghiệp
Vai trò của criolit trong sản xuất nhôm công nghiệpCriolit làm chất điện phân trong luyện nhôm
Criolit trong sản xuất nhôm có nhiệm vụ hòa tan Al2O3 ở nhiệt độ thấp hơn điểm nóng chảy của nó. Criolit nóng chảy ở 1012°C trong khi Al2O3 nóng chảy ở 2072°C.
Khi hòa tan trong criolit nóng chảy, Al2O3 sẽ phân ly thành các ion Al3+ và O2-. Các ion này di chuyển về các điện cực tương ứng để tạo thành nhôm kim loại và khí oxy.
Các ưu điểm khi sử dụng criolit trong luyện nhôm
Criolit trong công nghiệp mang lại nhiều lợi ích quan trọng. Chất này có khả năng dẫn điện tốt ở trạng thái nóng chảy và không bị phân hủy trong quá trình điện phân.
Criolit còn giúp tiết kiệm năng lượng đáng kể. Theo nghiên cứu của Viện Luyện kim Moscow, sử dụng criolit giúp giảm 30% điện năng tiêu thụ so với phương pháp truyền thống.
Ngoài ra, criolit có độ bền nhiệt cao và ít bay hơi ở nhiệt độ làm việc. Điều này giúp duy trì ổn định quá trình điện phân trong thời gian dài.
Quy trình sử dụng criolit trong sản xuất nhôm
Ứng dụng criolit trong sản xuất nhôm cần tuân thủ quy trình chặt chẽ. Đầu tiên, criolit được nấu chảy trong bể điện phân ở 960-980°C.
Tiếp theo, Al2O3 được hòa tan vào criolit nóng chảy với tỷ lệ 2-8%. Dung dịch điện phân này được duy trì ở nhiệt độ và nồng độ ổn định trong suốt quá trình.
Quá trình điện phân diễn ra liên tục với anot than chì và catot than chì phủ thép. Nhôm kim loại được thu ở đáy bể, còn khí oxy thoát ra ở anot.
FAQ: Câu hỏi thường gặp về criolit
Criolit là hợp chất quan trọng trong công nghiệp luyện nhôm. Tôi nhận được rất nhiều câu hỏi từ học sinh về chất này trong suốt 20 năm giảng dạy. Sau đây là một số thắc mắc phổ biến nhất.
Criolit có độc không?
Criolit có độc tính trung bình với cơ thể con người. Khi tiếp xúc trực tiếp, criolit có thể gây kích ứng da và niêm mạc.
Theo nghiên cứu của Viện An toàn và Sức khỏe Nghề nghiệp Mỹ (NIOSH), phơi nhiễm lâu dài với criolit có thể gây tổn thương phổi và xương.
Tuy nhiên trong điều kiện bình thường, công thức criolit Na3AlF6 rất ổn định và ít phản ứng. Chỉ cần tuân thủ quy tắc an toàn khi làm việc.
Criolit có thể thay thế bằng chất nào?
Hiện nay các nhà khoa học đang nghiên cứu nhiều chất thay thế criolit tự nhiên. Một số muối flo tổng hợp đã được thử nghiệm.
Tuy nhiên chưa có chất nào hoàn toàn thay thế được vai trò của criolit trong luyện nhôm. Criolit tổng hợp là lựa chọn phổ biến nhất.
Tại sao criolit quan trọng trong luyện nhôm?
Criolit có nhiệt độ nóng chảy thấp (khoảng 1000°C) và dẫn điện tốt. Nó hòa tan được oxit nhôm Al2O3.
Khi điện phân, criolit nóng chảy tạo môi trường lý tưởng để khử Al3+ thành Al kim loại. Không có criolit, nhiệt độ điện phân sẽ cao hơn nhiều.
Criolit còn bảo vệ nhôm nóng chảy khỏi bị oxi hóa. Đây là lý do criolit không thể thiếu trong sản xuất nhôm công nghiệp.
Chất điện phân công thức criolit đóng vai trò then chốt trong ngành luyện nhôm công nghiệp. Với cấu trúc phân tử Na3AlF6 độc đáo, criolit tự nhiên và nhân tạo đều có điểm nóng chảy thấp, tính dẫn điện tốt. Đặc biệt, criolit là dung môi không thể thiếu trong quá trình điện phân nhôm oxit để sản xuất nhôm kim loại tinh khiết. Các tính chất ưu việt này khiến criolit trở thành vật liệu không thể thay thế trong công nghiệp luyện nhôm hiện đại.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

