Công thức chung của ankin và các tính chất hóa học quan trọng cần nhớ
Công thức chung của ankin CnH2n-2 là nền tảng để hiểu về hydrocarbon không no. Ankin chứa liên kết ba C≡C độc đáo trong cấu trúc phân tử. Các phản ứng cộng đặc trưng tạo nên tính chất hóa học quan trọng của ankin. Chúng có nhiều ứng dụng thiết thực trong công nghiệp và đời sống.
Công thức chung của ankin
Ankin là một trong những dãy đồng đẳng quan trọng của hydrocarbon không no. Công thức chung của ankin có dạng CnH2n-2 (với n ≥ 2).
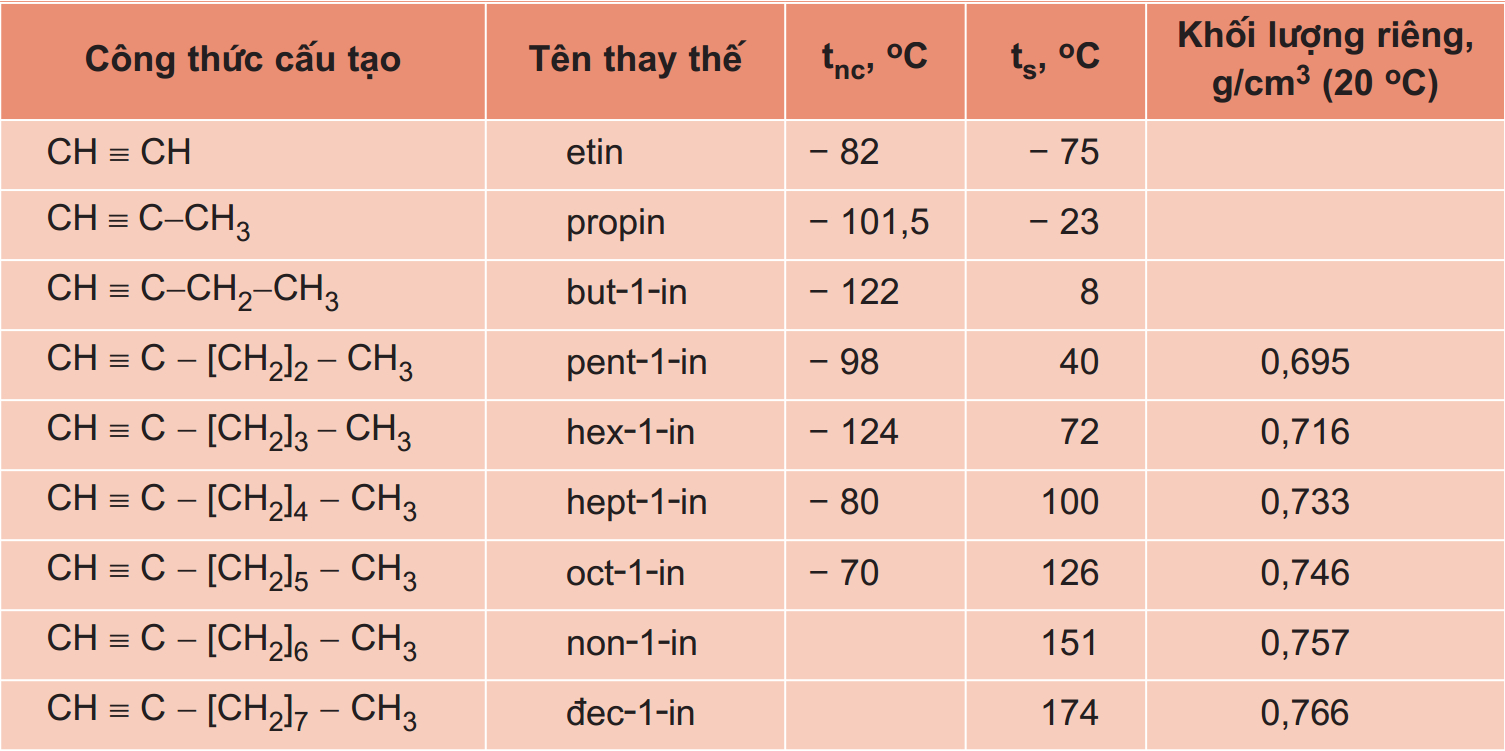
Trong đó:
– C: nguyên tử cacbon
– H: nguyên tử hydro
– n: số nguyên dương, biểu thị số nguyên tử cacbon trong phân tử
– 2n-2: số nguyên tử hydro trong phân tử
Khi được hỏi “công thức ankin là gì“, tôi thường giải thích với học sinh rằng đây là nhóm hydrocarbon chứa một liên kết ba C≡C. Điều này giúp phân biệt ankin với các dãy đồng đẳng khác.
Để dễ nhớ công thức, tôi thường gợi ý học sinh quan sát quy luật: số H luôn ít hơn 2 nguyên tử so với anken (CnH2n). Ví dụ với n=2, ta có C2H2 là axetilen – ankin đơn giản nhất.
Một cách khác để ghi nhớ là ankin có số H ít nhất trong 3 dãy hydrocarbon thẳng mạch (ankan, anken, ankin). Điều này phản ánh đặc điểm cấu tạo có liên kết ba của chúng.
Cấu tạo và đặc điểm phân tử ankin trong hóa học
Ankin là một loại hydrocarbon không no, có chứa một liên kết ba giữa hai nguyên tử carbon. Đây là một trong những hợp chất quan trọng trong hóa học hữu cơ.
Cấu trúc phân tử ankin có công thức chung là CnH2n-2 (n ≥ 2). Tương tự như công thức chung của anken, ankin cũng là một dãy đồng đẳng với sự khác biệt về số nguyên tử carbon.
Cấu tạo phân tử ankin
Ankin là gì? Đó là hydrocarbon mà trong phân tử có chứa một liên kết ba C≡C. Mỗi nguyên tử carbon tham gia liên kết ba đều có cấu hình lai hóa sp.
Trong phân tử ankin, hai nguyên tử carbon liên kết ba nằm trên một đường thẳng với góc liên kết 180°. Điều này tạo nên hình dạng thẳng đặc trưng của phân tử.
Các electron π trong liên kết ba tạo thành hai mặt phẳng vuông góc với nhau. Đặc điểm này giúp ankin có khả năng phản ứng cộng cao hơn so với anken.
Liên kết ba trong phân tử ankin
Liên kết ba trong ankin bao gồm một liên kết σ và hai liên kết π. Liên kết σ được hình thành từ sự xen phủ trục của hai orbital sp.
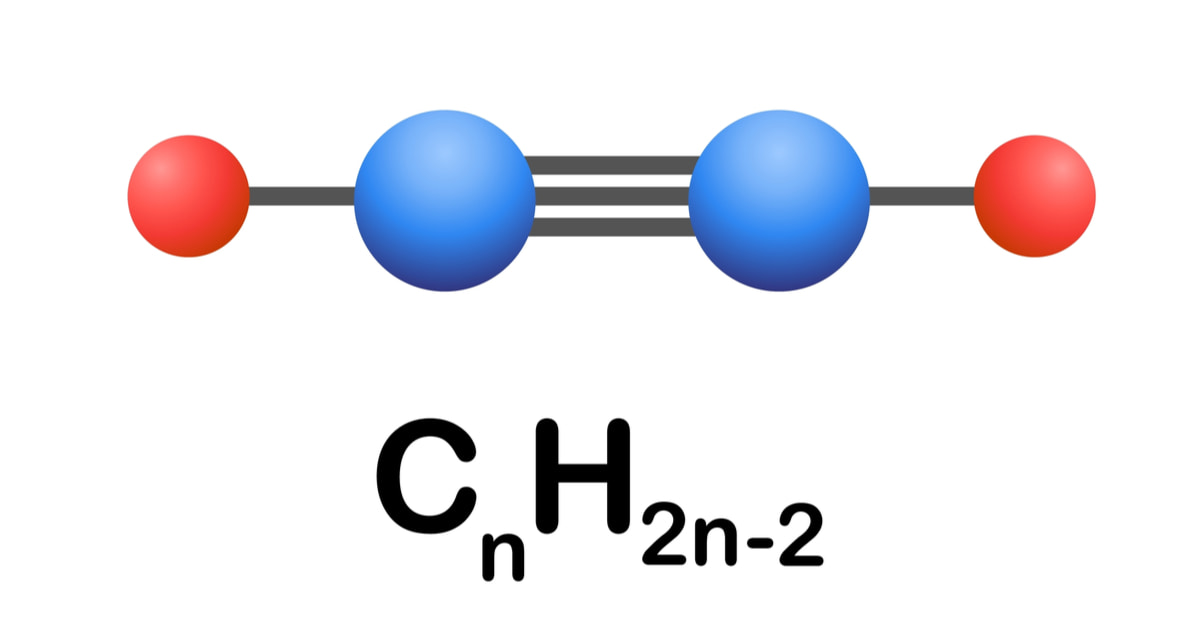
Hai liên kết π được tạo thành từ sự xen phủ bên của hai cặp orbital p còn lại. Năng lượng liên kết ba cao hơn nhiều so với liên kết đơn và đôi.
Trong quá trình giảng dạy, tôi thường ví von liên kết ba như ba sợi dây thừng bện vào nhau, giúp học sinh dễ hình dung về độ bền của nó.
Cách viết công thức cấu tạo ankin
Cách viết công thức ankin tuân theo nguyên tắc thể hiện rõ vị trí liên kết ba và các nhóm thế. Đầu tiên, cần xác định mạch carbon chính chứa liên kết ba.
Số thứ tự carbon được đánh từ đầu gần liên kết ba nhất. Tên gọi ankin được xác định dựa vào số carbon trong mạch chính và vị trí liên kết ba.
Các nhóm thế được ghi theo thứ tự alphabet và chỉ rõ vị trí carbon mang nhóm thế. Ví dụ: CH3-C≡C-CH3 là but-2-in.
Danh pháp và quy tắc gọi tên ankin theo IUPAC
Cách gọi tên ankin tuân theo quy tắc danh pháp IUPAC với những nguyên tắc rõ ràng và chặt chẽ. Tôi sẽ hướng dẫn chi tiết từng bước để các em dễ dàng nắm bắt và áp dụng.
Nguyên tắc đánh số mạch cacbon
Việc đánh số mạch cacbon trong ankin rất quan trọng và quyết định tên gọi của hợp chất. Mạch cacbon chính phải chứa liên kết ba và có độ dài lớn nhất.
Đánh số từ đầu mạch gần nhánh thế hoặc liên kết ba nhất. Nếu có nhiều nhánh thế, ưu tiên đánh số sao cho tổng chỉ số các nhánh thế nhỏ nhất.
Trong trường hợp có cả nhánh thế và liên kết ba, ưu tiên đánh số để liên kết ba có chỉ số nhỏ nhất.
Quy tắc gọi tên ankin
Tên ankin được tạo thành từ tên gốc hydrocarbon tương ứng và thay đuôi -an bằng -in. Vị trí liên kết ba được chỉ rõ bằng số thứ tự cacbon đầu tiên của liên kết.
Các nhánh thế được gọi tên theo thứ tự alphabet và đặt trước tên gốc chính. Số chỉ vị trí nhánh thế được đặt trước tên nhánh thế.
Khi có nhiều nhánh thế giống nhau, dùng tiền tố di-, tri-, tetra-… để chỉ số lượng nhánh.
Ví dụ minh họa cách gọi tên
Tôi sẽ lấy ví dụ điển hình mà tôi thường dùng để giảng dạy:
CH≡C-C
prop-1-in
CH3-C≡C-C
but-2-in
Với hợp chất phức tạp hơn:
CH3-CH(CH3)-C≡C-C
4-metylpent-2-in
Qua 20 năm giảng dạy, tôi nhận thấy học sinh dễ nhớ nhất khi phân tích từng thành phần của tên gọi:
– Gốc chính: số cacbon trong mạch chính
– Vị trí liên kết ba: số thứ tự cacbon đầu tiên của liên kết
– Nhánh thế: tên và vị trí các nhóm thế
Tính chất hóa học đặc trưng của ankin
Tính chất của ankin thể hiện qua các phản ứng cộng đặc trưng nhờ liên kết ba C≡C. Các phản ứng này diễn ra theo cơ chế cộng electrophin.
Khi giảng dạy, tôi thường ví von liên kết ba như một sợi dây thừng chắc chắn. Khi bị tác động, nó sẽ đứt từng sợi một cách có trật tự.
Phản ứng cộng hidro
Ankin cộng H2 xảy ra qua 2 giai đoạn, tạo thành anken rồi ankan. Phản ứng cần xúc tác Ni, Pt hoặc Pd.
Công thức tổng quát:
R-C≡C-R’ + H2 → R-CH=CH-R’ (anken)
R-CH=CH-R’ + H2 → R-CH2-CH2-R’ (ankan)
Phản ứng cộng halogen
Ankin cộng halogen (Cl2, Br2) theo tỉ lệ mol 1:2 tạo thành dẫn xuất dihalogen.
Công thức phản ứng:
R-C≡C-R’ + 2X2 → R-CX2-CX2-R’ (X là halogen)
Đây là phản ứng tôi hay dùng để kiểm tra nhanh sự có mặt của ankin thông qua màu nâu đỏ của dung dịch brom.
Phản ứng cộng HX
Ankin phản ứng với HX (HCl, HBr, HI) theo quy tắc Markovnikov. Phản ứng xảy ra qua 2 giai đoạn.
Công thức phản ứng:
R-C≡C-R’ + HX → R-CX=CH-R’
R-CX=CH-R’ + HX → R-CX2-CH2-R’
Khi dạy về công thức tổng quát của ancol, tôi thường liên hệ với phản ứng này để học sinh hiểu sâu hơn.
Phản ứng trùng hợp
Các ankin có thể trùng hợp tạo thành polime trong điều kiện xúc tác thích hợp. Acetylen là ví dụ điển hình.
Phản ứng trùng hợp acetylen:
nHC≡CH → (-CH=CH-)n
Sản phẩm trùng hợp có nhiều ứng dụng quan trọng trong công nghiệp nhựa và vật liệu.
Ứng dụng và vai trò của ankin trong đời sống
Ứng dụng của ankin ngày càng đa dạng và quan trọng trong nhiều lĩnh vực. Các hợp chất ankin đóng vai trò then chốt trong sản xuất công nghiệp và đời sống hàng ngày của con người.
Ứng dụng trong công nghiệp
Axetilen (C2H2) là ankin được sử dụng phổ biến nhất trong công nghiệp. Tôi thường lấy ví dụ về đèn hàn axetilen để minh họa cho học sinh về ứng dụng này.
Nhiệt độ ngọn lửa axetilen có thể đạt tới 3000°C, giúp cắt và hàn kim loại hiệu quả. Đây là công cụ không thể thiếu trong ngành cơ khí.
Trong công nghiệp hóa chất, axetilen là nguyên liệu quan trọng để sản xuất nhiều hợp chất hữu cơ. Từ axetilen, các nhà máy tổng hợp được axit axetic, vinyl axetat và nhiều sản phẩm khác.
Ứng dụng trong đời sống
Các sản phẩm từ ankin xuất hiện trong cuộc sống hàng ngày nhiều hơn bạn nghĩ. Tôi thường giúp học sinh nhận ra điều này qua các ví dụ cụ thể.
Vinyl axetat được dùng sản xuất sơn, keo dán và các vật liệu xây dựng. Khi bạn sơn tường nhà hay dán giấy dán tường, rất có thể đang sử dụng sản phẩm từ ankin.
Axit axetic – thành phần chính của giấm ăn cũng được tổng hợp từ axetilen. Đây là minh chứng cho mối liên hệ mật thiết giữa hóa học và đời sống thường ngày.
Bài tập và phương pháp giải về ankin
Trong quá trình giảng dạy bài tập về ankin, tôi nhận thấy học sinh thường gặp khó khăn ở 3 dạng chính: viết công thức, gọi tên và tính chất hóa học. Mỗi dạng bài tập đều có những đặc thù riêng cần nắm vững.
Với môn ankin trong hóa học 11, việc nắm chắc các dạng bài tập sẽ giúp học sinh tự tin hơn khi làm bài kiểm tra và thi cử. Tôi sẽ hướng dẫn chi tiết từng dạng bài tập phổ biến.
Bài tập về viết công thức
Khi viết công thức ankin, học sinh cần nhớ công thức tổng quát CnH2n-2. Đây là nền tảng quan trọng để giải các bài tập liên quan.

Ví dụ: Viết công thức cấu tạo của but-2-in
CH3-C≡C-CH3
Một mẹo nhỏ tôi thường chia sẻ với học sinh là đếm số carbon trước, sau đó xác định vị trí liên kết ba. Cuối cùng điền đủ số hydro theo quy tắc hóa trị.
Bài tập về gọi tên
Quy tắc gọi tên ankin tuân theo 3 bước cơ bản:
– Xác định mạch carbon chính chứa liên kết ba
– Đánh số thứ tự sao cho liên kết ba có chỉ số nhỏ nhất
– Gọi tên theo quy tắc: số chỉ vị trí + tên gốc + “in”
Tôi thường cho học sinh thực hành nhiều với các công thức đơn giản trước khi chuyển sang các công thức phức tạp hơn. Điều này giúp các em hình thành phản xạ đúng.
Bài tập về tính chất hóa học
Ankin có 2 loại phản ứng đặc trưng cần nắm vững:
– Phản ứng cộng H2, X2, HX
– Phản ứng thế H trong nhóm ≡CH đầu mạch
Kinh nghiệm của tôi là học sinh nên vẽ sơ đồ phản ứng tổng quát trước khi giải bài tập cụ thể. Việc này giúp hình dung rõ sự thay đổi liên kết trong phân tử.
Với phản ứng cộng, cần chú ý tỉ lệ mol giữa các chất tham gia phản ứng và điều kiện phản ứng. Đây thường là điểm mấu chốt để giải đúng bài toán.
FAQ: Câu hỏi thường gặp về ankin
Ankin là một trong những chất hữu cơ quan trọng với công thức chung của ankin là CnH2n-2. Các câu hỏi dưới đây sẽ giúp bạn hiểu rõ hơn về đặc điểm của ankin.
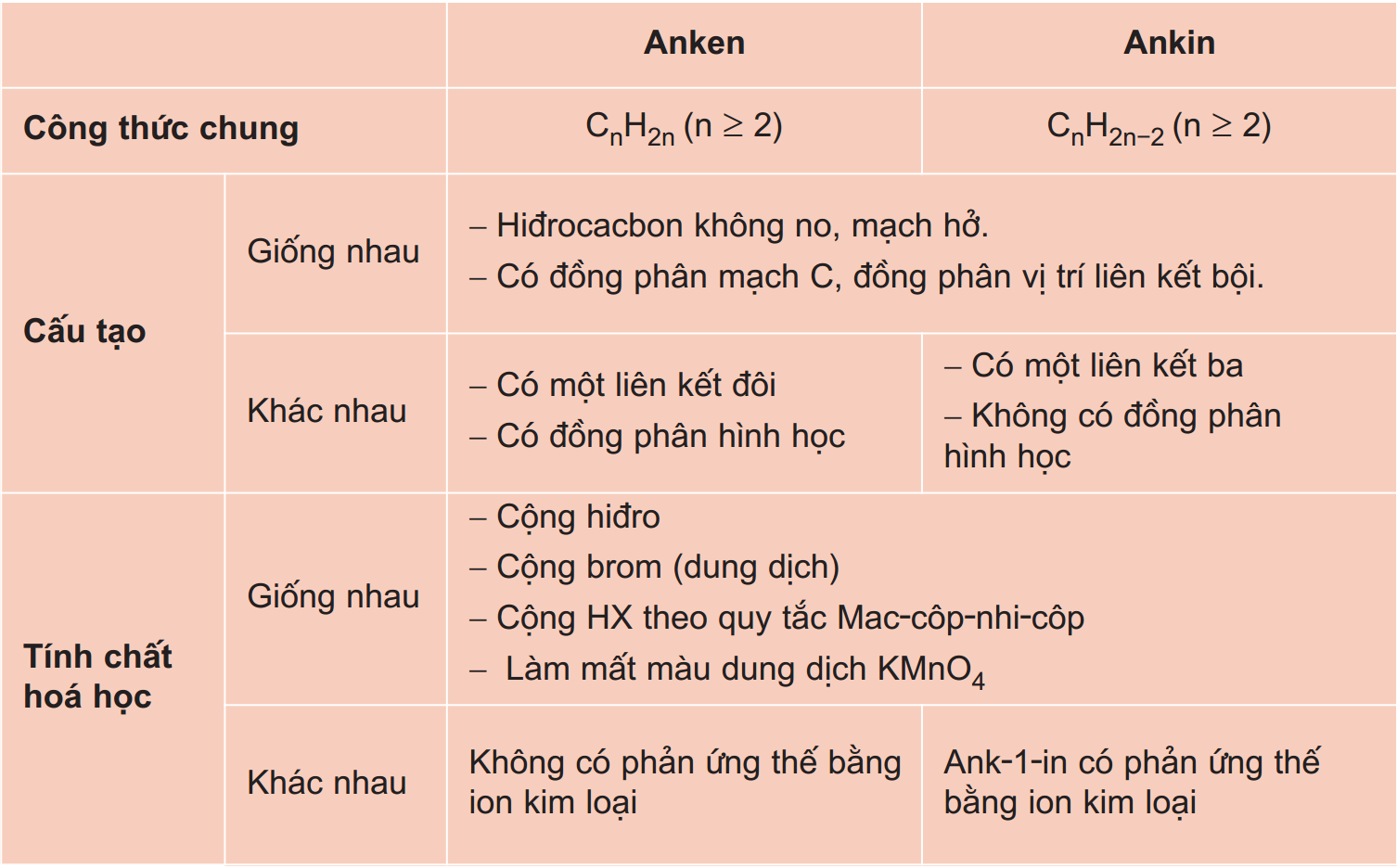
Sự khác biệt giữa ankin và anken?
Ankin và anken khác nhau ở cấu tạo phân tử và độ bão hòa. Ankin có liên kết ba giữa 2 nguyên tử carbon, còn anken chỉ có liên kết đôi.
Ankin có công thức CnH2n-2, trong khi anken có công thức CnH2n. Điều này cho thấy ankin thiếu hydro hơn so với anken.
Về độ hoạt động hóa học, ankin hoạt động mạnh hơn anken do liên kết ba dễ bị phá vỡ hơn liên kết đôi.
Tại sao ankin có liên kết ba?
Liên kết ba trong ankin hình thành do sự xen phủ của các obitan p. Mỗi nguyên tử carbon đều lai hóa sp.
Một liên kết σ được tạo bởi sự xen phủ trục của hai obitan sp. Hai liên kết π được tạo bởi sự xen phủ bên của hai cặp obitan p.
Cấu trúc này làm cho phân tử ankin có dạng thẳng với góc liên kết 180°.
Điều kiện nào để xảy ra phản ứng cộng của ankin?
Phản ứng cộng của ankin xảy ra khi có mặt xúc tác thích hợp. Với H2 cần xúc tác Pd/PbCO3 hoặc Ni.
Nhiệt độ phản ứng thường từ 150-200°C. Áp suất cần đủ cao để đẩy nhanh tốc độ phản ứng.
Phản ứng cộng của ankin thường xảy ra theo cơ chế cộng nucleophil, với sự tấn công của tác nhân nucleophil vào liên kết ba.
Kiến thức về công thức chung của ankin là nền tảng quan trọng trong chương trình hóa học 11. Ankin có cấu tạo đặc trưng với liên kết ba và các tính chất hóa học đa dạng như phản ứng cộng, trùng hợp. Việc nắm vững cấu tạo phân tử, quy tắc gọi tên và các phản ứng hóa học của ankin giúp học sinh vận dụng tốt trong giải bài tập và ứng dụng thực tiễn.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

