Công thức cấu tạo N2O5 và các tính chất hóa học quan trọng cần nắm
Công thức cấu tạo N2O5 thể hiện cấu trúc phân tử độc đáo của đinitơ pentaoxit. Phân tử này có cấu trúc không gian đặc biệt với các liên kết N-O. N2O5 là một chất oxi hóa mạnh và có nhiều ứng dụng quan trọng trong công nghiệp hóa chất.
Công thức cấu tạo N2O5
Đinitơ pentaoxit N2O5 là một hợp chất vô cơ quan trọng trong hóa học. Công thức cấu tạo N2O5 có dạng:
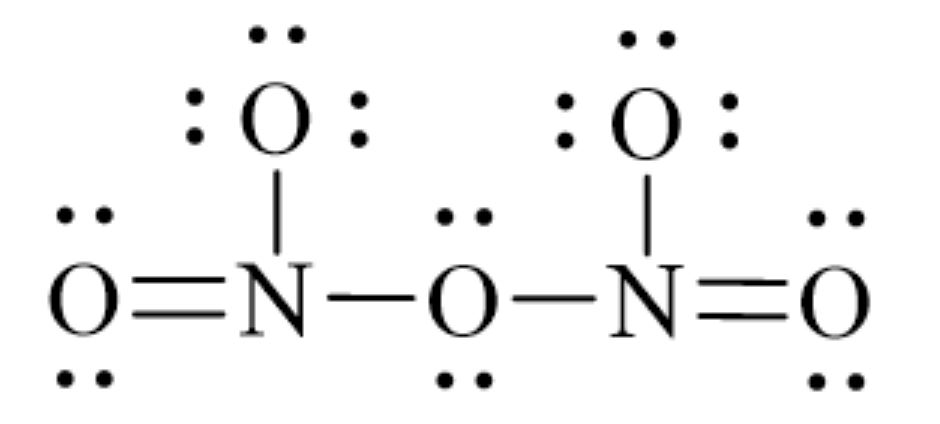
O2N-O-NO2
Trong đó:
- Hai nguyên tử nitơ (N) liên kết với 5 nguyên tử oxi (O)
- Cầu nối O ở giữa kết nối hai nhóm NO2
Cấu trúc phân tử N2O5 có dạng phẳng, với góc liên kết O-N-O xấp xỉ 120°. Các liên kết N-O trong nhóm NO2 có độ dài khoảng 1.2Å.
Qua 20 năm giảng dạy, tôi thường gợi ý học sinh ghi nhớ cấu trúc này bằng cách hình dung như chiếc cầu nối. Hai nhóm NO2 như hai bờ sông và nguyên tử O ở giữa là cây cầu bắc ngang.
Khi vẽ công thức cấu tạo, các em cần chú ý:
- Vẽ hai nhóm NO2 riêng biệt
- Nối chúng bằng một nguyên tử O ở giữa
- Kiểm tra tổng số nguyên tử N và O phải là 2 và 5
Hiểu rõ cấu trúc này giúp các em dễ dàng giải thích các tính chất hóa học của N2O5 như khả năng phân hủy hay tính oxi hóa mạnh.
Cấu trúc phân tử và liên kết trong N2O5
Phân tử N2O5 có cấu trúc phức tạp với 2 nguyên tử nitơ và 5 nguyên tử oxi. Trong quá trình giảng dạy, tôi thường ví von nó như một “tòa lâu đài” với các liên kết đan xen.
Công thức cấu tạo của n2o5 có dạng O2N-O-NO2, trong đó hai nhóm NO2 được nối với nhau qua cầu nối O. Cấu trúc này tương tự như công thức cấu tạo của h2o2 nhưng phức tạp hơn.
Cấu tạo không gian của phân tử N2O5
Trong không gian 3 chiều, phân tử N2O5 có dạng hình học phẳng. Hai nhóm NO2 nằm ở hai bên cầu nối O theo dạng đối xứng.
Các nguyên tử oxi trong nhóm NO2 sắp xếp theo hình chữ V, với nguyên tử N ở đỉnh. Điều này tạo nên sự cân bằng về mặt điện tích trong phân tử.
Các liên kết hóa học trong N2O5
Trong N2O5 tồn tại hai loại liên kết chính: liên kết đơn N-O và liên kết đôi N=O. Liên kết đơn N-O có năng lượng thấp hơn và dễ bị phân hủy hơn.
Mỗi nguyên tử N trong nhóm NO2 tạo một liên kết đôi với một nguyên tử O và hai liên kết đơn với hai nguyên tử O còn lại. Đây là lý do khiến N2O5 không bền trong điều kiện thường.
Góc liên kết và độ dài liên kết
Góc liên kết O-N-O trong nhóm NO2 xấp xỉ 130°. Góc này lớn hơn góc 120° lý thuyết do sự đẩy electron của các cặp electron tự do.
Độ dài liên kết N=O (1,20Å) ngắn hơn đáng kể so với liên kết đơn N-O (1,40Å). Sự chênh lệch này ảnh hưởng trực tiếp đến tính chất hóa học của phân tử.
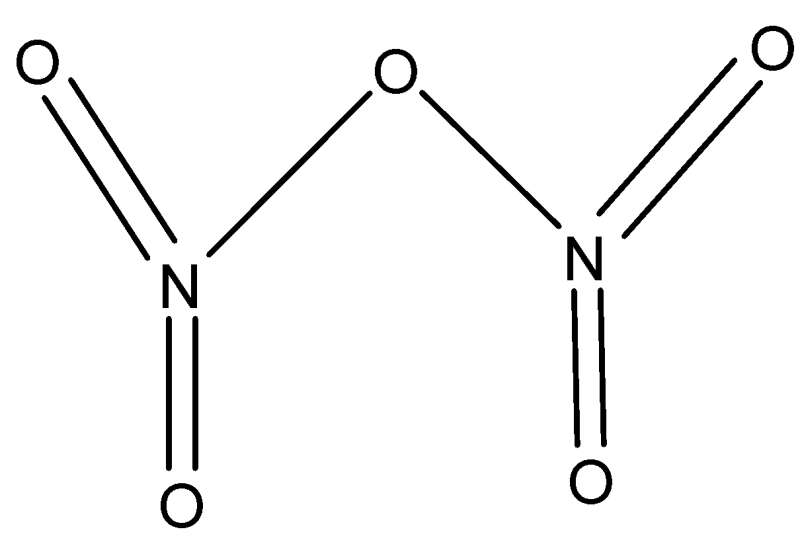
Khi giảng dạy, tôi thường nhấn mạnh rằng các thông số này rất quan trọng để hiểu được tính chất và phản ứng của N2O5.
Tính chất hóa học của N2O5 dựa trên cấu tạo
Đinitơ pentaoxit (N2O5) có công thức cấu tạo N2O5 dạng phân tử đối xứng. Cấu trúc này quyết định các tính chất hóa học đặc trưng của hợp chất.
Tương tự như công thức cấu tạo p2o5, N2O5 có cấu trúc phân tử phức tạp với liên kết N-O và O-O. Điều này tạo nên tính chất hóa học đa dạng.
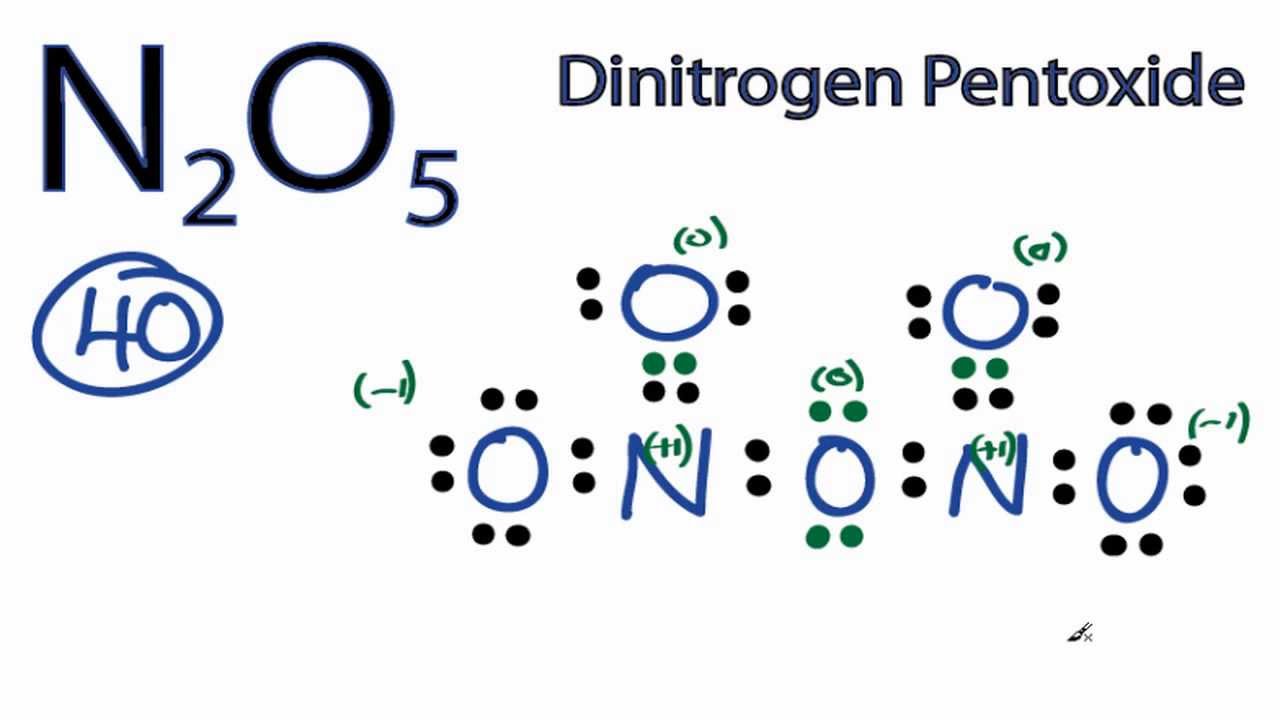
Phản ứng thủy phân
N2O5 phản ứng mạnh với nước tạo thành axit nitric theo phương trình:
N2O5 + H2O → 2HNO3
Phản ứng xảy ra nhanh và tỏa nhiệt mạnh. Đây là phương pháp điều chế axit nitric trong phòng thí nghiệm.
Khi tiếp xúc với hơi ẩm không khí, N2O5 cũng bị thủy phân từ từ tạo khói trắng HNO3.
Tính oxi hóa mạnh
N2O5 là chất oxi hóa rất mạnh do có số oxi hóa của nitơ cao (+5). Nó oxi hóa được nhiều kim loại và phi kim.
Với kim loại, phản ứng xảy ra mãnh liệt tạo muối nitrat:
2N2O5 + 4Cu → 4Cu(NO3)2 + 2NO2
Với phi kim như cacbon, lưu huỳnh, phản ứng tạo oxit và NO2.
Khả năng phân hủy
N2O5 không bền, dễ phân hủy thành NO2 và O2 theo phương trình:
2N2O5 → 4NO2 + O2
Phản ứng phân hủy xảy ra nhanh khi đun nóng trên 50°C. Ở nhiệt độ thường, N2O5 cũng tự phân hủy chậm.
Ánh sáng và xúc tác kim loại làm tăng tốc độ phân hủy đáng kể.
So sánh cấu tạo N2O5 với các oxit nitơ khác
Công thức cấu tạo N2O5 có cấu trúc phân tử đặc biệt với 2 nguyên tử N liên kết với 5 nguyên tử O. Đây là oxit cao nhất của nitơ và có tính oxit axit mạnh nhất trong dãy.
Cấu trúc phân tử của N2O5 gồm 2 nhóm NO2 được nối với nhau qua 1 nguyên tử O trung tâm:
O2N-O-NO2
Khi tác dụng với nước, N2O5 tạo thành axit HNO3 theo phương trình:
N2O5 + H2O → 2HNO3
So sánh với NO và NO2
NO có cấu tạo đơn giản với 1 liên kết đôi N=O. Phân tử có tính trung tính và không tạo thành axit khi tác dụng với nước.
NO2 có cấu tạo góc với góc liên kết O-N-O là 134°. Phân tử có màu nâu đỏ đặc trưng và tạo thành hỗn hợp axit công thức cấu tạo của HNO2 và HNO3 khi tác dụng với nước.
So sánh với N2O3 và N2O4
N2O3 có cấu tạo gồm NO và NO2 liên kết với nhau. Phân tử có màu xanh đen và tạo thành HNO2 khi tác dụng với nước.
N2O4 là dimer của NO2, có cấu tạo đối xứng qua liên kết N-N. Phân tử không màu ở nhiệt độ thấp và phân hủy thành NO2 khi nhiệt độ tăng.
Như vậy, N2O5 có cấu tạo phức tạp hơn các oxit nitơ khác và thể hiện tính axit mạnh nhất trong dãy.
Ứng dụng của N2O5 trong thực tế
Đinitơ pentaoxit (N2O5) là một hợp chất quan trọng trong ngành công nghiệp hóa chất. Hợp chất này có vai trò then chốt trong nhiều quy trình sản xuất và ứng dụng thực tiễn.
Trong phòng thí nghiệm, N2O5 thường được sử dụng làm chất oxi hóa mạnh. Tôi thường hướng dẫn sinh viên thực hiện các phản ứng nitrat hóa với N2O5 để tổng hợp các hợp chất hữu cơ như công thức cấu tạo của c 2 h 5 oh h.
Sản xuất axit nitric
N2O5 là nguyên liệu quan trọng trong sản xuất axit nitric công nghiệp. Khi phản ứng với nước, N2O5 cho axit nitric tinh khiết với hiệu suất cao.
Quá trình này đặc biệt hiệu quả vì không tạo ra sản phẩm phụ độc hại như n2h4 công thức cấu tạo. Theo kinh nghiệm giảng dạy của tôi, đây là phương pháp an toàn nhất để sản xuất HNO3 trong phòng thí nghiệm.
Các ứng dụng trong công nghiệp
N2O5 đóng vai trò quan trọng trong công nghiệp sản xuất thuốc nổ và chất propellant. Hợp chất này tham gia vào quá trình nitrat hóa các hợp chất hữu cơ.
Trong ngành điện tử, N2O5 được sử dụng để tạo lớp oxit mỏng trên bề mặt silicon. Lớp oxit này có tính cách điện cao, giúp bảo vệ các linh kiện bán dẫn.
Ngoài ra, N2O5 còn được ứng dụng trong sản xuất phân bón, thuốc nhuộm và một số ngành công nghiệp hóa chất khác. Tuy nhiên cần tuân thủ nghiêm ngặt các quy trình an toàn khi sử dụng.
FAQ: Câu hỏi thường gặp về N2O5
Các câu hỏi thường gặp về N2O5 giúp làm rõ thêm tính chất và đặc điểm của hợp chất này. Tôi sẽ giải đáp những thắc mắc phổ biến nhất.
N2O5 có phải là một anhydric không?
N2O5 là một anhydric của axit nitric HNO3. Khi tác dụng với nước, nó tạo thành axit nitric theo phương trình:
N2O5 + H2O → 2HNO3
Đây là một phản ứng điển hình của anhydric axit với nước. Trong quá trình giảng dạy, tôi thường ví von N2O5 như “cha đẻ” của axit nitric.
Tại sao N2O5 dễ phân hủy?
N2O5 dễ phân hủy do liên kết N-O trong phân tử không bền. Nguyên nhân chính là do:
Nitơ có số oxi hóa +5 không ổn định
Nhiệt độ cao làm đứt liên kết N-O
Ánh sáng cũng có thể kích thích phân hủy
Phản ứng phân hủy xảy ra theo phương trình:
2N2O5 → 4NO2 + O2
N2O5 có độc không?
N2O5 là chất rất độc với cơ thể. Khi tiếp xúc có thể gây:
Kích ứng đường hô hấp nghiêm trọng
Bỏng da và niêm mạc
Tổn thương phổi nặng nếu hít phải
Cần thao tác trong tủ hút và trang bị đầy đủ bảo hộ khi làm việc với chất này. Tôi luôn nhắc học sinh phải tuân thủ nghiêm ngặt quy tắc an toàn phòng thí nghiệm.
Nghiên cứu về công thức cấu tạo N2O5 giúp làm rõ cấu trúc phân tử đặc biệt của hợp chất này. N2O5 có cấu tạo không gian phức tạp với các liên kết N-O và góc liên kết đặc trưng. Đặc điểm cấu tạo này quyết định tính chất hóa học như khả năng thủy phân, tính oxi hóa mạnh và xu hướng phân hủy của N2O5. Hiểu rõ cấu tạo và tính chất của N2O5 là nền tảng để ứng dụng hiệu quả trong sản xuất axit nitric và các ngành công nghiệp khác.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

