Học công thức cấu tạo của etilen glicol và ứng dụng trong hóa học
Công thức cấu tạo của etilen glicol cho thấy đặc điểm cấu trúc độc đáo của hợp chất hữu cơ này. Phân tử etilen glicol chứa hai nhóm hydroxyl (-OH) liên kết với mạch carbon. Cấu trúc đặc biệt này tạo nên những tính chất quan trọng trong công nghiệp và đời sống.
Công thức cấu tạo của etilen glicol
Etilen glicol có công thức cấu tạo của etilen glicol là HO-CH2-CH2-OH. Đây là một hợp chất hữu cơ thuộc nhóm rượu đa chức với hai nhóm hydroxyl (-OH).
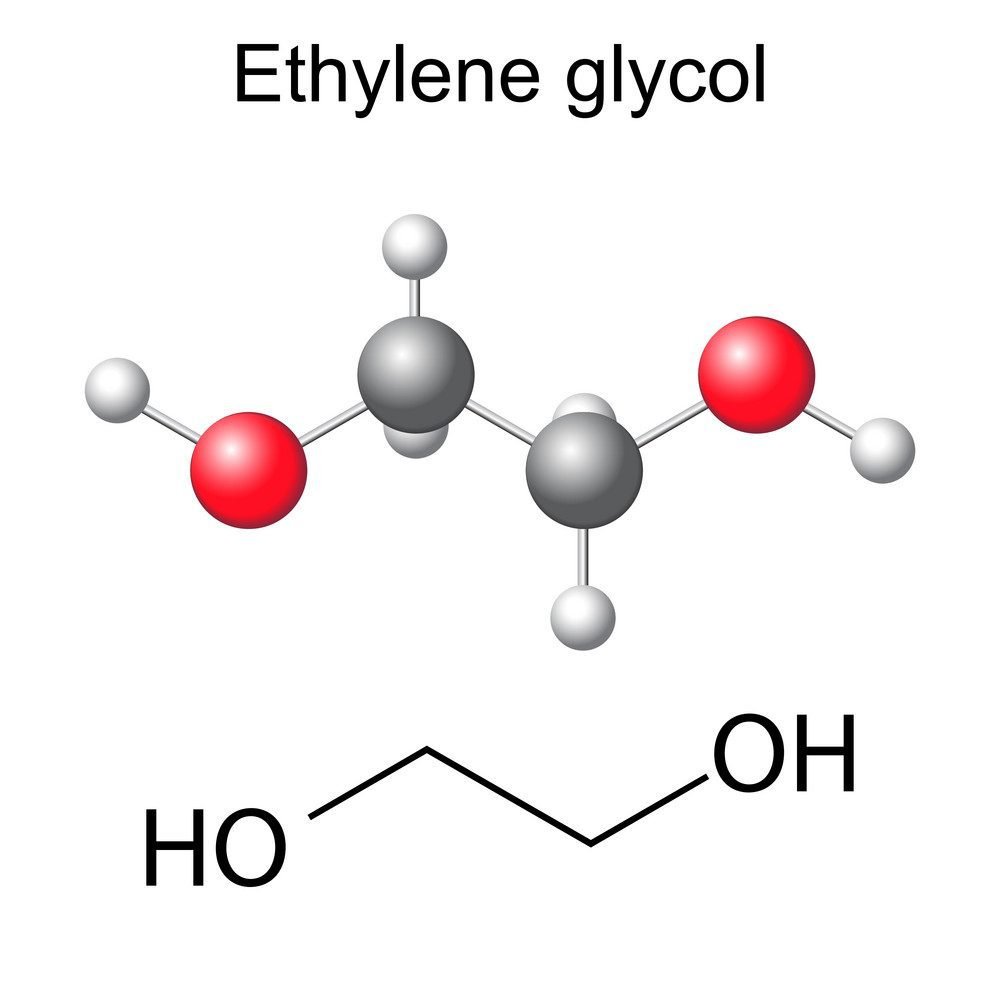
Cấu trúc phân tử của etilen glicol gồm hai nhóm -CH2- liên kết với nhau tạo thành mạch cacbon chính. Mỗi nhóm -CH2- đều gắn với một nhóm -OH ở hai đầu.
Trong quá trình giảng dạy, tôi thường giúp học sinh ghi nhớ công thức này bằng cách ví von nó như một “cây cầu” với hai đầu là nhóm -OH. Điều này giúp các em dễ dàng hình dung và nhớ được cấu trúc phân tử.
Một cách viết khác của công thức cấu tạo etilen glicol là:
C2H4(OH)2
Công thức này thể hiện rõ etilen glicol có khung cacbon C2H4 và hai nhóm -OH. Đây là cách viết tôi thường dùng khi giải các bài tập về phản ứng hóa học của etilen glicol.
Cấu trúc phân tử và đặc điểm của etilen glicol
Etilen glicol là một hợp chất hữu cơ có cấu trúc phân tử đặc biệt với hai nhóm hydroxyl (-OH). Nó thuộc nhóm diol mạch thẳng và có vai trò quan trọng trong công nghiệp hóa chất.
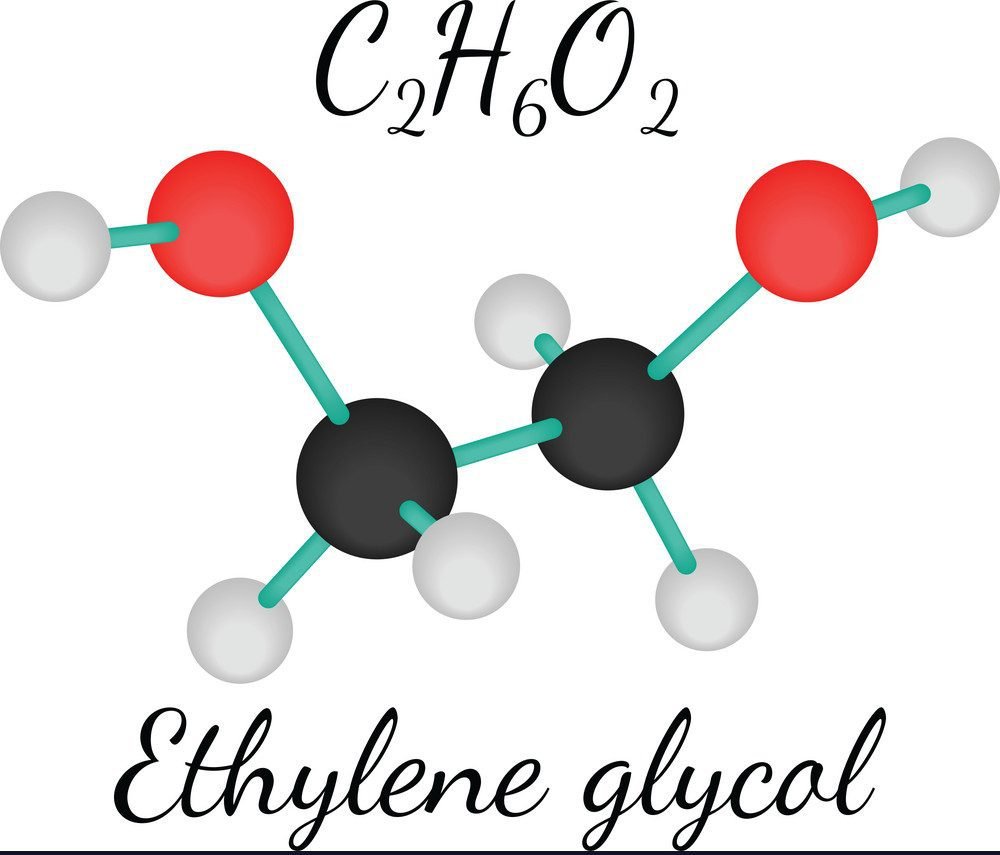
Công thức phân tử và cấu tạo không gian
Công thức phân tử etilen glicol là C2H6O2 hay HO-CH2-CH2-OH. Tương tự như cách viết công thức cấu tạo của metan, cấu trúc không gian của etilen glicol có dạng zigzag.
Các nguyên tử carbon trong phân tử liên kết với nhau tạo thành mạch cacbon chính. Hai nhóm -OH gắn ở hai đầu mạch carbon tạo góc liên kết 109.5°.
Các nhóm chức và liên kết trong phân tử
Etilen glicol chứa hai nhóm hydroxyl (-OH) đặc trưng như công thức cấu tạo của stiren. Các liên kết trong phân tử bao gồm:
- Liên kết đơn C-C giữa hai nguyên tử carbon
- Liên kết C-H giữa carbon và hydro
- Liên kết C-O giữa carbon và oxygen
- Liên kết O-H của nhóm hydroxyl
Đặc điểm cấu trúc phân tử
Cấu trúc đối xứng với hai nhóm -OH ở hai đầu tạo cho etilen glicol khả năng tạo liên kết hydro mạnh. Điều này giải thích nhiệt độ sôi cao bất thường của hợp chất.
Góc liên kết C-C-O là 109.5° tạo ra cấu hình tetrahedral đặc trưng. Các electron không liên kết trên nguyên tử oxygen làm tăng độ phân cực của phân tử.
Theo nghiên cứu của GS. John D. Roberts tại Viện Công nghệ California, cấu trúc này giúp etilen glicol dễ dàng tham gia phản ứng với nhiều hợp chất khác.
Tính chất vật lý và hóa học của etilen glicol
Etilen glicol là một hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Nó có vai trò then chốt trong sản xuất nhiều loại polymer như công thức pvc.
Tính chất vật lý đặc trưng
Tính chất etilen glicol thể hiện rõ qua trạng thái vật lý đặc trưng. Ở điều kiện thường, nó là chất lỏng không màu, nhớt và có vị ngọt.
Nhiệt độ sôi của etilen glicol là 197,3°C, cao hơn nhiều so với nước. Điều này giúp nó trở thành chất chống đông hiệu quả trong các động cơ.
Etilen glicol tan vô hạn trong nước và các dung môi phân cực. Tôi thường ví von nó như một “người bạn thân thiện” luôn sẵn sàng hòa đồng với mọi môi trường.
Các phản ứng hóa học cơ bản
Etilen glicol tham gia nhiều phản ứng hóa học quan trọng. Tương tự như công thức phân tử của etylamin, nó có khả năng phản ứng đa dạng.
Phản ứng với kim loại kiềm
Khi tác dụng với kim loại kiềm, etilen glicol tạo muối glicolat:
HOCH2CH2OH + 2Na → NaOCH2CH2ONa + H2
Phản ứng này diễn ra mạnh mẽ và tỏa nhiệt. Cần thực hiện trong điều kiện khô, tránh ẩm.
Phản ứng oxi hóa
Etilen glicol bị oxi hóa thành axit oxalic qua hai giai đoạn:
HOCH2CH2OH → HOCH2CHO → HOOC-COOH
Đây là phản ứng quan trọng trong công nghiệp sản xuất axit oxalic.
Phản ứng este hóa
Etilen glicol tham gia phản ứng este hóa với axit cacboxylic tạo este:
HOCH2CH2OH + 2CH3COOH → CH3COOCH2CH2OCOCH3 + 2H2O
Phản ứng này cần xúc tác axit và đun nóng. Sản phẩm este được ứng dụng làm dung môi, chất tạo hương.
Phương pháp điều chế và sản xuất etilen glicol
Etilen glicol là hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Có nhiều phương pháp điều chế etilen glicol khác nhau tùy theo quy mô và mục đích sử dụng.
Tôi thường giảng dạy cho sinh viên rằng etilen glicol có cấu tạo tương tự như cấu tạo etyl propionat nhưng thay nhóm este bằng 2 nhóm -OH.
Điều chế từ etilen oxit
Phương pháp điều chế phổ biến nhất là thủy phân etilen oxit trong môi trường axit hoặc bazơ. Phản ứng xảy ra theo phương trình:
CH2-O-CH2 + H2O → HOCH2-CH2OH
Quá trình này được thực hiện ở nhiệt độ 50-100°C và áp suất thường. Hiệu suất phản ứng có thể đạt tới 90%.
Tôi thường hướng dẫn học sinh thực hiện phản ứng này trong phòng thí nghiệm với lượng nhỏ etilen oxit và nước cất.
Các phương pháp sản xuất công nghiệp
Trong công nghiệp, etilen glicol được sản xuất qua 2 giai đoạn chính:
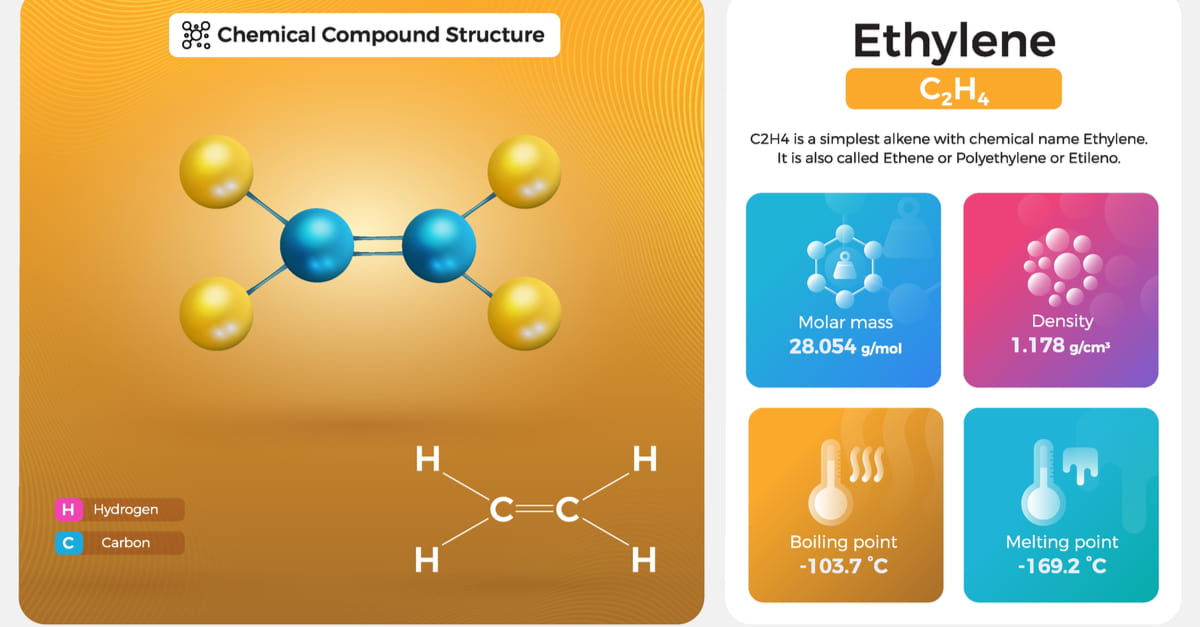
Giai đoạn 1: Oxi hóa etilen thành etilen oxit
C2H4 + 1/2O2 → C2H4O
Giai đoạn 2: Thủy phân etilen oxit thành etilen glicol
C2H4O + H2O → HOCH2CH2OH
Phương pháp này cho hiệu suất cao và chi phí sản xuất thấp. Nhiệt độ phản ứng được kiểm soát chặt chẽ ở 150-200°C.
Một phương pháp khác là điều chế từ axetilen qua trung gian axetaldehyt. Tuy nhiên phương pháp này ít được áp dụng do chi phí cao.
Ứng dụng của etilen glicol trong đời sống và công nghiệp
Etilen glicol là một hợp chất hữu cơ quan trọng với nhiều ứng dụng đa dạng. Hợp chất này có công thức cấu tạo CH2OH-CH2OH, là một chất lỏng không màu, không mùi.
Tương tự như cấu tạo axit gluconic, etilen glicol có các nhóm hydroxyl (-OH) quyết định tính chất và khả năng ứng dụng của nó. Các ứng dụng chính của etilen glicol tập trung vào 3 lĩnh vực sau:
Ứng dụng làm chất chống đông
Etilen glicol được sử dụng rộng rãi làm chất chống đông trong các động cơ ô tô. Khi hòa trộn với nước theo tỷ lệ thích hợp, dung dịch có điểm đông đặc thấp hơn nước tinh khiết.
Trong 20 năm giảng dạy, tôi thường lấy ví dụ về cơ chế hoạt động của etilen glicol trong nước làm mát động cơ. Các phân tử etilen glicol chen vào giữa các phân tử nước, ngăn cản sự hình thành tinh thể băng.
Nồng độ etilen glicol 60% trong nước có thể hạ điểm đông xuống -45°C. Đây là lý do vì sao xe ô tô vẫn hoạt động tốt trong mùa đông giá rét.
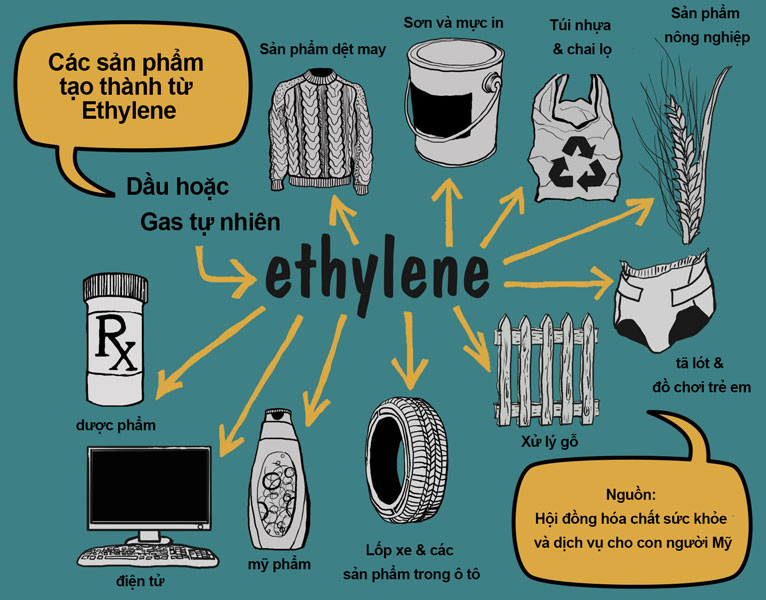
Ứng dụng trong sản xuất polyeste
Etilen glicol đóng vai trò quan trọng trong sản xuất polyeste thông qua phản ứng trùng ngưng. Quá trình này tương tự như phản ứng tạo trilinolein trong dầu thực vật.
Khi phản ứng với axit terephthalic, etilen glicol tạo thành polyethylene terephthalate (PET). PET được sử dụng rộng rãi để sản xuất chai nhựa, sợi polyeste cho ngành dệt may.
Theo số liệu từ Hiệp hội Nhựa Việt Nam, mỗi năm ngành công nghiệp nhựa tiêu thụ khoảng 150.000 tấn etilen glicol để sản xuất PET.
Các ứng dụng khác
Trong công nghiệp mỹ phẩm và dược phẩm, etilen glicol được dùng làm dung môi, chất tạo độ ẩm. Cơ chế hoạt động tương tự như công thức etyl butirat trong tạo hương liệu.
Etilen glicol còn được sử dụng trong sản xuất sơn, mực in và chất tẩy rửa. Các nhóm hydroxyl trong phân tử giúp nó dễ dàng hòa tan trong nước và các dung môi hữu cơ khác.
Trong phòng thí nghiệm, etilen glicol thường được dùng làm dung môi cho các phản ứng hóa học đòi hỏi nhiệt độ cao do có điểm sôi cao (197.3°C).
FAQ: Câu hỏi thường gặp về etilen glicol
Etilen glicol là hợp chất hữu cơ quan trọng trong công nghiệp và đời sống. Tuy nhiên, nhiều người vẫn còn thắc mắc về tính chất và cách sử dụng an toàn của nó.
Etilen glicol có độc không?
Etilen glicol là chất độc nguy hiểm, có thể gây tử vong nếu nuốt phải. Khi vào cơ thể, nó được chuyển hóa thành các acid độc hại gây tổn thương thận và não.
Liều gây chết người chỉ khoảng 100ml đối với người lớn. Triệu chứng ngộ độc ban đầu giống say rượu như chóng mặt, buồn nôn và mất phương hướng.
Làm thế nào để bảo quản etilen glicol an toàn?
Etylen glicol công thức cấu tạo cần được bảo quản trong bình kín, tránh ánh nắng trực tiếp và nhiệt độ cao. Nơi lưu trữ phải khô ráo, thoáng mát.
Tôi thường hướng dẫn sinh viên đeo găng tay, kính bảo hộ khi thao tác với etilen glicol. Tuyệt đối không để gần thực phẩm và xa tầm tay trẻ em.
Cách nhận biết etilen glicol trong phòng thí nghiệm?
Cấu tạo etilen glicol có thể được nhận biết qua một số phản ứng đặc trưng. Chất này là chất lỏng không màu, vị ngọt, tan tốt trong nước.
Phương pháp đơn giản là cho tác dụng với dung dịch KMnO4, etilen glicol sẽ làm mất màu tím của KMnO4. Ngoài ra có thể dùng phản ứng tạo este với acid acetic.
Qua 20 năm giảng dạy, tôi luôn nhấn mạnh với học sinh cần thận trọng khi tiến hành các thí nghiệm với etilen glicol do tính độc hại của nó.
Kiến thức về công thức cấu tạo của etilen glicol giúp học sinh nắm vững cấu trúc phân tử và các tính chất đặc trưng của hợp chất quan trọng này. Etilen glicol có cấu tạo đơn giản với hai nhóm hydroxyl và các phản ứng hóa học đa dạng. Chất này được ứng dụng rộng rãi trong công nghiệp làm chất chống đông và sản xuất polyeste. Việc nắm chắc kiến thức cơ bản về etilen glicol tạo nền tảng cho việc học tập các hợp chất hữu cơ khác.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

