Nắm rõ ancol butylic công thức và tính chất hóa học cơ bản
Ancol butylic công thức là một chất hữu cơ quan trọng trong ngành công nghiệp hóa chất. Hợp chất này có 4 đồng phân cấu tạo với nhiều tính chất đặc trưng. Các phản ứng hóa học của ancol butylic tạo nên nhiều sản phẩm giá trị trong đời sống.
Ancol butylic công thức và cấu tạo phân tử
Ancol butylic là hợp chất hữu cơ thuộc nhóm ancol có 4 nguyên tử cacbon trong phân tử. Ancol butylic là một chất lỏng không màu với mùi đặc trưng.
Công thức phân tử của ancol butylic là C4H9OH. Tùy vào vị trí nhóm -OH, ancol butylic có 4 đồng phân cấu tạo:
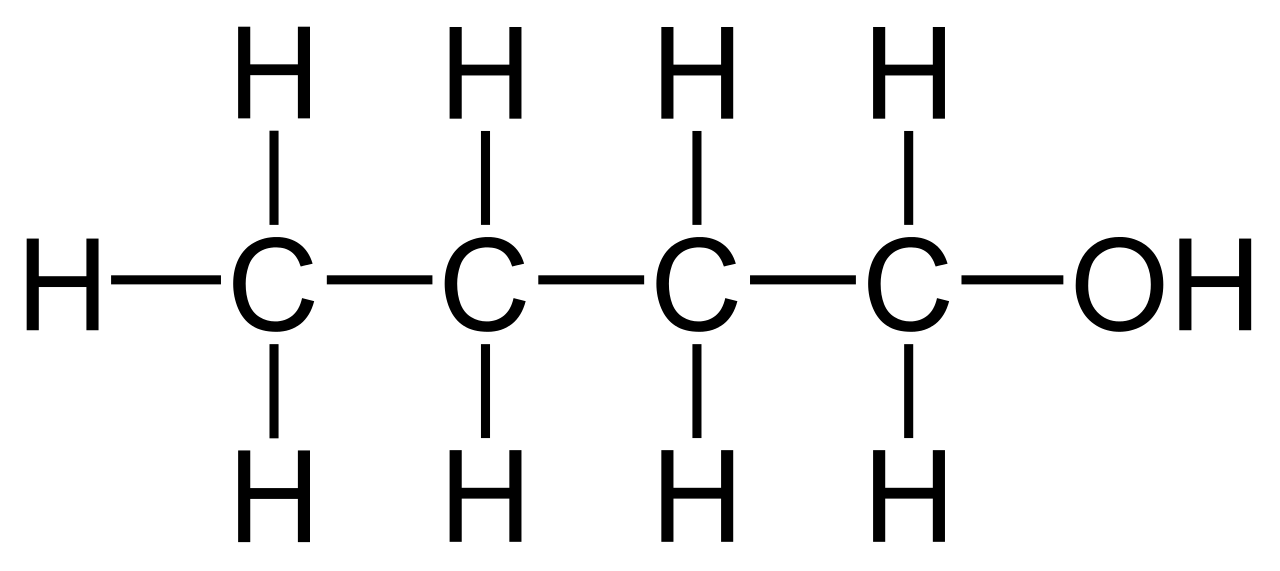
Butan-1-ol (n-butanol): CH3-CH2-CH2-CH2OH
- Là ancol bậc một, mạch thẳng
- Nhiệt độ sôi: 117,7°C
- Ứng dụng làm dung môi trong công nghiệp
Butan-2-ol (sec-butanol): CH3-CH2-CHOH-CH3
- Là ancol bậc hai, mạch thẳng
- Nhiệt độ sôi: 99,5°C
- Dùng sản xuất chất tẩy rửa
2-metylpropan-1-ol (iso-butanol): (CH3)2CH-CH2OH
- Là ancol bậc một, mạch nhánh
- Nhiệt độ sôi: 108°C
- Sử dụng trong tổng hợp hữu cơ
2-metylpropan-2-ol (tert-butanol): (CH3)3C-OH
- Là ancol bậc ba, mạch nhánh
- Nhiệt độ sôi: 82,4°C
- Ứng dụng làm chất chống đông
Trong quá trình giảng dạy, tôi thường gợi ý học sinh nhớ công thức ancol butylic thông qua cấu trúc “4C + 1OH”. Điều này giúp các em dễ dàng phân biệt với ancol anlylic công thức.
Mỗi đồng phân của ancol butylic có tính chất hóa học đặc trưng khác nhau. Điều này phụ thuộc vào bậc của ancol và cấu trúc mạch cacbon.
Các dạng đồng phân của ancol butylic trong hóa học hữu cơ
Ancol butylic có công thức phân tử C4H9OH và tồn tại nhiều dạng đồng phân khác nhau. Mỗi dạng đồng phân ancol butylic đều có những tính chất hóa học đặc trưng riêng.
Tương tự như ancol benzylic công thức cấu tạo, các dạng đồng phân của ancol butylic có sự khác biệt về cấu trúc phân tử. Điều này ảnh hưởng trực tiếp đến tính chất vật lý và hóa học của chúng.
Đồng phân cấu tạo của ancol butylic
Đồng phân cấu tạo của ancol butylic có thể phân thành 2 loại chính dựa vào cấu trúc mạch cacbon. Loại thứ nhất là mạch thẳng với công thức CH3-CH2-CH2-CH2OH.
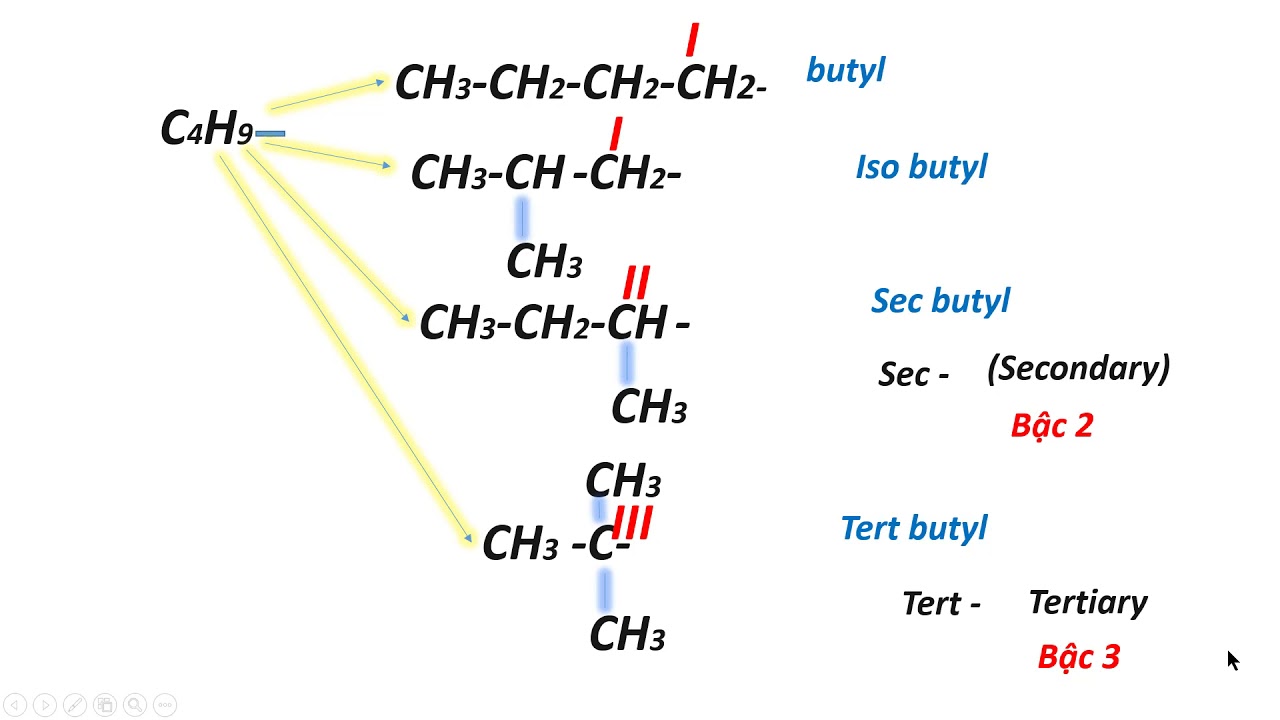
Loại thứ hai là mạch nhánh với cấu tạo ancol butylic dạng (CH3)2CH-CH2OH. Sự khác biệt về cấu trúc mạch cacbon tạo nên những tính chất đặc trưng cho mỗi đồng phân.
Trong quá trình giảng dạy, tôi thường ví von mạch cacbon như một chuỗi xích. Mạch thẳng giống như sợi xích thẳng, còn mạch nhánh như sợi xích có mắc thêm các móc phụ.
Đồng phân vị trí nhóm -OH
Nhóm -OH trong ancol butylic có thể gắn vào các vị trí cacbon khác nhau. Khi nhóm -OH gắn vào cacbon số 1, ta có butan-1-ol (CH3-CH2-CH2-CH2OH).
Nếu nhóm -OH gắn vào cacbon số 2, ta có butan-2-ol (CH3-CH2-CHOH-CH3). Vị trí gắn nhóm -OH quyết định tính chất của ancol.
Kinh nghiệm của tôi cho thấy học sinh dễ nhớ hơn khi liên tưởng vị trí nhóm -OH như vị trí ghế ngồi trong rạp chiếu phim. Mỗi vị trí sẽ cho góc nhìn và trải nghiệm khác nhau.
Đồng phân không gian của ancol butylic
Đồng phân không gian của ancol butylic xuất hiện khi phân tử có cacbon bất đối xứng. Butan-2-ol là một ví dụ điển hình với cacbon số 2 bất đối xứng.
Hai đồng phân không gian của butan-2-ol là đồng phân R và S. Chúng là hình ảnh gương của nhau nhưng không thể chồng khít.
Để giúp học sinh hiểu rõ hơn, tôi thường so sánh với đôi găng tay trái phải. Chúng giống nhau về hình dạng nhưng không thể đeo chéo cho nhau được.
Tính chất vật lý và hóa học của ancol butylic
Ancol butylic là một hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Tương tự như Ancol propylic công thức, ancol butylic có nhiều ứng dụng đa dạng.
Các tính chất vật lý đặc trưng
Tính chất ancol butylic thể hiện rõ qua trạng thái vật lý đặc trưng. Ở điều kiện thường, ancol butylic là chất lỏng không màu, có mùi đặc trưng.
Nhiệt độ sôi của ancol butylic khoảng 117°C, cao hơn so với các ancol mạch ngắn hơn. Điều này giúp tôi dễ dàng phân biệt ancol butylic với các đồng đẳng khác trong phòng thí nghiệm.
Ancol butylic tan tốt trong nước nhờ liên kết hydro giữa nhóm -OH với phân tử H2O. Tuy nhiên độ tan giảm dần khi nhiệt độ tăng.
Phản ứng hóa học của ancol butylic
Phản ứng ancol butylic diễn ra đa dạng do có nhóm -OH hoạt động. Các phản ứng chính gồm thế, oxi hóa và este hóa.
Phản ứng thế
Ancol butylic tham gia phản ứng thế với kim loại kiềm tạo muối ancoholat:
CH3-CH2-CH2-CH2OH + Na → CH3-CH2-CH2-CH2ONa + 1/2H2
Phản ứng với HX (X=Cl, Br, I) tạo halogenua ancol tương ứng:
CH3-CH2-CH2-CH2OH + HCl → CH3-CH2-CH2-CH2Cl + H2O
Phản ứng oxi hóa
Khi oxi hóa ancol butylic bằng CuO hoặc KMnO4, thu được andehyt butyric:
CH3-CH2-CH2-CH2OH + [O] → CH3-CH2-CH2-CHO + H2O
Oxi hóa mạnh hơn bằng K2Cr2O7/H2SO4 tạo axit butyric:
CH3-CH2-CH2-CH2OH + 2[O] → CH3-CH2-CH2-COOH + H2O
Phản ứng este hóa
Ancol butylic phản ứng với axit cacboxylic tạo este:
CH3-CH2-CH2-CH2OH + CH3COOH ⇌ CH3-CH2-CH2-CH2OCOCH3 + H2O
Phản ứng este hóa là phản ứng thuận nghịch, cần xúc tác axit và đun nóng để tăng hiệu suất.
Phương pháp điều chế và ứng dụng của ancol butylic
Ancol butylic là hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Chất này có thể được điều chế bằng nhiều phương pháp khác nhau và có nhiều ứng dụng thiết thực.
Các phương pháp điều chế trong phòng thí nghiệm
Phương pháp phổ biến nhất để điều chế ancol butylic là thủy phân este butyl acetat. Phản ứng được thực hiện trong môi trường kiềm như công thức axit oxalic.
Một phương pháp khác là khử andehit butyric bằng LiAlH4 hoặc NaBH4. Phản ứng diễn ra nhanh chóng ở nhiệt độ phòng và cho hiệu suất cao.
Ngoài ra, ancol butylic còn được điều chế từ phản ứng Grignard giữa CH3MgBr với propanal. Phương pháp này đòi hỏi điều kiện phản ứng khắt khe nhưng cho sản phẩm tinh khiết.
Quy trình sản xuất công nghiệp
Ancol butylic trong công nghiệp được sản xuất chủ yếu qua phản ứng oxo hóa propen. Đây là phương pháp hiệu quả và kinh tế nhất hiện nay.
Quá trình sản xuất trải qua 3 giai đoạn chính: Tổng hợp propen từ cracking dầu mỏ, oxo hóa propen thành butanal và cuối cùng là khử butanal thành ancol butylic.
Theo số liệu từ Hiệp hội Hóa chất Mỹ, sản lượng ancol butylic toàn cầu đạt khoảng 2,5 triệu tấn/năm, chủ yếu phục vụ ngành công nghiệp nhựa và sơn.
Ứng dụng trong công nghiệp và đời sống
Ứng dụng ancol butylic rất đa dạng trong nhiều lĩnh vực. Chất này là dung môi quan trọng trong sản xuất sơn, vecni và mực in.
Trong công nghiệp nhựa, ancol butylic được dùng làm chất hóa dẻo cho PVC và các loại nhựa tổng hợp khác. Nó giúp cải thiện độ đàn hồi và độ bền của sản phẩm.
Ancol butylic còn là nguyên liệu để sản xuất các este butyl, được sử dụng làm hương liệu trong mỹ phẩm và thực phẩm. Tôi thường giới thiệu với sinh viên về vai trò của nó trong ngành công nghiệp hương liệu.
Bài tập và phương pháp giải về ancol butylic
Ancol butylic là hợp chất hữu cơ có 4 nguyên tử cacbon và nhóm -OH. Tôi sẽ hướng dẫn các em giải các dạng bài tập thường gặp về ancol butylic một cách chi tiết.
Bài tập về cấu tạo và đồng phân
Ancol butylic có 4 đồng phân cấu tạo chính. Mỗi đồng phân có tính chất riêng biệt và cách gọi tên khác nhau.
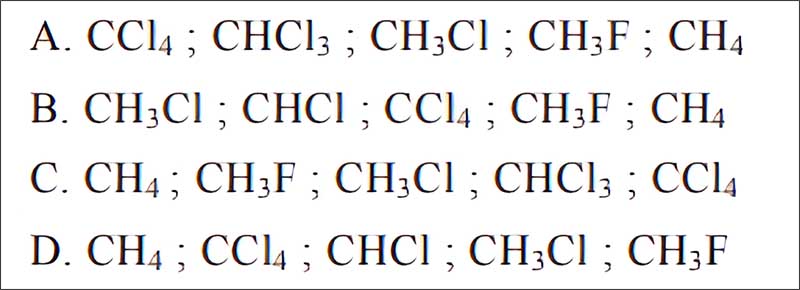
Để xác định đồng phân, ta vẽ mạch cacbon chính rồi gắn nhóm -OH vào các vị trí khác nhau. Tương tự như Ether ethylic là gì, cách gọi tên cũng dựa vào vị trí nhóm thế.
Ví dụ với butan-1-ol: CH3-CH2-CH2-CH2OH, nhóm -OH ở vị trí số 1 của mạch cacbon chính.
Bài tập về tính chất và điều chế
Ancol butylic tham gia các phản ứng đặc trưng của ancol như phản ứng tách nước và oxi hóa.
Phương trình phản ứng tách nước:
CH3-CH2-CH2-CH2OH → CH3-CH2-CH=CH2 + H2O
Phản ứng oxi hóa:
CH3-CH2-CH2-CH2OH + [O] → CH3-CH2-CH2-CHO
Khi giải bài tập, cần chú ý điều kiện phản ứng và chất xúc tác.
Bài tập tổng hợp
Bài tập tổng hợp thường yêu cầu viết chuỗi phản ứng điều chế ancol butylic từ các chất đầu.
Ví dụ điều chế từ butan:
CH3-CH2-CH2-CH3 → CH3-CH2-CH2-CH2Cl → CH3-CH2-CH2-CH2OH
Cần nắm vững các phương pháp điều chế và điều kiện phản ứng để giải được dạng bài này.
Một số phương pháp điều chế chính:
- Thủy phân halogenua ancyl
- Khử andehyt/xeton
- Hidrat hóa anken
FAQ: Câu hỏi thường gặp về ancol butylic
Ancol butylic là một nhóm hợp chất hữu cơ quan trọng trong công nghiệp hóa chất. Tôi sẽ giải đáp các thắc mắc phổ biến về nhóm chất này.
Sự khác biệt giữa các đồng phân ancol butylic
Ancol butylic có 4 đồng phân cấu tạo chính với công thức phân tử C4H9OH. Butan-1-ol có chuỗi carbon thẳng với nhóm OH ở vị trí đầu.
Butan-2-ol có nhóm OH ở carbon số 2. 2-metylpropan-1-ol có nhánh metyl và nhóm OH ở đầu. 2-metylpropan-2-ol có cấu trúc phân nhánh với nhóm OH ở carbon bậc 3.
Điểm sôi của các đồng phân giảm dần theo thứ tự: butan-1-ol > butan-2-ol > 2-metylpropan-1-ol > 2-metylpropan-2-ol do khả năng tạo liên kết hydro khác nhau.
Độc tính và cách bảo quản ancol butylic
Các ancol butylic có độc tính thấp hơn metanol nhưng vẫn cần thận trọng khi sử dụng. Tránh hít phải hơi và tiếp xúc trực tiếp với da.
Bảo quản trong bình kín, tránh ánh sáng mặt trời và nguồn nhiệt. Không để gần các chất oxy hóa mạnh.
Khi xảy ra sự cố, rửa ngay bằng nước sạch và đến cơ sở y tế. Trang bị đầy đủ bảo hộ lao động khi thao tác.
Phân biệt ancol butylic với các ancol khác
Ancol butylic có mùi đặc trưng và ít tan trong nước hơn các ancol mạch ngắn hơn. Điểm sôi cao hơn metanol, etanol.
Phản ứng với Na cho khí H2 và muối alkoxyt. Tốc độ phản ứng chậm hơn các ancol bậc một khác.
Có thể phân biệt bằng phản ứng oxi hóa: ancol bậc một cho andehyt, bậc hai cho xeton, bậc ba không bị oxi hóa.
Kiến thức về ancol butylic công thức là nền tảng quan trọng trong hóa học hữu cơ. Chất này có 4 đồng phân cấu tạo với những tính chất đặc trưng và ứng dụng rộng rãi trong công nghiệp. Các phản ứng hóa học đa dạng của ancol butylic như thế, oxi hóa và este hóa tạo nên nhiều sản phẩm có giá trị. Việc nắm vững cấu tạo phân tử và phương pháp điều chế giúp học sinh dễ dàng vận dụng giải các dạng bài tập về hợp chất này.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

