Thuộc lòng công thức muối khan và ứng dụng trong hóa học cơ bản
Muối khan công thức hóa học đóng vai trò quan trọng trong phòng thí nghiệm và đời sống. Chúng là hợp chất vô cơ có cấu tạo đặc biệt từ kim loại và gốc axit. Bài viết phân tích chi tiết về công thức, tính chất và ứng dụng của muối khan trong thực tiễn.
Muối khan công thức hóa học là gì?
Muối khan công thức hóa học là dạng muối không chứa nước kết tinh trong phân tử. Đây là loại muối được tạo thành từ phản ứng trung hòa giữa axit và bazơ.
Công thức tổng quát của muối khan là:
MaAb
Trong đó:
- M: Kim loại hoặc gốc NH4+
- A: Gốc axit
- a, b: Hệ số cân bằng điện tích
Ví dụ một số muối khan phổ biến:
- NaCl (Natri clorua): Muối ăn thông thường
- CaCO3 (Canxi cacbonat): Đá vôi
- K2SO4 (Kali sunfat): Phân bón
Khi giảng dạy về muối khan là gì, tôi thường lấy ví dụ về muối ăn NaCl. Đây là loại muối khan đơn giản và gần gũi với học sinh nhất.
Để phân biệt muối khan với muối ngậm nước, ta có thể quan sát hình dạng tinh thể. Muối khan thường có tinh thể đồng nhất và không bị chảy nước khi để ngoài không khí.

Một số muối khan khi hòa tan vào nước sẽ tạo thành dung dịch trong suốt. Điều này giúp học sinh dễ dàng nhận biết muối khan trong các thí nghiệm hóa học cơ bản.
Phân loại và tính chất cơ bản của muối khan trong hóa học
Muối khan là hợp chất vô cơ được tạo thành từ phản ứng trung hòa giữa axit và bazơ. Chúng có vai trò quan trọng trong đời sống và công nghiệp.
Các muối khan thường gặp như NaCl, CuSO4, Na2CO3 đều có cấu trúc tinh thể ion với liên kết ion mạnh mẽ. Điều này giúp chúng bền vững ở nhiệt độ thường.
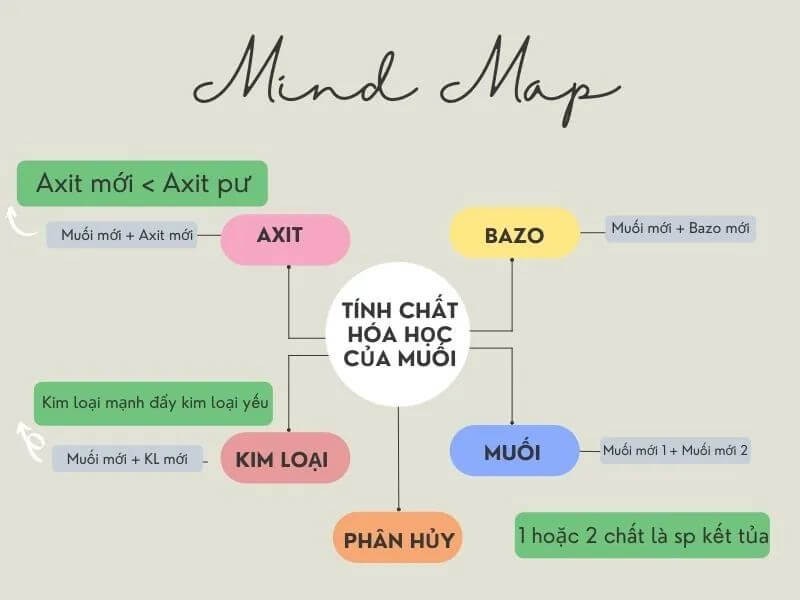
Các loại muối khan thường gặp
Muối halogen như NaCl, KCl có màu trắng và thường được sử dụng trong đời sống hàng ngày. Trong 20 năm giảng dạy, tôi thường lấy ví dụ về muối ăn để học sinh dễ hình dung.
Muối sunfat như CuSO4 khan có màu trắng xám đặc trưng. Khi thêm nước vào sẽ chuyển thành màu xanh do tạo phức với nước.
Muối nitrat như KNO3, NaNO3 thường được dùng làm phân bón. Chúng có tính tan tốt trong nước và dễ hút ẩm.
Đặc điểm và tính chất vật lý của muối khan
Các tính chất muối khan cơ bản bao gồm:
- Tinh thể rắn ở điều kiện thường
- Nhiệt độ nóng chảy và sôi cao
- Độ tan trong nước khác nhau
- Có cấu trúc tinh thể ion điển hình
Đa số muối khan có màu trắng, một số muối của kim loại chuyển tiếp có màu đặc trưng. Ví dụ muối đồng(II) thường có màu xanh, muối sắt(III) có màu nâu đỏ.
Tính chất hóa học đặc trưng
Muối khan thường tham gia các phản ứng trao đổi ion khi tan trong nước. Chúng có thể phản ứng với axit, bazơ hoặc muối khác tạo kết tủa.
Khi nung nóng, nhiều muối khan bị phân hủy thành oxit kim loại và oxit phi kim. Ví dụ CaCO3 khi nung sẽ phân hủy thành CaO và CO2.
Một số muối khan có tính chất oxi hóa – khử mạnh. Điều này giúp chúng được ứng dụng rộng rãi trong công nghiệp điện phân, mạ điện.
Công thức hóa học và cách viết muối khan chuẩn
Muối khan là hợp chất vô cơ không chứa nước kết tinh. Việc nắm vững công thức muối khan giúp học sinh dễ dàng viết phương trình phản ứng hóa học.
Tôi thường ví von muối khan như một “ngôi nhà” được xây dựng từ gốc acid và kim loại. Mỗi thành phần đều có vai trò riêng trong việc tạo nên công thức hoàn chỉnh.
Nguyên tắc viết công thức muối khan
Để viết đúng công thức muối khan, cần tuân thủ 3 nguyên tắc cơ bản:
Kim loại luôn đứng trước gốc acid và viết hóa trị bằng số La Mã. Ví dụ: Fe(III), Cu(II).
Gốc acid giữ nguyên và đặt trong ngoặc đơn nếu có nhiều hơn 1 gốc. Ví dụ: (SO4), (NO3).
Cân bằng điện tích dương và âm bằng cách thêm chỉ số phù hợp. Ví dụ: Fe2(SO4)3.
Các công thức muối khan phổ biến
Trong quá trình giảng dạy 20 năm, tôi nhận thấy các muối khan công thức hóa học thường gặp gồm:
Muối Sulfat: CuSO4, Fe2(SO4)3, Al2(SO4)3
Muối Nitrat: AgNO3, Cu(NO3)2, Fe(NO3)3
Muối Clorua: NaCl, CaCl2, FeCl3
Mỗi loại muối đều có đặc điểm riêng về màu sắc và tính tan, giúp dễ dàng nhận biết trong phòng thí nghiệm.
Bài tập ví dụ về viết công thức muối khan
Bài 1: Viết công thức muối tạo bởi Fe(III) và gốc SO4(2-)
Giải:
- Hóa trị Fe(III) = +3
- Hóa trị SO4(2-) = -2
- Cân bằng điện tích: 2Fe(III) + 3SO4(2-) = 0
- Công thức: Fe2(SO4)3
Bài 2: Viết công thức muối tạo bởi Al(3+) và PO4(3-)
Giải:
- Hóa trị Al(3+) = +3
- Hóa trị PO4(3-) = -3
- Cân bằng điện tích: Al(3+) + PO4(3-) = 0
- Công thức: AlPO4
Phương pháp nhận biết và điều chế muối khan
Muối khan là dạng muối không chứa nước kết tinh. Việc nhận biết và điều chế muối khan đóng vai trò quan trọng trong phòng thí nghiệm và công nghiệp hóa chất.
Các phương pháp nhận biết muối khan
Để cách nhận biết muối khan chính xác, tôi thường hướng dẫn học sinh quan sát một số đặc điểm sau:
Muối khan thường có dạng bột mịn, khô ráo và không vón cục. Khi đun nóng nhẹ, muối khan không tan chảy hoặc thoát nước.
Phương pháp thử nghiệm đơn giản là cho muối vào ống nghiệm và đun nóng. Nếu không có giọt nước đọng trên thành ống nghiệm, đó là muối khan.
Phản ứng tạo thành muối khan
Các phản ứng tạo muối khan thường diễn ra theo các cơ chế sau:
Phản ứng trung hòa giữa axit và bazơ là phương pháp phổ biến nhất. Ví dụ phản ứng giữa HCl và NaOH tạo NaCl khan.
Phản ứng giữa kim loại với phi kim cũng tạo ra muối khan. Như Na phản ứng với Cl2 tạo thành NaCl khan.
Quy trình điều chế muối khan trong phòng thí nghiệm
Quy trình điều chế muối khan cần tuân thủ các bước sau:
Bước 1: Chuẩn bị dung dịch muối ban đầu đã được lọc trong.
Bước 2: Cô cạn dung dịch muối ở nhiệt độ thích hợp để loại nước.
Bước 3: Sấy khô sản phẩm ở 105-110°C trong 2-3 giờ.
Bước 4: Bảo quản muối khan trong bình hút ẩm kín để tránh hút nước từ không khí.
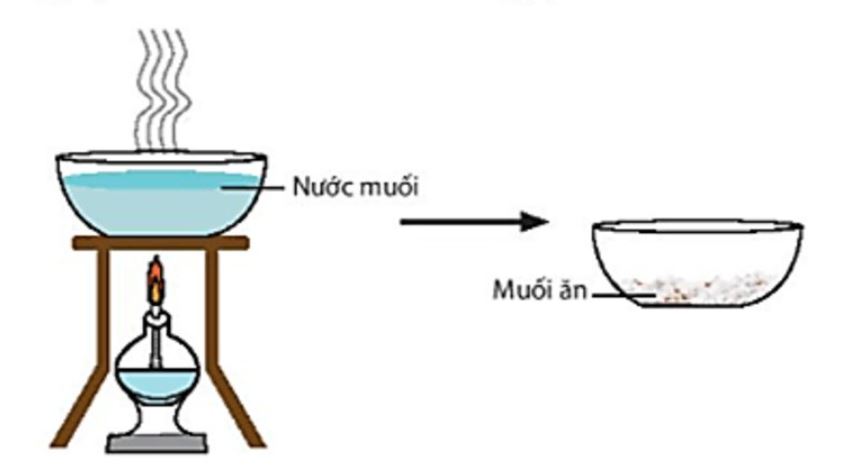
Trong quá trình giảng dạy, tôi luôn nhấn mạnh việc kiểm soát nhiệt độ sấy để tránh phân hủy muối và đảm bảo độ tinh khiết của sản phẩm.
Ứng dụng của muối khan trong đời sống và công nghiệp
Muối khan là một hợp chất vô cơ với công thức hóa học NaCl. Đây là loại muối phổ biến và có nhiều ứng dụng muối khan quan trọng trong cuộc sống cũng như sản xuất công nghiệp.

Vai trò của muối khan trong sinh hoạt
Muối khan trong đời sống đóng vai trò thiết yếu với sức khỏe con người. Nó tham gia vào quá trình dẫn truyền thần kinh và duy trì cân bằng điện giải trong cơ thể.
Trong chế biến thực phẩm, muối khan không chỉ là gia vị tạo vị mặn. Nó còn giúp bảo quản thực phẩm bằng cách ức chế sự phát triển của vi khuẩn gây hại.
Tôi thường khuyên học sinh nên nhớ muối khan còn có tác dụng làm sạch vết ố trên quần áo. Chỉ cần hòa tan muối với nước ấm và ngâm quần áo khoảng 30 phút.
Ứng dụng muối khan trong công nghiệp
Trong công nghiệp hóa chất, muối khan là nguyên liệu quan trọng để điều chế nhiều hợp chất khác. Quá trình điện phân muối nóng chảy tạo ra natri kim loại và khí clo.
Ngành công nghiệp dệt may sử dụng muối khan để cố định màu nhuộm. Tôi từng tham quan một nhà máy dệt, họ cho biết muối giúp màu vải bền đẹp và không bị phai.
Muối khan còn được dùng trong xử lý nước, làm mềm nước cứng. Muối khan công thức hóa học NaCl khi điện phân tạo ra chất khử trùng hiệu quả.
Lưu ý khi sử dụng muối khan
Cần bảo quản muối khan trong hộp kín, tránh ẩm ướt. Muối dễ hút ẩm và vón cục khi tiếp xúc với không khí ẩm.
Liều lượng sử dụng muối cần phù hợp, đặc biệt trong ăn uống. WHO khuyến cáo người trưởng thành không nên tiêu thụ quá 5g muối/ngày.
Trong công nghiệp, cần trang bị bảo hộ khi làm việc với muối khan. Dung dịch muối đậm đặc có thể gây ăn mòn kim loại và kích ứng da.
FAQ: Câu hỏi thường gặp về muối khan
Muối khan là một dạng muối không chứa nước kết tinh, được sử dụng phổ biến trong phòng thí nghiệm và công nghiệp. Tôi sẽ giải đáp các thắc mắc thường gặp về loại muối này.
Sự khác biệt giữa muối khan và muối ngậm nước
Muối khan hóa học khác biệt với muối ngậm nước ở thành phần và tính chất. Muối khan không chứa phân tử nước trong cấu trúc tinh thể.
Khi tiếp xúc với không khí ẩm, muối khan có khả năng hút ẩm mạnh và chuyển thành muối ngậm nước. Điều này làm thay đổi khối lượng phân tử của muối.
Muối khan thường có màu sắc nhạt hơn và độ tan trong nước cao hơn so với muối ngậm nước cùng loại.
Cách bảo quản muối khan
Muối khan cần được bảo quản trong bình kín, tránh tiếp xúc với không khí ẩm. Tôi thường hướng dẫn học sinh đặt bình đựng trong tủ hút ẩm.
Nhiệt độ bảo quản tốt nhất là 15-25°C, tránh để nơi có nhiệt độ cao gây phân hủy muối.
Nên sử dụng thìa hoặc spatula sạch, khô khi lấy muối khan để tránh nhiễm ẩm từ dụng cụ.
Độc tính của muối khan
Mức độ độc tính của muối khan phụ thuộc vào bản chất hóa học của từng loại muối cụ thể.
Một số muối khan như CuSO4 khan có độc tính cao, có thể gây kích ứng da, mắt và đường hô hấp nếu tiếp xúc trực tiếp.
Khi làm việc với muối khan, cần mang đầy đủ thiết bị bảo hộ như găng tay, kính bảo vệ mắt và khẩu trang để đảm bảo an toàn.
Kiến thức về muối khan công thức hóa học đóng vai trò quan trọng trong việc học tập và nghiên cứu hóa học. Các công thức muối khan giúp học sinh nắm vững cách viết, nhận biết và điều chế chất này trong phòng thí nghiệm. Việc phân loại và hiểu rõ tính chất của muối khan tạo nền tảng cho ứng dụng thực tiễn trong đời sống và công nghiệp. Mỗi loại muối khan đều có những đặc điểm riêng và cách sử dụng phù hợp.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

