Thuộc lòng công thức hóa học của canxi oxit và ứng dụng thực tế
Công thức hóa học của canxi oxit là nền tảng để hiểu về hợp chất vô cơ quan trọng này. Canxi oxit tồn tại phổ biến trong tự nhiên dưới dạng đá vôi. Chất này đóng vai trò thiết yếu trong công nghiệp sản xuất vật liệu xây dựng và nông nghiệp. Các phản ứng hóa học đặc trưng của nó tạo nên nhiều ứng dụng hữu ích trong đời sống hàng ngày.
Công thức hóa học của canxi oxit
Công thức hóa học của canxi oxit là CaO. Đây là một hợp chất vô cơ phổ biến trong tự nhiên và công nghiệp.
CaO được tạo thành từ 2 nguyên tố:
- Ca (Canxi): Nguyên tử có hóa trị +2
- O (Oxi): Nguyên tử có hóa trị -2
Trong quá trình giảng dạy, tôi thường giúp học sinh ghi nhớ công thức canxi oxit bằng cách liên hệ với vôi tôi – một vật liệu xây dựng quen thuộc. Vôi tôi chính là CaO.
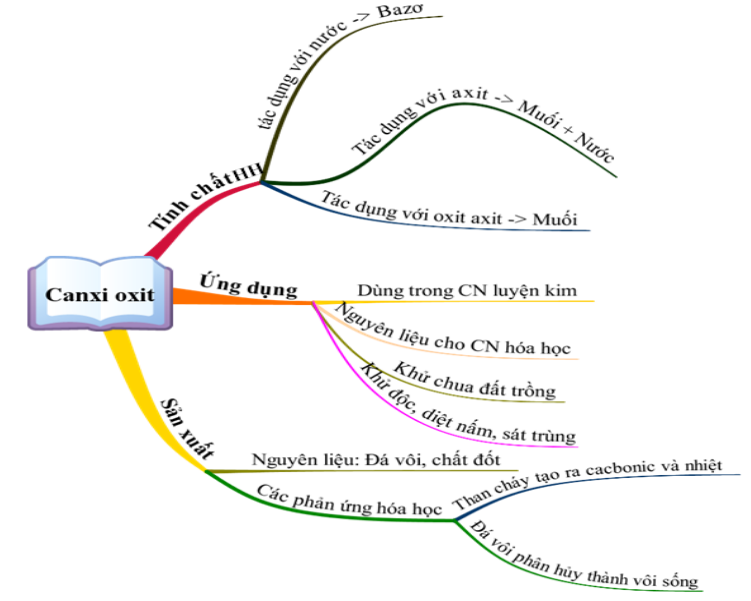
CaO được điều chế bằng cách nung đá vôi (CaCO3) ở nhiệt độ cao theo phương trình:
CaCO3 → CaO + CO2
Một mẹo nhỏ để nhớ công thức này là: “Ca luôn đứng trước, O luôn đứng sau – giống như cách viết tên người Việt Nam”. Cách này giúp học sinh của tôi không bao giờ viết nhầm thành OCa.
Khi tiếp xúc với nước, CaO tạo ra phản ứng tỏa nhiệt mạnh:
CaO + H2O → Ca(OH)2
Đây là phản ứng tôi thường làm thí nghiệm minh họa để học sinh dễ nhớ và hiểu rõ tính chất của CaO.
Cấu tạo và tính chất của canxi oxit (CaO)
Canxi oxit là một hợp chất vô cơ quan trọng, thường được gọi là vôi sống. Hợp chất này có vai trò thiết yếu trong nhiều ngành công nghiệp như xây dựng và sản xuất thủy tinh.
Cấu tạo phân tử của canxi oxit
Canxi oxit cấu tạo gồm liên kết ion giữa ion Ca2+ và O2-. Cấu trúc tinh thể của CaO có dạng lập phương tâm diện, tương tự như công thức hóa học của natri oxit.
Mỗi ion Ca2+ được bao quanh bởi 6 ion O2- theo hình bát diện. Điều này tạo nên một cấu trúc rất bền vững và ổn định.
Tính chất vật lý của canxi oxit
CaO hóa học tồn tại ở dạng bột màu trắng ở nhiệt độ thường. Chất này có nhiệt độ nóng chảy cao (2613°C) và nhiệt độ sôi khoảng 2850°C.
CaO không tan trong nước lạnh nhưng tan được trong nước nóng. Khi tiếp xúc với không khí ẩm, nó hút ẩm mạnh và chuyển thành Ca(OH)2.
Tính chất hóa học đặc trưng
Canxi oxit tính chất nổi bật là khả năng phản ứng mạnh với nhiều chất. Tương tự như công thức hóa học của oxygen, CaO thể hiện tính bazơ mạnh.
Phản ứng với nước
CaO tác dụng mạnh với nước tạo thành canxi hidroxit:
CaO + H2O → Ca(OH)2 + Q
Phản ứng này tỏa nhiệt mạnh, nhiệt độ có thể lên tới 90°C. Đây là phản ứng tôi thường dùng làm thí nghiệm minh họa cho học sinh.
Phản ứng với axit
CaO phản ứng với axit tạo muối và nước:
CaO + 2HCl → CaCl2 + H2O
CaO + H2SO4 → CaSO4 + H2O
Phản ứng với CO2
CaO hấp thụ CO2 trong không khí tạo thành CaCO3:
CaO + CO2 → CaCO3
Phản ứng này được ứng dụng trong việc làm sạch không khí và xử lý khí thải công nghiệp.
Các tên gọi và phân loại của canxi oxit
Canxi oxit là gì? Đây là một hợp chất vô cơ có công thức hóa học CaO, được tạo thành từ phản ứng nhiệt phân công thức canxi cacbonat. Hợp chất này có vai trò quan trọng trong công nghiệp và đời sống.
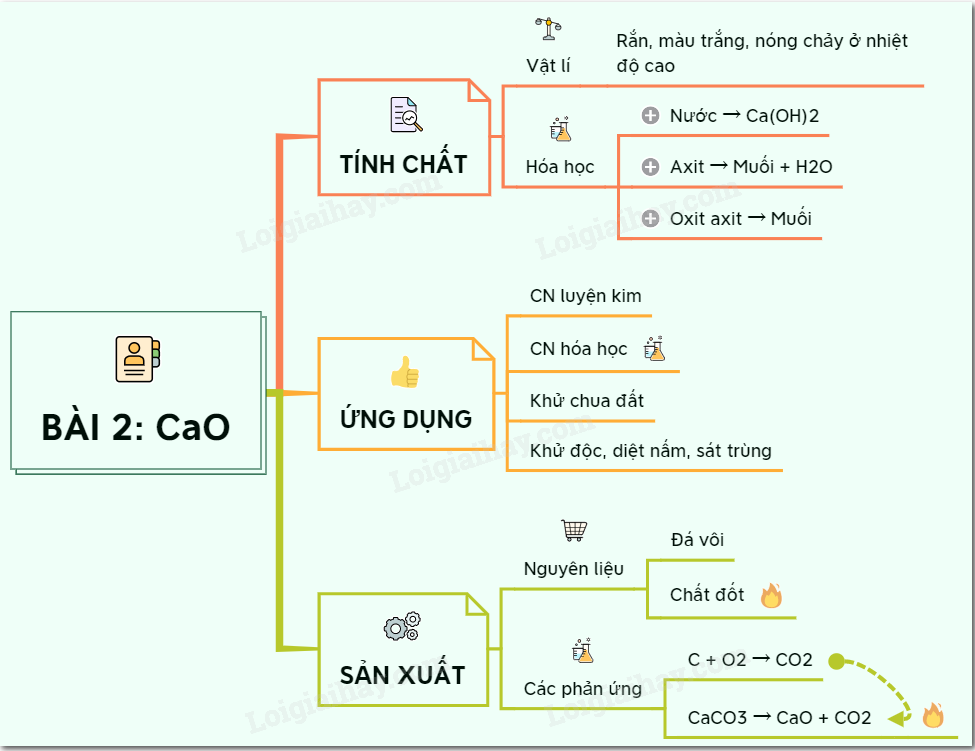
Trong thực tế, canxi oxit thường tồn tại dưới dạng bột màu trắng và có khả năng hút ẩm mạnh. Khi tiếp xúc với nước, nó tạo ra phản ứng tỏa nhiệt mạnh và chuyển thành canxi hidroxit Ca(OH)2.
Tên thường gọi và tên khoa học
Canxi oxit tên gọi khác phổ biến nhất là vôi sống, được sử dụng rộng rãi trong ngành xây dựng và nông nghiệp. Tên này xuất phát từ đặc tính “sống” – phản ứng mạnh mẽ với nước của hợp chất.
Trong hóa học, canxi oxit còn được gọi là calcium oxide (tiếng Anh) hoặc calx. Tên gọi calx có nguồn gốc từ tiếng Latin, thể hiện lịch sử lâu đời của việc sử dụng vôi trong các hoạt động của con người.
Phân loại theo nhóm hợp chất
Canxi oxit hợp chất thuộc nhóm oxit bazơ – một dạng oxit của kim loại. Khi phản ứng với nước, nó tạo thành bazơ tương ứng là Ca(OH)2.
Theo cấu tạo phân tử, vôi sống công thức CaO là một oxit ion, trong đó ion Ca2+ liên kết với ion O2- bằng liên kết ion. Đặc điểm này giải thích cho nhiệt độ nóng chảy cao và độ hòa tan thấp của hợp chất trong dung môi hữu cơ.
Phản ứng hóa học và ứng dụng của canxi oxit
Canxi oxit (CaO) là một hợp chất vô cơ phổ biến, thường được gọi là vôi sống. Chất này có nhiều phản ứng hóa học đặc trưng và ứng dụng quan trọng trong công nghiệp và đời sống.
Các phản ứng hóa học quan trọng
Công thức hóa học của canxi oxit tham gia nhiều phản ứng quan trọng. Phản ứng đầu tiên là với nước tạo thành công thức hóa học của canxi hiđroxit:
CaO + H2O → Ca(OH)2 + Q
Phản ứng tỏa nhiệt mạnh, tạo ra canxi hiđroxit có tính bazơ. Trong quá trình giảng dạy, tôi thường nhắc học sinh cẩn thận khi thực hiện phản ứng này.
Canxi oxit phản ứng với các oxit axit tạo muối. Ví dụ với CO2:
CaO + CO2 → CaCO3
Ứng dụng trong công nghiệp
Canxi oxit ứng dụng rộng rãi trong công nghiệp luyện kim. Nó được dùng làm chất trợ dung trong lò cao để loại bỏ tạp chất.

Trong công nghiệp xi măng, CaO là nguyên liệu chính để sản xuất Muối khan công thức hóa học. Nó chiếm tới 60-67% thành phần clinker xi măng.
Ngành công nghiệp giấy sử dụng CaO để tách lignin ra khỏi cellulose trong quá trình sản xuất bột giấy kraft.
Ứng dụng trong đời sống
CaO được dùng phổ biến trong xây dựng để sản xuất vữa xây. Khi trộn với nước và cát sẽ tạo thành hỗn hợp vữa bền chắc.
Trong nông nghiệp, nông dân thường rải vôi sống để cải tạo đất chua. CaO sẽ trung hòa độ pH của đất.
Ngành xử lý nước thải cũng sử dụng CaO để điều chỉnh pH và kết tủa các ion kim loại nặng độc hại.
FAQ: Câu hỏi thường gặp về canxi oxit
Canxi oxit là hợp chất phổ biến trong công nghiệp và đời sống. Tuy nhiên, nhiều người vẫn còn thắc mắc về tính chất và cách sử dụng an toàn của nó. Tôi sẽ giải đáp các câu hỏi thường gặp về công thức hóa học của canxi oxit.
Canxi oxit có độc không?
Canxi oxit không độc nhưng rất nguy hiểm nếu tiếp xúc trực tiếp. Chất này có tính ăn mòn mạnh, gây bỏng da và niêm mạc.
Khi tác dụng với nước, công thức hóa học của điphotpho pentaoxit sinh ra nhiệt độ cao có thể gây bỏng nặng. Vì vậy cần đeo găng tay, kính bảo hộ khi thao tác.
Cách bảo quản canxi oxit an toàn
Canxi oxit cần được bảo quản trong điều kiện khô ráo, tránh tiếp xúc với không khí ẩm. Tương tự như Công thức hóa học của nhôm, chất này dễ hút ẩm.
Đựng trong các thùng kín, có nắp đậy chắc chắn. Không để gần các chất như k2cr2o7 là gì hay kali clorua cấu tạo để tránh phản ứng không mong muốn.
Phân biệt canxi oxit với các oxit khác
Canxi oxit có màu trắng, dạng bột mịn. Khác với kali nitrat là gì, nó không tan trong nước mà tạo phản ứng tỏa nhiệt mạnh.
Khi tiếp xúc với không khí ẩm, canxi oxit chuyển thành canxi hidroxit. Đây là tính chất đặc trưng giúp phân biệt với các oxit kim loại khác.
Canxi oxit còn có khả năng hấp thụ khí CO2 tạo thành canxi cacbonat, đặc điểm này không có ở hầu hết các oxit khác.
Kiến thức về công thức hóa học của canxi oxit CaO là nền tảng quan trọng trong chương trình hóa học phổ thông. Hợp chất này có cấu tạo ion đơn giản nhưng sở hữu nhiều tính chất hóa học đặc trưng và ứng dụng thiết thực. Việc nắm vững cấu tạo, tính chất và phản ứng của CaO giúp học sinh dễ dàng vận dụng trong học tập và thực tiễn. Đây là một trong những oxit kim loại điển hình cần được nghiên cứu kỹ lưỡng.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

