Nắm rõ công thức cấu tạo của SO3 và các đặc điểm liên kết hóa học
Công thức cấu tạo của SO3 thể hiện cấu trúc phân tử phẳng với góc liên kết đặc trưng. Phân tử này có vai trò quan trọng trong sản xuất axit sunfuric. Các liên kết trong SO3 mang tính đối xứng cao và thể hiện sự lai hóa orbital độc đáo.
Công thức cấu tạo của SO3
SO3 (lưu huỳnh trioxit) có công thức cấu tạo của SO3 dạng phân tử tam giác phẳng. Trong đó, nguyên tử S ở trung tâm và 3 nguyên tử O ở 3 đỉnh tam giác.
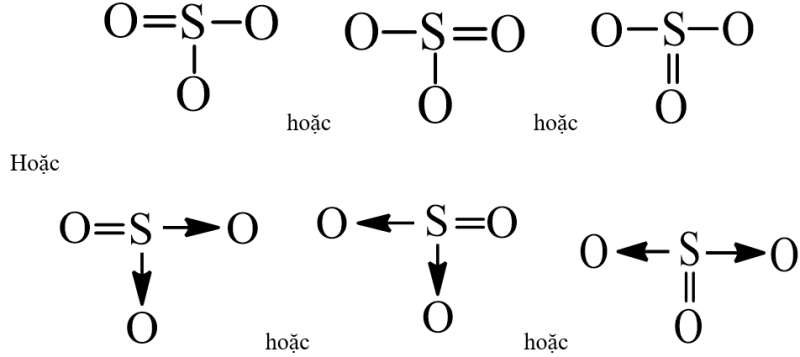
Cấu trúc phân tử SO3 được mô tả bằng công thức Lewis:
O=S=O
‖
O
Trong cấu trúc này, nguyên tử S tạo 3 liên kết đôi với 3 nguyên tử O. Mỗi liên kết đôi gồm 1 liên kết σ và 1 liên kết π.
Góc liên kết O-S-O trong phân tử SO3 là 120°. Đây là góc lý tưởng cho cấu trúc tam giác phẳng, giúp các electron phân bố đều và giảm lực đẩy tĩnh điện.
Qua 20 năm giảng dạy, tôi thường ví von cấu trúc SO3 như chiếc quạt 3 cánh. Điều này giúp học sinh dễ hình dung và nhớ được cấu trúc phân tử.
Khi vẽ công thức cấu tạo SO3, cần chú ý:
- Vẽ nguyên tử S ở trung tâm
- Vẽ 3 nguyên tử O ở 3 đỉnh tam giác
- Thể hiện rõ 3 liên kết đôi S=O
- Góc giữa các liên kết là 120°
Cấu tạo phân tử SO3 và các đặc điểm cơ bản
SO3 (lưu huỳnh trioxit) có cấu tạo phân tử SO3 dạng phẳng tam giác. Nguyên tử S ở trung tâm liên kết với 3 nguyên tử O theo dạng sp2.
Phân tử SO3 có cấu trúc đối xứng cao với 3 liên kết S-O tương đương nhau. Điều đặc biệt là các electron được phân bố đều trên 3 liên kết này.
Để hiểu rõ hơn về cấu trúc của SO3, bạn có thể tham khảo thêm công thức cấu tạo của SO2 để so sánh sự khác biệt.
Cấu tạo phân tử SO3 trong không gian
Hình dạng phân tử SO3 trong không gian là một tam giác đều. Nguyên tử S nằm ở tâm tam giác, còn 3 nguyên tử O nằm ở 3 đỉnh.
Cấu trúc này tạo nên một phân tử phẳng hoàn toàn, không có góc nghiêng. Các orbital lai hóa sp2 của S hướng về 3 nguyên tử O theo góc 120°.
Góc liên kết trong phân tử SO3
Các góc liên kết SO3 đều bằng 120°. Đây là kết quả của sự sắp xếp đối xứng của 3 orbital lai hóa sp2.
Góc 120° giúp giảm thiểu lực đẩy giữa các cặp electron liên kết. Điều này tạo nên cấu trúc bền vững cho phân tử.
Độ dài liên kết S-O trong SO3
Độ dài liên kết S-O trong SO3 là 142 pm (picomet). Ba liên kết S-O có độ dài bằng nhau do cấu trúc đối xứng.
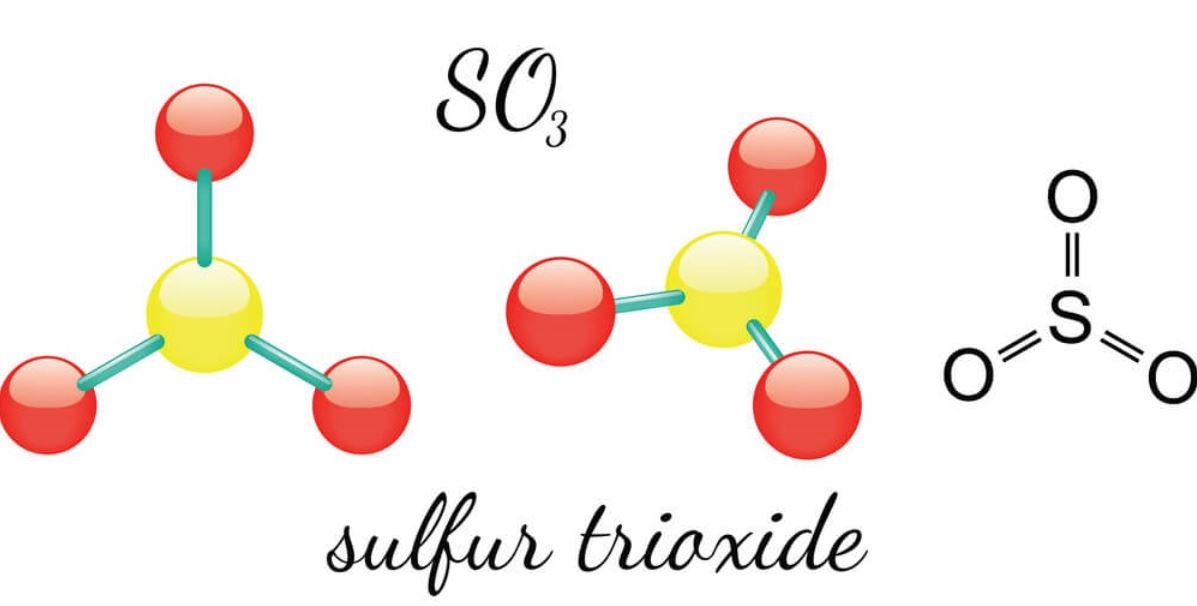
Liên kết S-O trong SO3 ngắn hơn so với liên kết đơn S-O thông thường. Nguyên nhân là do có sự tham gia của orbital d của lưu huỳnh tạo liên kết π.
Theo nghiên cứu của GS. John D. Roberts tại Viện Công nghệ California, độ dài liên kết này phản ánh tính chất liên kết π phân tán trong phân tử.
Liên kết hóa học và lai hóa trong SO3
SO3 là một phân tử có cấu trúc phẳng hình tam giác đều. Nguyên tử S ở trung tâm liên kết với 3 nguyên tử O. Sự phân bố electron và liên kết trong SO3 rất đặc biệt.
Các liên kết trong phân tử SO3
Trong SO3, liên kết trong SO3 được hình thành bởi 3 liên kết σ S-O và 3 liên kết π S-O. Mỗi nguyên tử O đều tạo một liên kết đôi với nguyên tử S trung tâm.
Các liên kết σ S-O được tạo bởi sự xen phủ trực tiếp giữa orbital lai hóa sp2 của S với orbital p của O. Liên kết π được hình thành từ orbital d của S và orbital p của O.
Sự lai hóa orbital trong SO3
Lai hóa SO3 xảy ra khi orbital 3s và hai orbital 3p của S lai hóa tạo thành 3 orbital lai sp2. Orbital d còn lại tham gia tạo liên kết π với O.
Quá trình lai hóa giúp phân tử SO3 đạt được cấu trúc bền vững nhất. Đây là kiến thức quan trọng để hiểu về h2so4 công thức cấu tạo.
Cấu hình electron của SO3
Cấu hình electron SO3 cho thấy nguyên tử S có 6 electron hóa trị, mỗi O có 6 electron hóa trị. Electron hóa trị SO3 phân bố đều trên các orbital lai hóa.
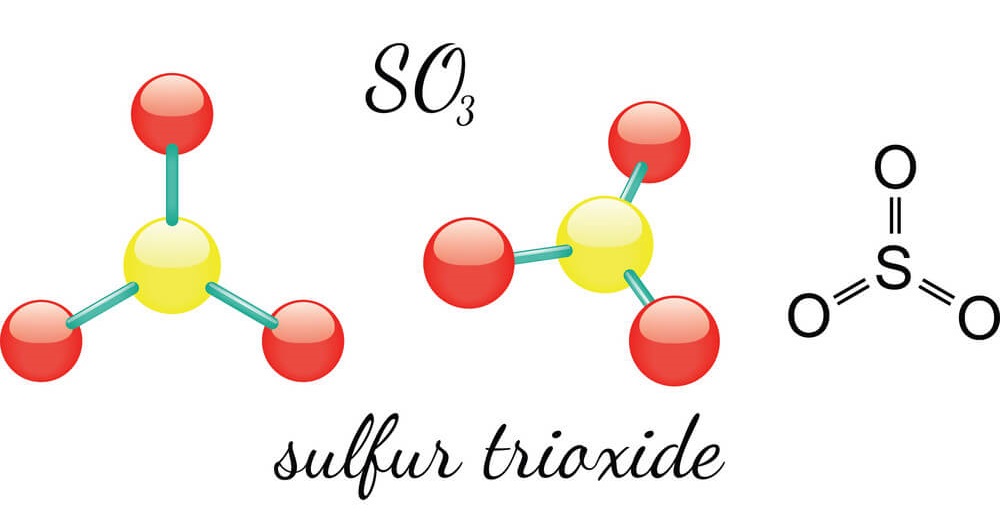
Trong phân tử, mỗi liên kết S-O chứa 4 electron (2 electron σ và 2 electron π). Tổng số electron liên kết là 18, tạo nên cấu trúc bền vững cho phân tử.
Các electron không liên kết trên nguyên tử O giúp phân tử có khả năng phản ứng mạnh với nước tạo thành axit sunfuric.
Ứng dụng và phản ứng của SO3 trong công nghiệp
SO3 (lưu huỳnh trioxit) đóng vai trò quan trọng trong nhiều quy trình công nghiệp. Công thức cấu tạo SO3 có cấu trúc phân tử dạng tam giác phẳng, với nguyên tử S ở trung tâm.
Trong công nghiệp, SO3 được sử dụng chủ yếu để sản xuất axit sunfuric và các hợp chất sunfat. Tương tự như cách viết công thức sắt 3 oxit, công thức SO3 là gì thường được học sinh nhầm lẫn khi viết.
Vai trò của SO3 trong sản xuất axit sunfuric
SO3 là chất trung gian quan trọng trong quy trình sản xuất axit sunfuric theo phương pháp tiếp xúc. Quá trình này diễn ra qua hai giai đoạn chính:
Giai đoạn 1: SO2 + 1/2O2 → SO3 (xúc tác V2O5)
Giai đoạn 2: SO3 + H2O → H2SO4
Hiệu suất của phản ứng phụ thuộc vào nhiệt độ và áp suất. Theo kinh nghiệm giảng dạy của tôi, nhiệt độ tối ưu khoảng 400-450°C và áp suất 1-2 atm.
Các phản ứng quan trọng của SO3
SO3 là một chất có tính oxi hóa mạnh và dễ phản ứng với nhiều chất. Các phản ứng đặc trưng bao gồm:
SO3 + H2O → H2SO4 (phản ứng tỏa nhiệt mạnh)
SO3 + NaOH → Na2SO4 + H2O
SO3 + CaO → CaSO4
Khi giảng dạy, tôi thường nhấn mạnh với học sinh về tính nguy hiểm của SO3 khi tiếp xúc với nước. Phản ứng xảy ra mạnh mẽ và có thể gây bỏng nặng.
FAQ: Câu hỏi thường gặp về SO3
SO3 là một hợp chất vô cơ quan trọng trong công nghiệp hóa chất. Tôi sẽ giải đáp các thắc mắc thường gặp về cấu tạo và tính chất của nó.
SO3 có cấu tạo như thế nào?
SO3 có cấu tạo như thế nào – đây là câu hỏi tôi thường nhận được từ học sinh. SO3 có cấu tạo phân tử gồm 1 nguyên tử S và 3 nguyên tử O.
Trong phân tử SO3, nguyên tử S liên kết với 3 nguyên tử O bằng 3 liên kết đôi S=O. Điều này tương tự như cấu tạo của công thức cấu tạo h2co3 nhưng thay C bằng S.
Tại sao SO3 có hình dạng phẳng?
SO3 có hình dạng phẳng do sự sắp xếp không gian của các electron hóa trị. Ba liên kết đôi S=O nằm trong cùng một mặt phẳng.
Góc liên kết O=S=O là 120° do lực đẩy electron giữa các liên kết đôi. Cấu trúc này giúp phân tử bền vững về mặt năng lượng.
SO3 có tính chất vật lý và hóa học gì đặc biệt?
SO3 ở điều kiện thường là chất lỏng không màu, dễ bay hơi. Nó có khả năng hút ẩm mạnh từ không khí.
Về tính chất hóa học, SO3 rất hoạt động. Nó tác dụng mạnh với nước tạo thành axit sunfuric H2SO4.
SO3 còn là tác nhân sunfon hóa quan trọng trong tổng hợp hữu cơ. Tôi thường nhấn mạnh với sinh viên về tính nguy hiểm của SO3 khi tiếp xúc với da.
Kiến thức về công thức cấu tạo của SO3 giúp học sinh nắm vững cấu trúc phân tử phẳng tam giác đều với góc liên kết 120° và liên kết S-O dài 142pm. Phân tử SO3 có sự lai hóa sp2 của nguyên tử S trung tâm tạo thành 3 liên kết σ với O. Đây là hợp chất quan trọng trong sản xuất axit sunfuric và các phản ứng công nghiệp. Các đặc điểm cấu tạo độc đáo này quyết định tính chất vật lý và hóa học của SO3.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

