Hiểu sâu công thức cấu tạo CO và các hợp chất hữu cơ quan trọng
Công thức cấu tạo CO thể hiện cách liên kết giữa các nguyên tử trong phân tử. Bài viết trình bày chi tiết cách viết công thức cấu tạo cho các hợp chất hữu cơ phổ biến. Các quy tắc và ví dụ minh họa giúp học sinh dễ dàng áp dụng vào thực tế.
Công thức cấu tạo CO và ý nghĩa trong hóa học
Carbon monoxide (CO) là một hợp chất hóa học quan trọng với công thức cấu tạo CO khá đơn giản nhưng thú vị.
Phân tử CO có cấu tạo tuyến tính với liên kết ba giữa nguyên tử carbon và oxygen:
C ≡ O
Trong đó:
- C: nguyên tử carbon có số oxi hóa +2
- O: nguyên tử oxygen có số oxi hóa -2
- Dấu ≡: thể hiện liên kết ba giữa C và O
Cấu trúc điện tử của CO rất đặc biệt. Phân tử có 10 electron hóa trị, trong đó:
- 4 electron từ nguyên tử carbon (2s2 2p2)
- 6 electron từ nguyên tử oxygen (2s2 2p4)
Kinh nghiệm giảng dạy của tôi cho thấy học sinh thường nhầm lẫn CO với CO2. Để phân biệt, các em cần nhớ CO chỉ có 1 liên kết ba với oxygen, còn CO2 có 2 liên kết đôi với oxygen.
CO đóng vai trò quan trọng trong nhiều phản ứng hóa học công nghiệp như:
- Tổng hợp methanol
- Sản xuất acid acetic
- Quá trình Fischer-Tropsch tạo hydrocarbon
Tuy nhiên, CO cũng là khí độc nguy hiểm vì có khả năng liên kết mạnh với hemoglobin trong máu, gây ngộ độc nghiêm trọng nếu hít phải.
Cách viết và biểu diễn công thức cấu tạo trong hóa học
Công thức cấu tạo đóng vai trò quan trọng trong việc mô tả cấu trúc phân tử của các hợp chất hóa học. Nó giúp thể hiện rõ vị trí và liên kết giữa các nguyên tử trong phân tử.
Để hiểu rõ hơn về cách viết và biểu diễn, chúng ta sẽ tìm hiểu chi tiết từng khía cạnh của công thức cấu tạo hóa học.
Khái niệm và vai trò của công thức cấu tạo
Công thức cấu tạo hóa học là cách biểu diễn chi tiết sự sắp xếp và liên kết của các nguyên tử trong phân tử. Nó cho biết số lượng, bản chất và vị trí tương đối của các nguyên tử.
Trong quá trình giảng dạy, tôi thường ví von công thức cấu tạo như bản thiết kế chi tiết của một ngôi nhà. Nó giúp ta hiểu được “kiến trúc” bên trong của phân tử.
Một ví dụ điển hình là công thức cấu tạo co2 với cấu trúc O=C=O, thể hiện rõ hai liên kết đôi giữa carbon và oxygen.
Các quy tắc viết công thức cấu tạo chuẩn
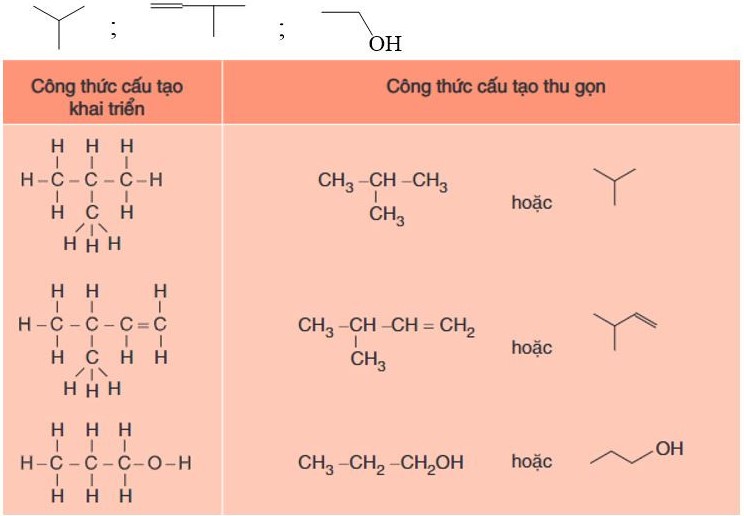
Khi viết công thức cấu tạo, cần tuân thủ các nguyên tắc cơ bản sau:
Nguyên tắc 1: Nguyên tử carbon luôn tạo 4 liên kết, hydrogen tạo 1 liên kết, oxygen tạo 2 liên kết.
Nguyên tắc 2: Các liên kết phải được thể hiện rõ ràng bằng gạch ngang (-), gạch kép (=) hoặc gạch ba (≡).
Kinh nghiệm của tôi cho thấy việc vẽ khung carbon trước, sau đó điền các nguyên tử khác sẽ giúp học sinh dễ dàng hơn trong việc viết công thức.
Phân biệt công thức cấu tạo và công thức phân tử
Công thức phân tử chỉ cho biết loại và số lượng nguyên tử trong phân tử. Ví dụ: C2H6O.
Công thức cấu tạo thể hiện chi tiết hơn về cách các nguyên tử liên kết. Cùng C2H6O có thể là CH3-CH2-OH (ethanol) hoặc CH3-O-CH3 (dimethyl ether).
Sự khác biệt này giúp giải thích hiện tượng đồng phân trong hóa học hữu cơ, khi các chất có cùng công thức phân tử nhưng cấu trúc và tính chất khác nhau.
Hướng dẫn viết công thức cấu tạo cho các hợp chất hữu cơ quan trọng
Công thức cấu tạo giúp biểu diễn cách các nguyên tử liên kết với nhau trong phân tử. Việc nắm vững cách viết công thức cấu tạo rất quan trọng để hiểu bản chất hóa học.
Tôi sẽ hướng dẫn chi tiết cách viết công thức cấu tạo cho từng nhóm hợp chất hữu cơ phổ biến. Mỗi nhóm có những đặc điểm cấu tạo riêng cần lưu ý.
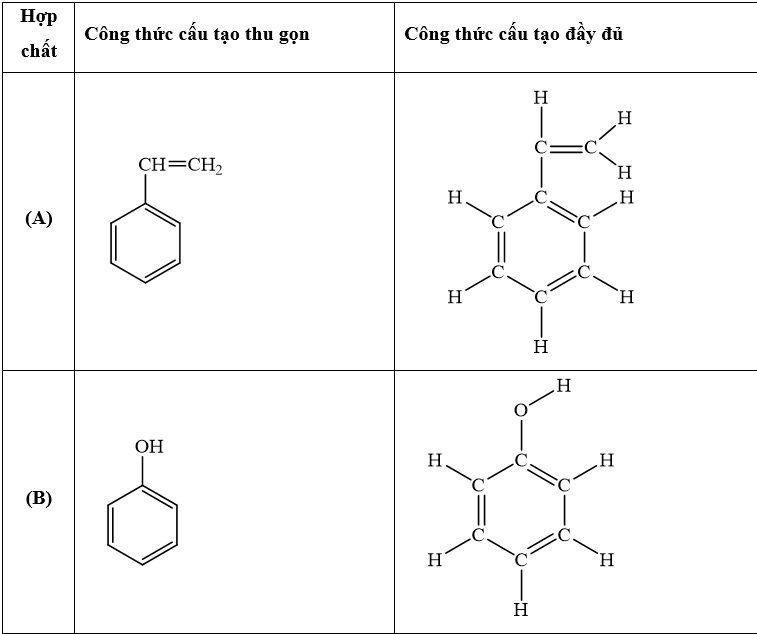
Công thức cấu tạo của ancol và phenol
Công thức cấu tạo của ancol có nhóm -OH gắn với carbon no. Ancol đơn giản nhất là CH3OH (metanol).
Khi viết công thức cấu tạo ancol, cần thể hiện rõ vị trí nhóm -OH và mạch carbon. Ví dụ: CH3-CH2-OH (etanol).
Công thức cấu tạo của phenol có nhóm -OH gắn trực tiếp vào vòng benzen. Phenol có công thức C6H5OH.
Công thức cấu tạo của anđehit và axit cacboxylic
Công thức cấu tạo của anđehit chứa nhóm -CHO ở đầu mạch. Anđehit đơn giản nhất là HCHO (metanal).
Công thức cấu tạo của axit có nhóm -COOH đặc trưng. Axit axetic CH3COOH là ví dụ điển hình.
Khi giảng dạy, tôi thường nhấn mạnh sự khác biệt giữa nhóm -CHO và -COOH để học sinh không nhầm lẫn.
Công thức cấu tạo của este và amin
Công thức cấu tạo của este có cấu trúc R-COO-R’, trong đó R và R’ là gốc hydrocarbon.
Công thức cấu tạo của amin chứa nhóm -NH2, -NHR hoặc -NR2. Amin đơn giản nhất là CH3NH2.
Este thường được tạo ra từ phản ứng giữa ancol và axit cacboxylic, như stiren công thức cấu tạo.
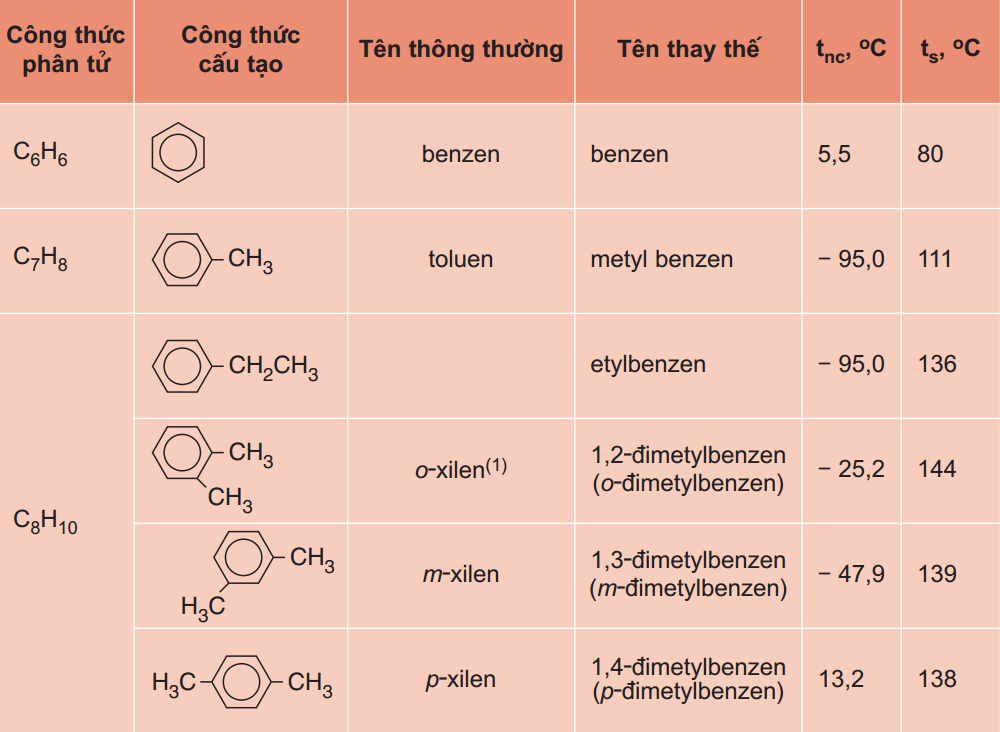
Công thức cấu tạo của benzen và dẫn xuất
Công thức cấu tạo của benzen là vòng 6 cạnh với 3 liên kết đôi xen kẽ. Benzen có công thức phân tử C6H6.
Các dẫn xuất benzen như cumen là gì được tạo thành khi thay thế H bằng các nhóm thế.
Khi vẽ công thức cấu tạo benzen, tôi khuyên học sinh nên vẽ vòng 6 cạnh trước rồi mới thêm liên kết đôi.
Ứng dụng công thức cấu tạo trong học tập và nghiên cứu hóa học
Công thức cấu tạo đóng vai trò then chốt trong việc nghiên cứu và phát triển hóa học. Nó giúp các nhà khoa học hiểu rõ cấu trúc phân tử và dự đoán phản ứng hóa học. Công thức cấu tạo co giản của các hợp chất hữu cơ là nền tảng để phát triển các vật liệu mới.
Xác định cấu trúc phân tử và tính chất hóa học
Việc xác định cấu trúc phân tử giúp dự đoán được tính chất vật lý và hóa học của hợp chất. Các nhóm chức trong phân tử quyết định khả năng phản ứng với các chất khác.
Trong 20 năm giảng dạy, tôi thường ví von cấu trúc phân tử như bản thiết kế của một ngôi nhà. Mỗi liên kết hóa học là một cột trụ, còn các nguyên tử là các phòng ốc được kết nối với nhau.
Dự đoán phản ứng và sản phẩm
Hiểu rõ cấu trúc phân tử giúp dự đoán chính xác sản phẩm của phản ứng hóa học. Các electron trong phân tử di chuyển theo quy luật nhất định khi tham gia phản ứng.
Kinh nghiệm cho thấy học sinh thường nhớ tốt hơn khi vẽ sơ đồ chuyển electron. Việc này giúp hình dung rõ cơ chế phản ứng diễn ra như thế nào.

Ứng dụng trong công nghiệp polymer
Ngành công nghiệp polymer phát triển dựa trên hiểu biết về cấu trúc của các monomer. Công thức cấu tạo cao su buna-s là ví dụ điển hình về polymer tổng hợp.
Các nhà khoa học nghiên cứu cấu trúc phân tử để tạo ra vật liệu có tính năng mới. Polymer thông minh có khả năng thay đổi hình dạng theo nhiệt độ hoặc ánh sáng.
Việc kiểm soát cấu trúc phân tử giúp điều chỉnh độ bền, tính đàn hồi của vật liệu. Đây là cơ sở để sản xuất các sản phẩm polymer đáp ứng nhu cầu đa dạng của cuộc sống.
FAQ: Câu hỏi thường gặp về công thức cấu tạo
Công thức cấu tạo là nền tảng quan trọng giúp hiểu được cấu trúc phân tử và tính chất của hợp chất. Tôi sẽ giải đáp một số thắc mắc phổ biến về chủ đề này.
Làm sao để ghi nhớ công thức cấu tạo hiệu quả?
Sau 20 năm giảng dạy, tôi nhận thấy việc ghi nhớ công thức cấu tạo cần có phương pháp khoa học. Trước tiên, cần hiểu rõ quy luật liên kết giữa các nguyên tử trong phân tử.
Một cách hiệu quả là vẽ lại công thức nhiều lần, bắt đầu từ nguyên tử trung tâm rồi mở rộng dần ra các nhánh. Điều này giúp hình thành trí nhớ thị giác về cấu trúc phân tử.
Ngoài ra, việc liên hệ công thức với các vật thể quen thuộc trong cuộc sống sẽ tạo ấn tượng sâu sắc. Ví dụ, cấu trúc benzen giống như một bánh xe đạp có 6 nan hoa.
Cách kiểm tra công thức cấu tạo đúng hay sai?
Kiểm tra công thức cấu tạo cần dựa vào các nguyên tắc cơ bản. Đầu tiên, xác định hóa trị của các nguyên tố và số liên kết có thể tạo ra.
Tiếp theo, kiểm tra tổng số electron hóa trị và số electron dùng để liên kết. Nếu có sự chênh lệch bất thường, công thức có thể sai.
Cuối cùng, so sánh với các đồng phân cấu tạo đã biết để tránh nhầm lẫn. Kinh nghiệm cho thấy nhiều học sinh thường mắc lỗi khi vẽ các đồng phân.
Mối liên hệ giữa công thức cấu tạo và tính chất vật lý?
Cấu trúc phân tử quyết định trực tiếp nhiều tính chất vật lý của chất. Các nhóm chức trong phân tử ảnh hưởng đến nhiệt độ sôi, nhiệt độ nóng chảy và độ tan.
Ví dụ, các hợp chất có cùng khối lượng phân tử nhưng khác công thức cấu tạo sẽ có nhiệt độ sôi khác nhau. Điều này do sự khác biệt về lực tương tác giữa các phân tử.
Khi giảng dạy, tôi thường lấy ví dụ về rượu etylic và đimetyl ete. Hai chất này có cùng công thức phân tử C2H6O nhưng nhiệt độ sôi chênh lệch tới 100°C do cấu trúc khác nhau.
Việc nắm vững công thức cấu tạo CO và các hợp chất hữu cơ là nền tảng quan trọng trong học tập hóa học. Các quy tắc viết công thức cấu tạo giúp học sinh dễ dàng biểu diễn cấu trúc phân tử và hiểu được bản chất liên kết hóa học. Kiến thức này đóng vai trò then chốt trong việc dự đoán phản ứng, tổng hợp vật liệu polymer và nghiên cứu phát triển các hợp chất mới trong công nghiệp hóa chất.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

