Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
C3H6O3 công thức cấu tạo là một hợp chất hữu cơ đa chức năng. Phân tử này tồn tại dưới nhiều dạng đồng phân cấu trúc khác nhau. Axit lactic là dạng phổ biến nhất của C3H6O3 trong tự nhiên. Hợp chất này đóng vai trò quan trọng trong quá trình chuyển hóa năng lượng của cơ thể.
C3H6O3 công thức cấu tạo và đặc điểm phân tử
C3H6O3 là gì? Đây là công thức phân tử của axit lactic – một axit hữu cơ quan trọng trong cơ thể sống. Tôi thường ví von nó như “người anh em” của axit axetic trong gia đình các axit cacboxylic.
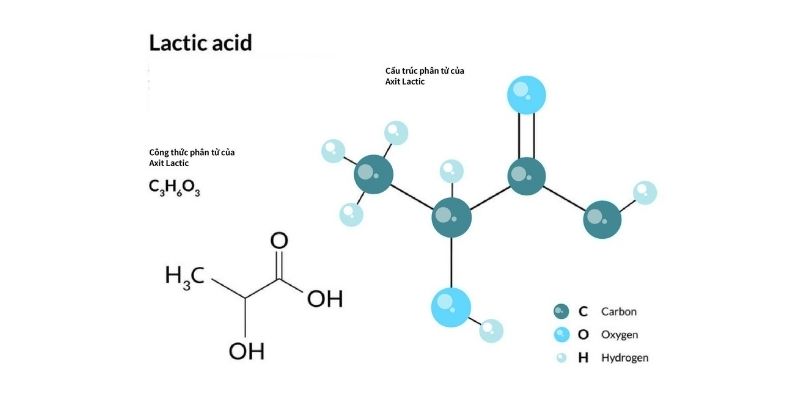
C3H6O3 công thức cấu tạo có dạng CH3-CH(OH)-COOH. Phân tử này có cấu trúc đặc biệt với:
- 1 nhóm cacboxyl (-COOH)
- 1 nhóm hydroxyl (-OH)
- 1 nhóm metyl (-CH3)
Trong quá trình giảng dạy, tôi thường nhấn mạnh với học sinh về 3 đặc điểm quan trọng của phân tử này:
Thứ nhất, phân tử có cấu trúc mạch hở, không phân nhánh với 3 nguyên tử cacbon liên kết đơn.
Thứ hai, phân tử có tính bất đối xứng do carbon số 2 mang nhóm -OH là carbon bất đối xứng.
Thứ ba, phân tử có khả năng tham gia phản ứng este hóa nhờ sự có mặt của cả nhóm -OH và -COOH.
Một điều thú vị là axit lactic có mặt trong sữa chua, đây là ví dụ tôi hay dùng để học sinh dễ nhớ về hợp chất này. Khi sữa bị lên men, vi khuẩn lactic sẽ chuyển hóa đường lactose thành axit lactic.
Cấu trúc phân tử và các dạng đồng phân của C3H6O3
Phân tử C3H6O3 có nhiều dạng đồng phân khác nhau do sự đa dạng trong cách sắp xếp các nguyên tử. Việc hiểu rõ cấu trúc và các dạng đồng phân giúp nắm vững tính chất hóa học của hợp chất này.
Phương pháp vẽ công thức cấu tạo C3H6O3
Để vẽ công thức cấu tạo, trước tiên xác định số liên kết có thể tạo ra:
- C: 4 liên kết/nguyên tử
- H: 1 liên kết/nguyên tử
- O: 2 liên kết/nguyên tử
Tương tự như cách vẽ công thức cấu tạo của c2h6, ta bắt đầu từ khung carbon rồi thêm các nhóm chức.
Kinh nghiệm 20 năm giảng dạy cho thấy học sinh dễ nhớ nhất khi vẽ theo trình tự: Vẽ khung C -> Thêm O -> Nối H cho đủ hóa trị.
Các dạng đồng phân của C3H6O3
C3H6O3 đồng phân tồn tại ở nhiều dạng cấu trúc khác nhau. Dạng phổ biến nhất là axit lactic với công thức CH3-CHOH-COOH.
Một số dạng đồng phân khác bao gồm:
- CH2OH-CH2-COOH (axit 3-hydroxypropanoic)
- CH3-O-CH2-COOH (axit methoxyacetic)
Tương tự như công thức cấu tạo c6h14, các đồng phân này có cùng công thức phân tử nhưng khác nhau về cấu trúc không gian.
Liên kết hóa học trong phân tử C3H6O3
 Cấu trúc phân tử và các dạng đồng phân của C3H6O3
Cấu trúc phân tử và các dạng đồng phân của C3H6O3Trong phân tử C3H6O3 tồn tại các liên kết cộng hóa trị đơn C-C, C-H, C-O và O-H. Các liên kết này có độ dài và năng lượng khác nhau.
Liên kết C-O trong nhóm -OH có độ phân cực lớn hơn so với C-O trong nhóm -COOH. Điều này ảnh hưởng trực tiếp đến tính acid của phân tử.
Góc liên kết giữa các nguyên tử carbon xấp xỉ 109.5° theo cấu trúc tứ diện. Đây là yếu tố quan trọng quyết định hình dạng không gian của phân tử.
Axit lactic – Dạng phổ biến nhất của C3H6O3
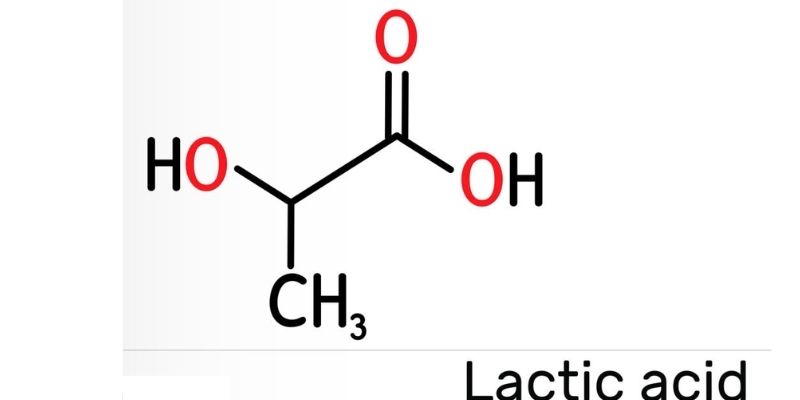
Axit lactic là một hợp chất hữu cơ thuộc nhóm axit cacboxylic với công thức cấu tạo axit lactic là CH3-CH(OH)-COOH.
Đây là một chất lỏng không màu, tan tốt trong nước và có vị chua đặc trưng. Cấu trúc phân tử của nó tương tự như công thức cấu tạo của c 3 h 8 nhưng thay một nguyên tử H bằng nhóm OH.
Axit lactic có thể tồn tại ở hai dạng đồng phân quang học là D-lactic và L-lactic, tương tự như công thức C6H12 với các cấu hình không gian khác nhau.
Cấu trúc phân tử axit lactic
Phân tử axit lactic có 3 nguyên tử cacbon liên kết với nhau tạo thành chuỗi cacbon thẳng.
Nguyên tử cacbon giữa mang nhóm hydroxyl (-OH), tạo nên tính chất đặc trưng của axit α-hydroxy. Nhóm cacboxyl (-COOH) ở đầu chuỗi quyết định tính axit của phân tử.
Liên kết hóa học trong phân tử chủ yếu là liên kết đơn C-C và C-H, riêng nhóm cacboxyl có một liên kết đôi C=O.
Vai trò của axit lactic trong sữa chua
 Axit lactic – Dạng phổ biến nhất của C3H6O3
Axit lactic – Dạng phổ biến nhất của C3H6O3Axit lactic trong sữa chua được tạo ra từ quá trình lên men của vi khuẩn có lợi Lactobacillus và Streptococcus.
Vi khuẩn này chuyển hóa đường lactose trong sữa thành axit lactic, tạo nên vị chua đặc trưng và kết cấu đông đặc của sữa chua.
Axit lactic còn giúp bảo quản sữa chua tự nhiên bằng cách tạo môi trường pH thấp, ức chế sự phát triển của vi khuẩn có hại.
Sự hình thành axit lactic trong cơ thể
Axit lactic trong cơ thể được tạo ra chủ yếu trong quá trình chuyển hóa glucose khi thiếu oxy.
Khi vận động mạnh, cơ bắp không được cung cấp đủ oxy sẽ chuyển sang phân giải glucose theo con đường yếm khí, tạo ra axit lactic.
Sự tích tụ axit lactic trong cơ bắp gây cảm giác mỏi cơ và đau nhức. Tuy nhiên, cơ thể sẽ nhanh chóng chuyển hóa axit lactic thành glucose khi được nghỉ ngơi và cung cấp đủ oxy.
Tính chất và ứng dụng của C3H6O3
Axit lactic C3H6O3 là một axit hữu cơ quan trọng, có vai trò thiết yếu trong nhiều quá trình sinh học và công nghiệp. Chất này được tìm thấy tự nhiên trong sữa chua và các sản phẩm lên men.
Tính chất vật lý của C3H6O3
C3H6O3 tính chất vật lý nổi bật là chất lỏng không màu, có vị chua đặc trưng. Nhiệt độ nóng chảy của axit lactic là 16,8°C và nhiệt độ sôi là 122°C.

Axit lactic tan tốt trong nước, cồn và ete. Khối lượng riêng của nó là 1,209 g/cm3 ở 20°C. Tương tự như cấu tạo licopen, axit lactic cũng có khả năng hòa tan trong dung môi hữu cơ.
Tính chất hóa học đặc trưng
Axit lactic có tính axit yếu hơn các axit vô cơ như HCl. Nó tác dụng được với kim loại hoạt động, bazơ và muối cacbonat tạo muối lactat tương ứng.
Khi đun nóng, phân tử axit lactic có thể tự ngưng tụ tạo thành polyme axit polylactic (PLA). Quá trình này tương tự như phản ứng trùng ngưng của cấu tạo cumen.
Axit lactic còn tham gia phản ứng este hóa với rượu tạo thành este có mùi thơm đặc trưng.
Ứng dụng trong công nghiệp và đời sống
Axit lactic được sử dụng rộng rãi trong công nghiệp thực phẩm làm chất bảo quản, điều vị. Nó là thành phần quan trọng trong quá trình lên men sữa chua, dưa muối.
Trong công nghiệp dược phẩm, axit lactic dùng sản xuất thuốc và mỹ phẩm. Polyme của nó (PLA) được ứng dụng làm vật liệu y tế phân hủy sinh học.
Ngành công nghiệp dệt may sử dụng axit lactic để xử lý vải, nhuộm màu. Nó còn là nguyên liệu quan trọng trong sản xuất nhựa sinh học thân thiện môi trường.
Axit alpha hydroxy và vai trò sinh học của C3H6O3
Axit alpha hydroxy là nhóm hợp chất hữu cơ có nhóm hydroxyl (-OH) gắn với carbon alpha. Đại diện tiêu biểu là axit lactic C3H6O3 – một axit hữu cơ quan trọng trong cơ thể.
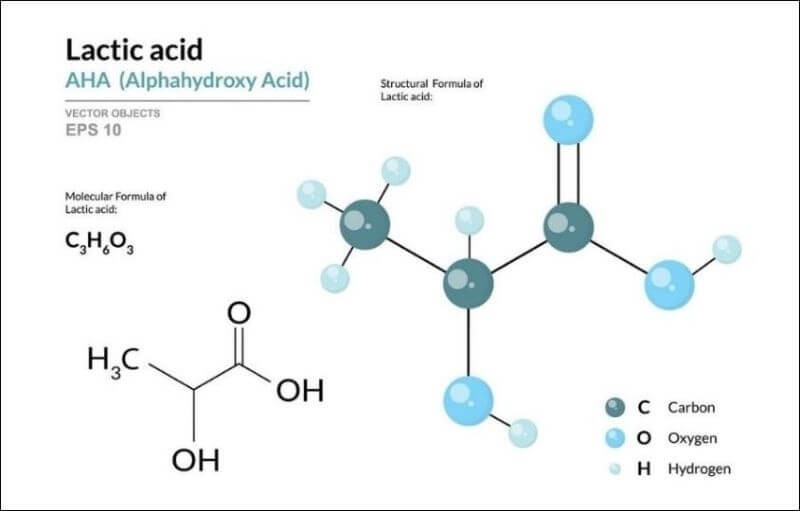
Cấu trúc phân tử của axit lactic có thể so sánh với liên kết trong CH3Cl và công thức cấu tạo ch3oh về mặt liên kết hóa học.
Đặc điểm của nhóm alpha hydroxy
Nhóm alpha hydroxy có đặc điểm cấu tạo đặc trưng với nhóm -OH và -COOH trên cùng phân tử. Vị trí nhóm -OH ở carbon alpha tạo ra tính chất đặc biệt.
Khả năng phân ly proton của nhóm carboxyl được tăng cường nhờ sự có mặt của nhóm -OH. Điều này làm tăng độ acid của phân tử.
Nhóm alpha hydroxy còn có khả năng tham gia phản ứng oxi hóa khử và tạo liên kết hydro. Các tính chất này quyết định vai trò sinh học quan trọng.
Chức năng sinh học trong cơ thể
Axit alpha hydroxy đóng vai trò then chốt trong quá trình chuyển hóa năng lượng của tế bào. Chúng tham gia vào chu trình Krebs sản sinh ATP.
Trong cơ bắp, axit lactic được tạo ra khi thiếu oxy, giúp duy trì hoạt động co cơ. Quá trình này được gọi là đường phân kỵ khí.
Theo nghiên cứu của Viện Dinh dưỡng Quốc gia, axit lactic còn có tác dụng điều hòa pH môi trường đường ruột và hỗ trợ hệ vi sinh đường ruột khỏe mạnh.
FAQ: Câu hỏi thường gặp về C3H6O3
Axit lactic C3H6O3 là một hợp chất hữu cơ quan trọng trong nhiều quá trình sinh học và công nghiệp. Dưới đây là một số câu hỏi thường gặp về hợp chất này.
Sự khác biệt giữa các dạng đồng phân C3H6O3?
Có 2 dạng đồng phân chính của C3H6O3 là axit lactic và axit 3-hydroxypropanoic. Axit lactic tồn tại dưới 2 dạng đồng phân quang học D và L.
D-lactic acid thường được tạo ra bởi vi khuẩn lactic, trong khi L-lactic acid được tạo ra trong cơ thể người trong quá trình chuyển hóa glucose.
Tại sao C3H6O3 quan trọng trong quá trình lên men?
C3H6O3 đóng vai trò then chốt trong quá trình lên men lactic. Nó là sản phẩm cuối cùng của quá trình chuyển hóa glucose trong điều kiện yếm khí.
Vi khuẩn lactic chuyển hóa đường thành axit lactic, tạo môi trường acid giúp bảo quản thực phẩm như dưa chua, kim chi.
Trong cơ bắp, khi thiếu oxy, glucose được chuyển hóa thành axit lactic gây mỏi cơ.
Cách nhận biết C3H6O3 trong phòng thí nghiệm?
C3H6O3 có thể được nhận biết qua phản ứng với dung dịch NaOH tạo muối lactat. Khi cho thêm FeCl3 sẽ tạo phức màu vàng đặc trưng.
Có thể dùng phương pháp chuẩn độ với NaOH và chỉ thị phenolphtalein để xác định nồng độ axit lactic.
Phương pháp sắc ký lỏng hiệu năng cao (HPLC) cũng được sử dụng để định lượng chính xác hàm lượng axit lactic.
Việc nghiên cứu công thức cấu tạo C3H6O3 giúp làm rõ cấu trúc phân tử và các đặc tính quan trọng của hợp chất này. Phân tử C3H6O3 tồn tại dưới nhiều dạng đồng phân, trong đó axit lactic đóng vai trò thiết yếu trong quá trình chuyển hóa năng lượng của cơ thể và công nghiệp thực phẩm. Các tính chất đặc trưng và ứng dụng đa dạng của C3H6O3 đã khẳng định vị trí quan trọng của hợp chất này trong đời sống và sản xuất công nghiệp.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Tổng quan về tơ capron công thức và ứng dụng trong hóa học 12
Tìm hiểu chi tiết về tơ capron công thức cấu tạo, phương pháp điều chế và quy trình sản xuất. Khám phá tính chất đặc trưng, ứng dụng trong dệt may và các lĩnh vực công nghiệp quan trọng.

