Công thức hóa học của ketamin và ứng dụng trong y tế hiện đại
Công thức hóa học của ketamin là một cấu trúc phân tử phức tạp với nhiều đặc tính độc đáo. Chất này có vai trò quan trọng trong y học hiện đại. Các đặc điểm cấu tạo phân tử ketamin quyết định tính chất và ứng dụng của nó. Bài viết phân tích chi tiết cấu trúc và đặc tính hóa học của ketamin.
Công thức hóa học của ketamin
Ketamin có công thức hoá học của ketamin là C13H16ClNO. Đây là một hợp chất hữu cơ thuộc nhóm arylcyclohexylamine.
Về cấu trúc phân tử, ketamin cấu tạo phân tử gồm một vòng cyclohexanone được gắn với một nhóm phenyl chloride và một nhóm methylamino. Các nguyên tử được liên kết với nhau tạo thành một cấu trúc không gian 3 chiều đặc trưng.
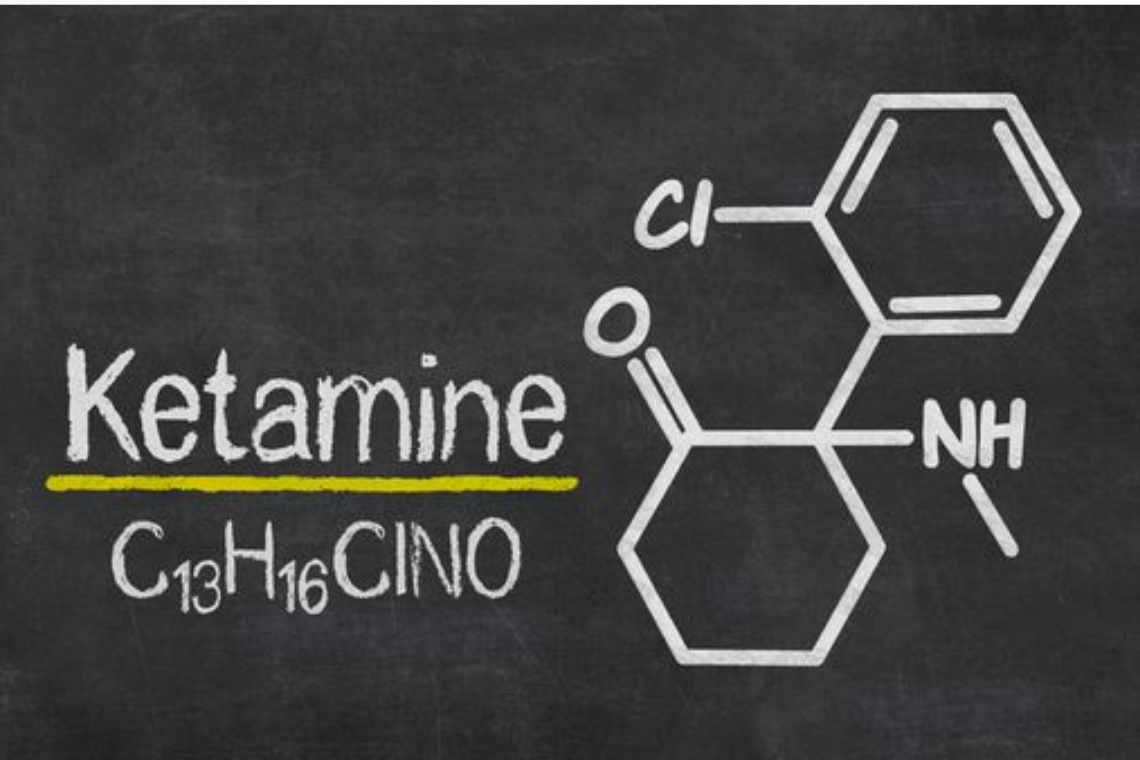
Công thức cấu tạo chi tiết của ketamin:
2-(2-chlorophenyl)-2-(methylamino)cyclohexanone
Trong đó:
- C13: 13 nguyên tử carbon tạo khung
- H16: 16 nguyên tử hydro
- Cl: 1 nguyên tử clo
- N: 1 nguyên tử nitơ
- O: 1 nguyên tử oxy
Ketamin tồn tại dưới 2 dạng đồng phân quang học R(-) và S(+). Trong y học, dạng S(+) được sử dụng phổ biến hơn do có tác dụng mạnh gấp 3-4 lần so với dạng R(-).
Với kinh nghiệm giảng dạy của tôi, để học sinh dễ nhớ cấu trúc ketamin, tôi thường ví von nó như một “cái móc áo” với vòng cyclohexanone là phần cong, còn nhóm phenyl chloride và methylamino như hai “tay móc” đối xứng.
Ketamin và các đặc điểm cấu tạo phân tử
Ketamin là một hợp chất hóa học thuộc nhóm amin có cấu trúc phân tử phức tạp. Để hiểu rõ về ketamin và thành phần hóa học của nó, chúng ta cần tìm hiểu từ lịch sử phát hiện đến các đặc điểm cấu tạo phân tử.
Ketamin là gì và lịch sử phát hiện
Ketamin là một loại thuốc gây mê được tổng hợp lần đầu vào năm 1962 bởi Calvin Stevens tại phòng thí nghiệm Parke Davis. Ban đầu, nó được phát triển như một chất thay thế cho phencyclidine (PCP) trong gây mê.
Với công thức phân tử C13H16ClNO, ketamin có cấu trúc tương tự như công thức phân tử của etylamin nhưng phức tạp hơn. Khác với công thức phân tử của trimetylamin là, ketamin có thêm vòng cyclohexanone và nhóm chloro.
Cấu trúc phân tử của ketamin
Phân tử ketamin có cấu trúc đặc trưng với một vòng cyclohexanone và một nhóm amin bậc hai. Vòng cyclohexanone tạo nên khung xương chính của phân tử, mang tính cứng và ổn định.
Nhóm amin trong cấu trúc ketamin đóng vai trò quan trọng trong hoạt tính sinh học. Nó tương tác với các thụ thể NMDA trong não, tạo nên tác dụng gây mê đặc trưng.
Các dạng đồng phân của ketamin
Ketamin tồn tại dưới hai dạng đồng phân quang học là S(+) và R(-). Dạng S(+)-ketamin có hoạt tính mạnh gấp 3-4 lần so với dạng R(-).
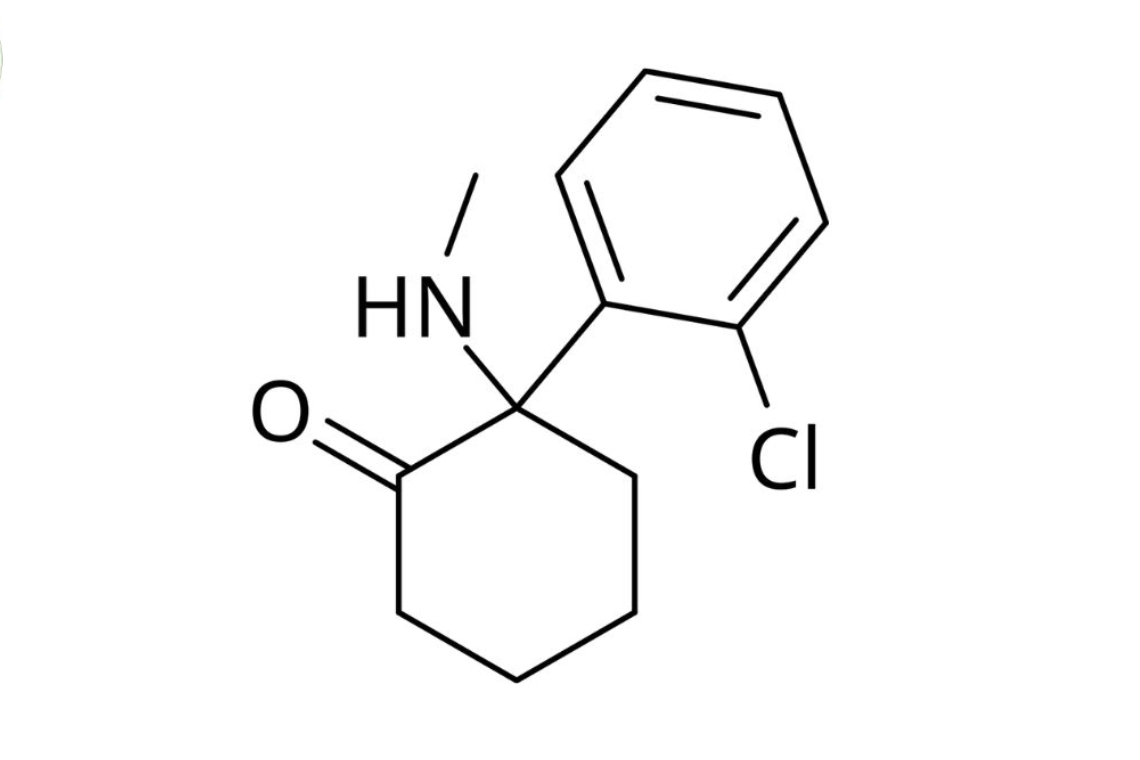
Sự khác biệt về hoạt tính giữa hai đồng phân là do cấu hình không gian khác nhau. Điều này ảnh hưởng trực tiếp đến khả năng tương tác với thụ thể trong cơ thể.
Trong thực tế lâm sàng, dạng hỗn hợp racemic (tỷ lệ 1:1 của hai đồng phân) được sử dụng phổ biến nhất. Tuy nhiên, xu hướng hiện nay là sử dụng dạng S(+) tinh khiết để giảm thiểu tác dụng phụ.
Các dạng tồn tại và đặc tính hóa học của ketamin
Ketamin là một hợp chất hóa học thuộc nhóm arylcyclohexylamine, có cấu trúc phân tử phức tạp. Chất này tồn tại ở nhiều dạng khác nhau và có những đặc tính hóa học độc đáo.
Cấu trúc phân tử của ketamin có điểm tương đồng với công thức metan ở nhóm CH3. Tuy nhiên, ketamin phức tạp hơn nhiều với vòng cyclohexanone và nhóm phenyl.
Ketamin dạng tinh thể và bột
Ketamin dạng bột là dạng phổ biến nhất, có màu trắng và mịn như bột đường. Dạng bột được tạo thành từ quá trình nghiền nhỏ tinh thể ketamin.
Tinh thể ketamin có dạng hình kim, trong suốt, tương tự như công thức kim cương. Chúng được hình thành qua quá trình kết tinh từ dung dịch.
Tính chất vật lý của ketamin
Ketamin có điểm nóng chảy từ 258-261°C ở áp suất thường. Chất này tan tốt trong các dung môi hữu cơ như cồn, ether.

Trong môi trường nước, ketamin thể hiện tính tan vừa phải. Độ tan của nó phụ thuộc nhiều vào nhiệt độ và pH của dung dịch.
Phản ứng hóa học đặc trưng
Ketamin tham gia phản ứng thế electrophile ở vòng thơm. Phản ứng này tạo ra các dẫn xuất mới có hoạt tính sinh học khác nhau.
Trong môi trường acid, ketamin có khả năng tạo muối với các acid vô cơ. Muối ketamin hydrochloride là dạng phổ biến nhất.
Phản ứng oxi hóa ketamin tạo ra các sản phẩm phân hủy đặc trưng. Các sản phẩm này thường được dùng để định danh ketamin trong phân tích pháp y.
Ứng dụng của ketamin trong y học và tác dụng sinh học
Ketamin trong y học đóng vai trò quan trọng như một thuốc gây mê và giảm đau mạnh. Thuốc được sử dụng rộng rãi trong phẫu thuật và cấp cứu.
Tương tự như công thức hóa học của vitamin c, ketamin có cấu trúc phân tử đặc biệt giúp nó thể hiện nhiều tác dụng sinh học. Các nhà khoa học đã nghiên cứu và phát triển nhiều ứng dụng mới của ketamin.
Cơ chế tác dụng của ketamin
Ketamin thuốc mê tác động chủ yếu lên thụ thể NMDA trong não. Nó ngăn chặn glutamate – chất dẫn truyền thần kinh chính gây kích thích não bộ.
Giống như cách công thức hoá học baking soda tạo phản ứng trung hòa, ketamin cũng tạo ra các phản ứng sinh hóa phức tạp. Thuốc làm giảm hoạt động của vùng não kiểm soát cảm giác đau và ý thức.
Quá trình này diễn ra nhanh chóng, chỉ trong vài phút sau khi tiêm ketamin vào cơ thể. Điều này giúp bác sĩ kiểm soát tốt tình trạng của bệnh nhân.

Ketamin trong gây mê và giảm đau
Ketamin gây mê được sử dụng phổ biến trong các ca phẫu thuật nhỏ và trung bình. Thuốc có ưu điểm là tác dụng nhanh và thời gian hồi phục ngắn.
Theo nghiên cứu của Hiệp hội Gây mê Hoa Kỳ (2022), ketamin giúp giảm đau hiệu quả trong 85% ca phẫu thuật. Bệnh nhân tỉnh táo nhanh và ít gặp các tác dụng phụ nghiêm trọng.
Liều lượng ketamin được điều chỉnh tùy theo cân nặng và tình trạng của từng bệnh nhân. Bác sĩ gây mê luôn theo dõi sát các chỉ số sinh tồn trong suốt quá trình.
Các tác dụng phụ và nguy cơ
Ketamin có thể gây một số tác dụng không mong muốn như:
- Ảo giác và mơ màng: Thường gặp khi tỉnh dậy sau gây mê
- Tăng huyết áp và nhịp tim: Cần theo dõi ở bệnh nhân tim mạch
- Buồn nôn và nôn: Có thể kiểm soát bằng thuốc chống nôn
Việc sử dụng ketamin cần được chỉ định và giám sát chặt chẽ bởi bác sĩ chuyên khoa. Lạm dụng thuốc có thể gây nghiện và tổn thương não nghiêm trọng.
Các bác sĩ luôn cân nhắc kỹ lợi ích và nguy cơ trước khi quyết định dùng ketamin. Thuốc chỉ được sử dụng trong môi trường y tế chuyên nghiệp.
FAQ: Câu hỏi thường gặp về ketamin
Ketamin là một loại thuốc gây mê được sử dụng rộng rãi trong y tế. Tuy nhiên, việc lạm dụng ketamin có thể gây ra nhiều tác hại nghiêm trọng.
Để phát hiện ketamin, các chuyên gia thường sử dụng quỳ tím công thức hóa học làm chất chỉ thị. Phương pháp này giúp xác định nhanh chóng sự hiện diện của ketamin trong mẫu thử.
Ngoài ra, công thức hoá học của thuốc tím cũng được ứng dụng trong quy trình kiểm nghiệm ketamin. Các phản ứng màu đặc trưng giúp phân biệt ketamin với các chất khác.
Một số phòng thí nghiệm sử dụng kali đicromat là gì để kiểm tra độ tinh khiết của ketamin. Phương pháp này cho kết quả chính xác cao.
Trong quá trình phân tích, các chuyên gia thường kết hợp nhiều phương pháp khác nhau. tripanmitin là chất gì đôi khi được dùng làm chất chuẩn để so sánh kết quả.
Việc kiểm nghiệm ketamin cần được thực hiện bởi các chuyên gia có chuyên môn. Kết quả phân tích giúp đảm bảo an toàn cho người sử dụng trong y tế.
Việc nghiên cứu công thức hóa học của ketamin đã mang lại những hiểu biết quan trọng về cấu trúc phân tử và đặc tính của hợp chất này. Ketamin có cấu trúc phân tử phức tạp với nhiều dạng đồng phân, tồn tại ở dạng tinh thể và bột với những tính chất hóa học đặc trưng. Trong y học, ketamin được ứng dụng rộng rãi làm thuốc gây mê và giảm đau dưới sự kiểm soát chặt chẽ của các chuyên gia y tế. Các phản ứng hóa học của ketamin cần được nghiên cứu kỹ lưỡng để đảm bảo an toàn khi sử dụng trong điều trị.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

