Thuộc lòng ancol benzylic công thức cấu tạo và tính chất hóa học cơ bản
Ancol benzylic công thức cấu tạo là một hợp chất hữu cơ thơm quan trọng. Cấu trúc phân tử độc đáo của nó bao gồm vòng benzen và nhóm hydroxyl methyl. Các phản ứng đặc trưng và ứng dụng đa dạng khiến ancol benzylic trở thành chất nền tảng trong tổng hợp hữu cơ.
Ancol benzylic công thức cấu tạo và đặc điểm phân tử
Ancol benzylic là hợp chất hữu cơ có nhóm -CH2OH gắn trực tiếp vào vòng benzen. Ancol benzylic công thức cấu tạo có dạng C6H5-CH2OH.
Cấu trúc phân tử của ancol benzylic gồm hai phần chính:
- Vòng benzen (C6H5-): Mang tính thơm đặc trưng
- Nhóm -CH2OH: Quyết định tính chất ancol
Tương tự như ancol anlylic công thức, ancol benzylic có khả năng phân ly proton từ nhóm -OH dễ dàng hơn các ancol no thông thường.
Trong quá trình giảng dạy, tôi thường ví von ancol benzylic như một “cây cầu nối” giữa hợp chất thơm và ancol. Điều này giúp học sinh dễ nhớ cấu trúc đặc biệt của nó.
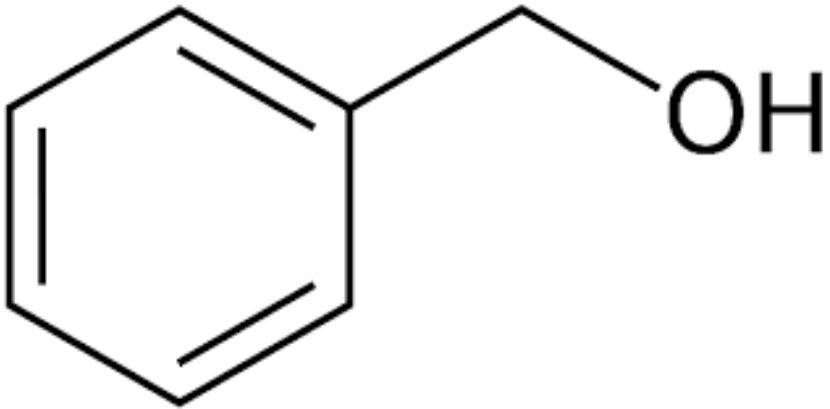
Phản ứng đặc trưng của ancol benzylic là oxi hóa tạo aldehyd:
C6H5-CH2OH + [O] → C6H5-CHO + H2O
Một số ví dụ điển hình về ancol benzylic:
- Benzyl ancol (C6H5CH2OH)
- p-methylbenzyl ancol (p-CH3C6H4CH2OH)
- m-chlorobenzyl ancol (m-ClC6H4CH2OH)
Cấu trúc phân tử và nhóm chức của ancol benzylic
Ancol benzylic là hợp chất hữu cơ có nhóm -CH2OH gắn trực tiếp vào vòng benzen. Đây là một nhóm chất quan trọng trong hóa học hữu cơ và công nghiệp hóa chất.
Tương tự như công thức ankin là gì, ancol benzylic có công thức tổng quát là C6H5-CH2OH. Cấu trúc này cho thấy sự kết hợp độc đáo giữa vòng thơm và nhóm ancol.
Công thức phân tử và công thức cấu tạo
Phenylmethanol là đại diện đơn giản nhất của nhóm công thức ancol benzylic. Công thức phân tử của nó là C7H8O.
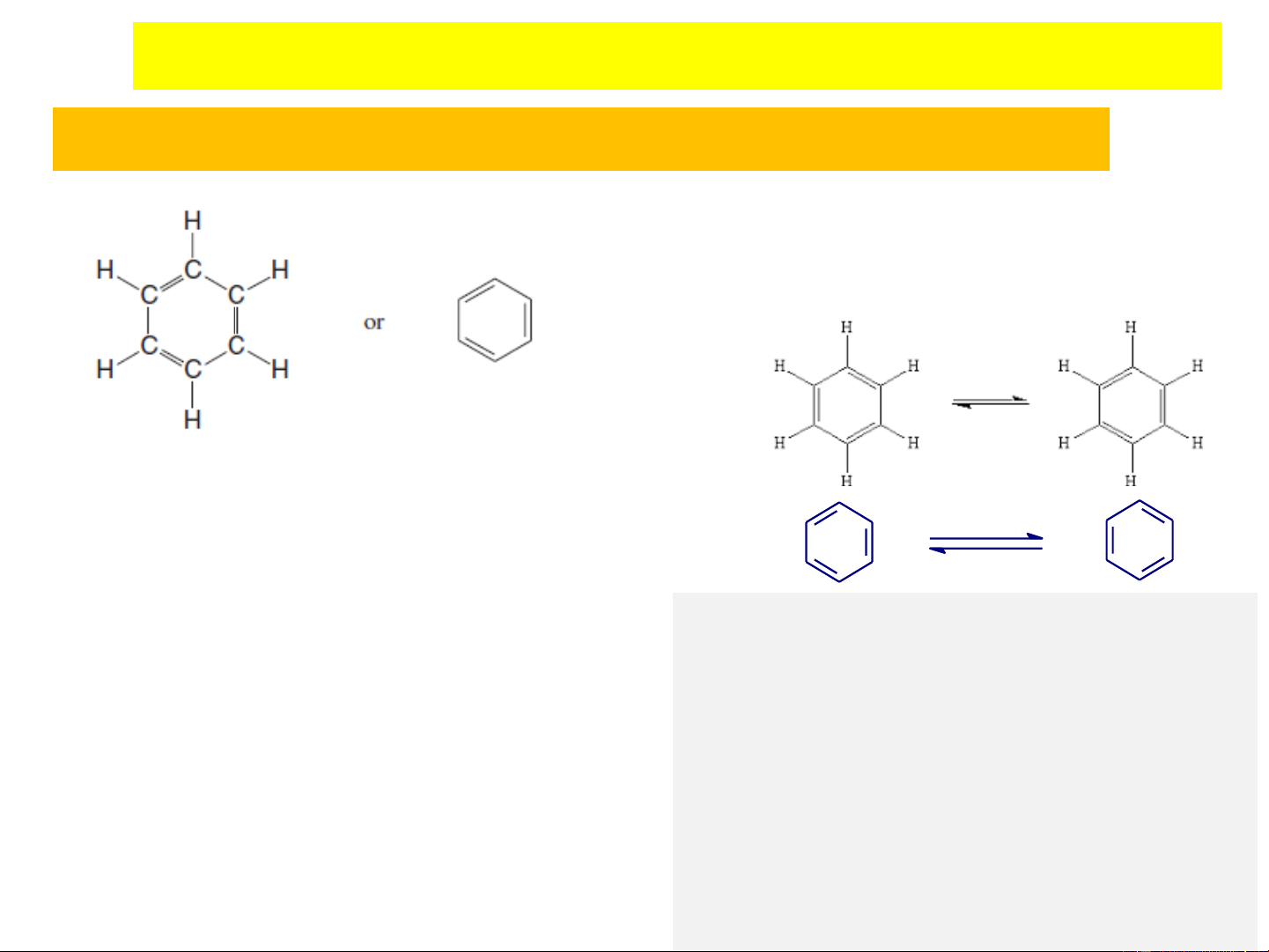
Trong công thức cấu tạo, vòng benzen C6H5- liên kết với nhóm -CH2OH tạo thành một chuỗi carbon mạch thẳng. Liên kết này tạo ra tính chất đặc trưng của ancol benzylic.
Các dạng đồng phân
Ancol benzylic có thể tồn tại dưới nhiều dạng đồng phân khác nhau. Vị trí nhóm -CH2OH trên vòng benzen quyết định tính chất của hợp chất.
Các đồng phân ortho, meta và para tạo ra những tính chất khác biệt về độ tan, nhiệt độ sôi và khả năng phản ứng. Điều này làm cho việc nghiên cứu ancol benzylic trở nên thú vị.
Nhóm chức đặc trưng
Cấu tạo phenylmethanol được đặc trưng bởi nhóm hydroxyl (-OH) gắn với carbon bậc một. Nhóm này quyết định tính chất hóa học của hợp chất.
Sự có mặt của vòng benzen và nhóm -CH2OH tạo ra khả năng phản ứng đặc biệt. Ancol benzylic dễ dàng tham gia phản ứng oxi hóa tạo thành aldehyd thơm.
Trong quá trình giảng dạy, tôi thường nhấn mạnh rằng nhóm -CH2OH là “cầu nối” giữa phần thơm và phần ancol của phân tử. Điều này giúp học sinh dễ nhớ và hiểu rõ cấu trúc.
Tính chất hóa học của ancol benzylic trong phản ứng
Tính chất ancol benzylic thể hiện rõ qua các phản ứng đặc trưng. Nhóm -CH2OH gắn trực tiếp với vòng benzen tạo nên độ hoạt động cao. Điều này giúp ancol benzylic tham gia nhiều phản ứng quan trọng.
Các phản ứng của ancol benzylic có liên quan mật thiết với axit linoleic công thức khi tham gia phản ứng oxi hóa tạo sản phẩm.
Phản ứng oxi hóa
Ancol benzylic dễ dàng bị oxi hóa thành aldehyd hoặc xeton tương ứng. Phản ứng này xảy ra nhanh chóng ở nhiệt độ thường với tác nhân oxi hóa nhẹ.
Công thức tổng quát:
R-CH2OH + [O] → R-CHO + H2O
Trong đó R là gốc phenyl hoặc các dẫn xuất của phenyl. Phản ứng oxi hóa thường dùng KMnO4 hoặc K2Cr2O7 làm chất oxi hóa.
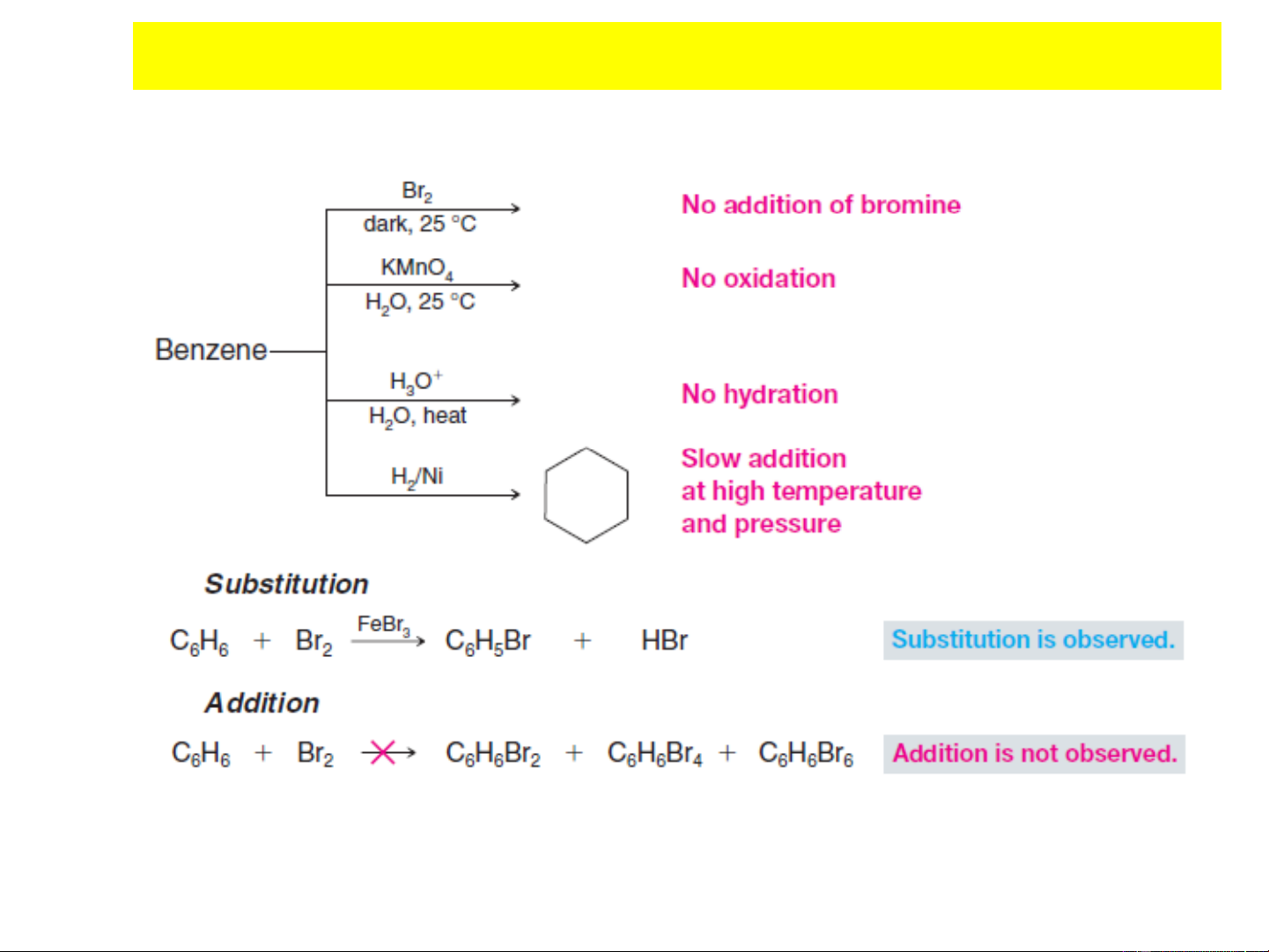
Phản ứng thế
Ancol benzylic tham gia phản ứng thế nucleophil dễ dàng hơn các ancol no. Nhóm -OH được thay thế bởi các halogen tạo halogenua benzylic.
Phản ứng với HCl tạo thành clorua benzylic:
C6H5CH2OH + HCl → C6H5CH2Cl + H2O
Sản phẩm halogenua benzylic rất hoạt động và thường được dùng làm chất trung gian tổng hợp.
Phản ứng cộng
Ancol benzylic có khả năng tham gia phản ứng cộng vào liên kết đôi C=C. Phản ứng thường xảy ra ở điều kiện xúc tác axit.
Ví dụ phản ứng với etilen:
C6H5CH2OH + CH2=CH2 → C6H5CH2OCH2CH3
Phản ứng cộng tạo ra các ete không đối xứng có ứng dụng quan trọng trong tổng hợp hữu cơ.
Phương pháp điều chế ancol benzylic trong phòng thí nghiệm và công nghiệp
Điều chế ancol benzylic là quá trình tổng hợp hóa học quan trọng trong ngành công nghiệp hóa chất. Quá trình này có thể thực hiện qua nhiều con đường khác nhau tùy thuộc vào nguyên liệu đầu và quy mô sản xuất.
Tương tự như Ancol propylic công thức, ancol benzylic cũng có thể được điều chế bằng nhiều phương pháp khác nhau. Mỗi phương pháp có những ưu nhược điểm riêng và phù hợp với từng mục đích sử dụng cụ thể.
Điều chế từ các hợp chất benzyl
Phương pháp phổ biến nhất là thủy phân benzyl halide với dung dịch kiềm loãng:
C6H5CH2X + NaOH → C6H5CH2OH + NaX
(X = Cl, Br, I)
Phản ứng này diễn ra trong điều kiện nhiệt độ phòng và cho hiệu suất cao. Tôi thường hướng dẫn học sinh thực hiện phản ứng này với benzyl clorua vì an toàn và dễ kiểm soát.
Một cách khác là oxi hóa toluen bằng KMnO4 trong môi trường acid:
C6H5CH3 + [O] → C6H5CH2OH
Điều chế từ phản ứng khử
Phản ứng khử aldehyd benzoic bằng LiAlH4 hoặc NaBH4 cho hiệu suất rất tốt:
C6H5CHO + H2 → C6H5CH2OH
Phương pháp này đặc biệt phù hợp trong phòng thí nghiệm vì:
- Phản ứng diễn ra nhanh và hoàn toàn
- Điều kiện phản ứng dễ kiểm soát
- Sản phẩm tinh khiết, ít tạp chất
Quy trình sản xuất công nghiệp
Trong sản xuất ancol benzylic công nghiệp, phương pháp chủ yếu là khử benzaldehyd bằng hydro hóa xúc tác:
C6H5CHO + H2 → C6H5CH2OH (xúc tác Ni/Raney)
Quy trình này có nhiều ưu điểm như nguyên liệu rẻ và sẵn có. Tuy nhiên cần kiểm soát chặt chẽ nhiệt độ và áp suất để tránh phản ứng phụ.

Kinh nghiệm của tôi cho thấy việc duy trì nhiệt độ ổn định ở 50-60°C và áp suất 3-5 atm sẽ cho hiệu suất tối ưu khoảng 85-90%.
Ứng dụng của ancol benzylic trong đời sống và công nghiệp
Ancol benzylic hay phenylmethanol là hợp chất hữu cơ quan trọng với nhiều ứng dụng đa dạng. Hợp chất này có cấu trúc đặc biệt khi vừa chứa nhóm hydroxyl vừa có vòng benzen.
Tương tự như ancol butylic công thức, ancol benzylic có khả năng phản ứng đa dạng. Điều này giúp nó trở thành nguyên liệu quan trọng trong nhiều lĩnh vực.
Ứng dụng trong tổng hợp hữu cơ
Ancol benzylic đóng vai trò then chốt trong tổng hợp nhiều hợp chất hữu cơ phức tạp. Hợp chất này có thể chuyển hóa thành aldehyd thông qua phản ứng oxi hóa nhẹ.
Trong phòng thí nghiệm, ancol benzylic thường được sử dụng làm chất bảo vệ nhóm hydroxyl. Phản ứng này giúp bảo vệ nhóm -OH khỏi các tác nhân không mong muốn.
Theo nghiên cứu của Viện Hóa học (2022), ancol benzylic còn là tiền chất quan trọng trong tổng hợp các hợp chất mạch vòng phức tạp.
Ứng dụng trong công nghiệp

Trong công nghiệp nhuộm, ancol benzylic được sử dụng làm dung môi pha loãng thuốc nhuộm. Khả năng hòa tan tốt giúp nó trở thành lựa chọn phổ biến.
Ngành công nghiệp mỹ phẩm sử dụng ancol benzylic làm chất định hương và chất bảo quản. Hợp chất này có mùi thơm dễ chịu và khả năng kháng khuẩn tốt.
Ứng dụng trong y dược
Ancol benzylic là nguyên liệu quan trọng trong tổng hợp nhiều loại thuốc. Đặc biệt là các thuốc kháng viêm và giảm đau.
Trong sản xuất thuốc, ancol benzylic thường được este hóa tạo thành các este có hoạt tính sinh học. Các este này có khả năng thấm qua màng tế bào tốt hơn.
Các nghiên cứu gần đây còn phát hiện tiềm năng kháng khuẩn của ancol benzylic. Điều này mở ra hướng phát triển thuốc kháng sinh mới.
FAQ: Câu hỏi thường gặp về ancol benzylic
Ancol benzylic là hợp chất hữu cơ thường được sử dụng trong công nghiệp hóa chất. Dưới đây là một số câu hỏi phổ biến về loại ancol này.
Ancol benzylic có độc không?
Ancol benzylic có độc tính trung bình với cơ thể con người. Khi tiếp xúc trực tiếp, nó có thể gây kích ứng da và niêm mạc.
Theo nghiên cứu của Viện Hóa học Công nghiệp, liều gây độc cấp tính LD50 qua đường miệng ở chuột là 1230 mg/kg trọng lượng cơ thể.
Cần tránh hít phải hơi của ancol benzylic vì có thể gây đau đầu, chóng mặt và buồn nôn.
Cách bảo quản ancol benzylic
Ancol benzylic cần được bảo quản trong bình kín, tránh ánh sáng trực tiếp và nhiệt độ cao.
Nhiệt độ bảo quản tối ưu là 15-25°C trong phòng thí nghiệm có hệ thống thông gió tốt.
Không để gần các chất oxy hóa mạnh vì có thể gây phản ứng nguy hiểm.
So sánh ancol benzylic với các ancol thơm khác
Về độ tan, ancol benzylic tan tốt trong nước hơn các ancol thơm khác nhờ nhóm -CH2OH linh động.
Khả năng phản ứng của ancol benzylic mạnh hơn do electron π của vòng benzen có thể giúp ổn định ion carbocation.
Điểm sôi của ancol benzylic (205°C) cao hơn phenol (182°C) do liên kết hydro mạnh hơn giữa các phân tử.
Kiến thức về ancol benzylic công thức cấu tạo giúp người học nắm vững cấu trúc phân tử đặc trưng của hợp chất hữu cơ quan trọng này. Với nhóm chức -CH2OH gắn trực tiếp vào vòng benzen, ancol benzylic thể hiện tính chất hóa học đa dạng trong các phản ứng oxi hóa và thế. Các phương pháp điều chế trong phòng thí nghiệm và công nghiệp tạo ra sản phẩm ứng dụng rộng rãi trong tổng hợp hữu cơ, dược phẩm và công nghiệp hóa chất.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

