Tìm hiểu công thức paracetamol và cấu trúc phân tử trong hóa học cơ bản
Công thức paracetamol là một trong những kiến thức quan trọng trong hóa dược. Paracetamol có cấu trúc phân tử đặc biệt với các nhóm chức đặc trưng. Các phản ứng tổng hợp paracetamol diễn ra qua nhiều giai đoạn phức tạp. Thuốc này có tác dụng giảm đau, hạ sốt hiệu quả khi sử dụng đúng liều lượng.
Công thức paracetamol
Paracetamol là một trong những thuốc giảm đau phổ biến nhất hiện nay. Công thức paracetamol có tên hóa học là N-acetyl-p-aminophenol hoặc acetaminophen.
Công thức phân tử: C8H9NO2
Công thức cấu tạo:
“`
O
||
H3C-C-NH-C6H4-OH
“`
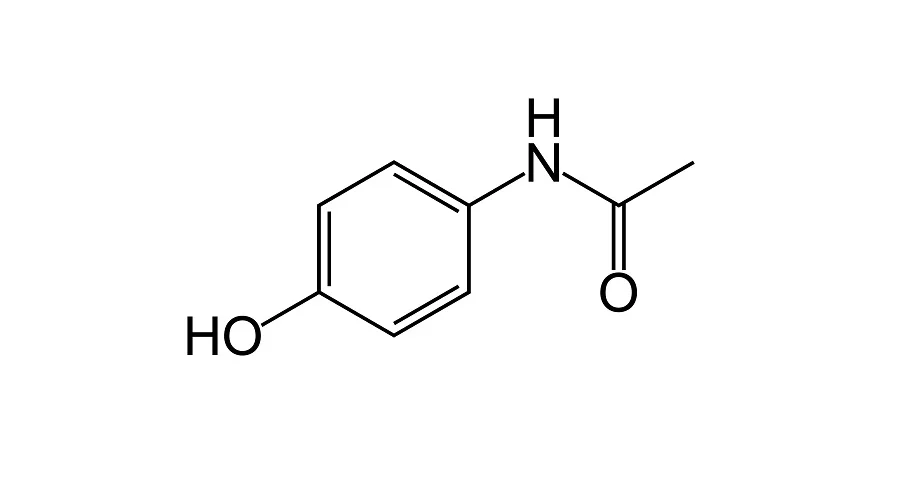
Paracetamol có cấu trúc gồm vòng benzene với 2 nhóm thế quan trọng:
- Nhóm hydroxyl (-OH) ở vị trí para
- Nhóm acetylamino (-NHCOCH3)
Trong quá trình giảng dạy, tôi thường giúp học sinh ghi nhớ công thức này bằng cách chia thành 3 phần:
- Nhóm methyl (CH3-)
- Nhóm carbonyl (-CO-)
- Phần còn lại (-NH-C6H4-OH)
Paracetamol tồn tại dưới dạng tinh thể màu trắng, không mùi. Nhiệt độ nóng chảy khoảng 169-170°C và tan tốt trong nước nóng.
Khi giải các bài tập về paracetamol, học sinh cần chú ý đến các phản ứng đặc trưng của nhóm hydroxyl và nhóm acetylamino. Điều này giúp xác định được tính chất hóa học của hợp chất.
Cấu tạo phân tử và công thức hóa học của paracetamol
Paracetamol là một trong những thuốc giảm đau phổ biến nhất hiện nay. Tôi sẽ phân tích chi tiết cấu trúc phân tử để giúp các bạn hiểu rõ hơn về loại thuốc này.
Công thức phân tử của paracetamol
Công thức phân tử paracetamol là C8H9NO2. Đây là một phân tử hữu cơ tương đối đơn giản, gồm 8 nguyên tử carbon, 9 nguyên tử hydro, 1 nguyên tử nitơ và 2 nguyên tử oxy.
Trong quá trình giảng dạy, tôi thường so sánh paracetamol với công thức aspirin để học sinh dễ nhớ. Cả hai đều là thuốc giảm đau nhưng có cấu trúc khác biệt.
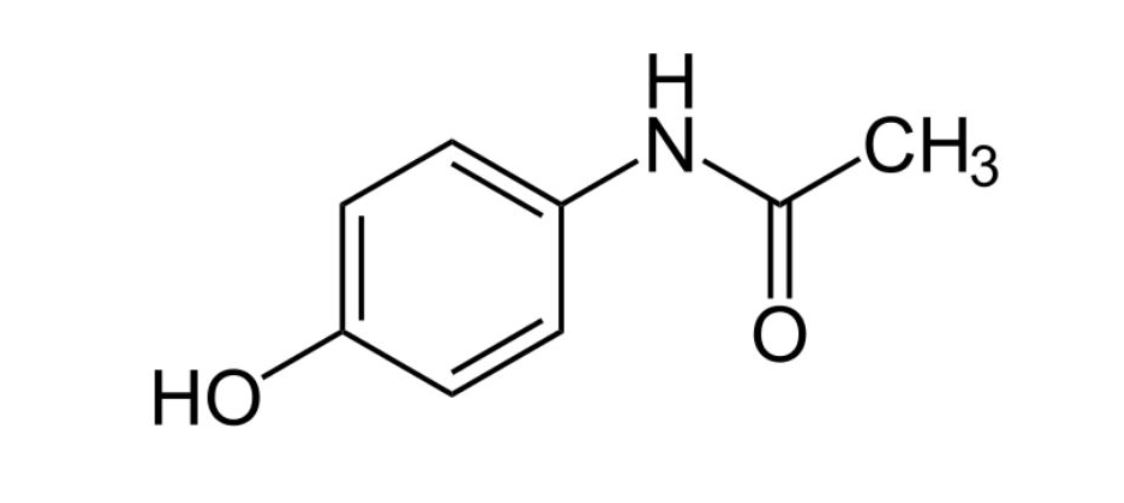
Cấu trúc phân tử paracetamol
Paracetamol cấu tạo phân tử dạng tinh thể màu trắng, không mùi. Phân tử có dạng phẳng với vòng benzen làm khung chính.
Các liên kết trong phân tử bao gồm liên kết đơn C-C, C-H và liên kết đôi C=O. Nhóm hydroxyl (-OH) gắn trực tiếp vào vòng benzen tạo nên hoạt tính của thuốc.
Các nhóm chức chính trong phân tử
Paracetamol cấu trúc có hai nhóm chức quan trọng quyết định tính chất của thuốc. Nhóm hydroxyl (-OH) ở vị trí para và nhóm acetamid (-NHCOCH3) tạo nên hoạt tính giảm đau.
Trong 20 năm giảng dạy, tôi nhận thấy học sinh thường nhớ tốt hơn khi liên hệ các nhóm chức với tác dụng của thuốc. Nhóm hydroxyl giúp tăng khả năng tan trong nước và nhóm acetamid tạo liên kết hydro với thụ thể đau.
Thành phần và tính chất hóa học của paracetamol
Paracetamol là một loại thuốc giảm đau, hạ sốt phổ biến được sử dụng rộng rãi trên toàn thế giới. Thuốc có công thức phân tử C8H9NO2 và tên hóa học là N-acetyl-p-aminophenol.
Để hiểu rõ hơn về loại thuốc này, tôi sẽ phân tích chi tiết về cấu tạo và đặc tính của nó. Việc nắm vững kiến thức này giúp sử dụng thuốc hiệu quả và an toàn hơn.
Các thành phần cấu tạo nên paracetamol
Paracetamol thành phần chính gồm một vòng benzene được thay thế bởi hai nhóm chức quan trọng:
Nhóm hydroxyl (-OH) ở vị trí para
Nhóm acetylamino (-NHCOCH3)
Cấu trúc này tạo nên tính ổn định và hoạt tính sinh học đặc trưng của thuốc. Tương tự như cholesterol là gì, cấu trúc phân tử quyết định tính chất và chức năng của hợp chất.
Tính chất vật lý của paracetamol
Paracetamol tồn tại ở dạng tinh thể màu trắng, không mùi. Nhiệt độ nóng chảy của nó là 169-170°C.
Thuốc có độ tan trong nước ở 20°C là 14g/L và tan tốt trong ethanol. Đây là lý do paracetamol thường được bào chế dưới dạng viên nén hoặc dung dịch uống.
Phản ứng hóa học đặc trưng
Paracetamol tham gia các phản ứng đặc trưng của nhóm phenol và amin. Phản ứng màu với FeCl3 cho màu xanh tím đặc trưng.
Trong môi trường kiềm, paracetamol bị thủy phân tạo p-aminophenol và acid acetic. Đây là cơ sở để xác định hàm lượng thuốc trong các mẫu phân tích.
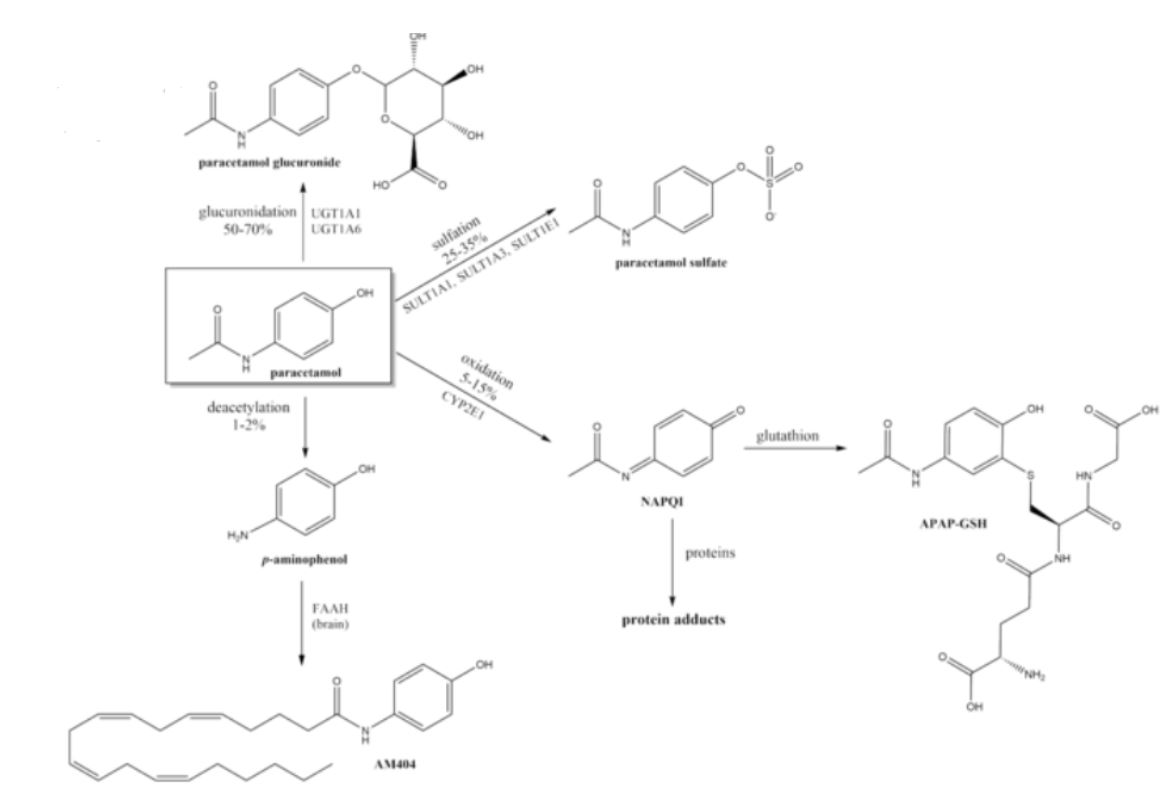
Khi bị oxy hóa mạnh, paracetamol chuyển thành N-acetyl-p-benzoquinone imine (NAPQI). Phản ứng này liên quan đến độc tính của thuốc khi sử dụng quá liều.
Quy trình tổng hợp và sản xuất paracetamol
Paracetamol là một trong những thuốc giảm đau phổ biến nhất hiện nay. Quá trình sản xuất công thức của paracetamol đòi hỏi nhiều công đoạn phức tạp và nghiêm ngặt. Tương tự như quá trình sản xuất công thức bột ngọt, việc tổng hợp cần tuân thủ các tiêu chuẩn GMP.
Nguyên liệu ban đầu
Phenol là nguyên liệu chính để tổng hợp paracetamol công thức C8H9NO2. Ngoài ra còn cần axit nitric đặc, natri borohydride và anhydric acetic. Các hóa chất này phải đạt độ tinh khiết cao, tương tự như nguyên liệu sản xuất tơ tằm công thức.
Phenol được bảo quản ở nhiệt độ phòng trong bình kín tránh ánh sáng. Axit nitric đặc cần được lưu trữ trong tủ hút riêng biệt.
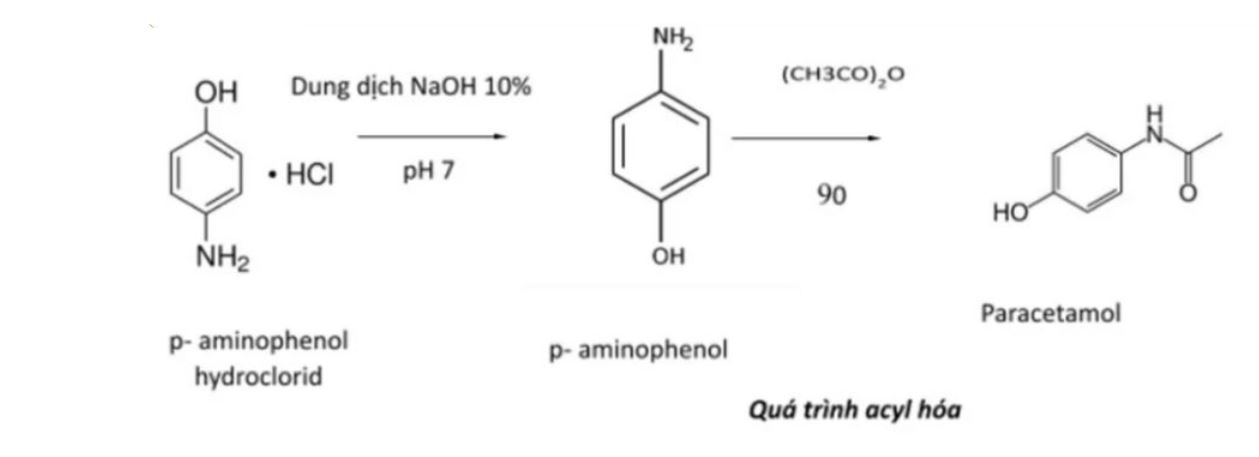
Các giai đoạn tổng hợp chính
Giai đoạn đầu là nitro hóa phenol bằng axit nitric đặc ở 15-20°C tạo p-nitrophenol. Phản ứng này cần kiểm soát nhiệt độ chặt chẽ để tránh tạo sản phẩm phụ.
Tiếp theo là khử nhóm nitro thành nhóm amino bằng natri borohydride tạo p-aminophenol. Phản ứng diễn ra ở 60-65°C trong 2-3 giờ.
Cuối cùng là acetyl hóa p-aminophenol bằng anhydric acetic ở 80-85°C trong 30 phút để tạo paracetamol thô.
Tinh chế sản phẩm
Paracetamol thô được kết tinh lại trong nước nóng để loại tạp chất. Tinh thể được lọc và sấy khô ở 60°C.
Sản phẩm tinh khiết phải đạt các tiêu chuẩn về độ tinh khiết, điểm nóng chảy và pH theo quy định của dược điển.
Kiểm tra chất lượng được thực hiện bằng sắc ký lỏng hiệu năng cao HPLC và quang phổ hồng ngoại IR.
FAQ: Câu hỏi thường gặp về paracetamol
Paracetamol là thuốc giảm đau hạ sốt phổ biến được sử dụng rộng rãi. Dưới đây là một số câu hỏi thường gặp về loại thuốc này.
Sự khác biệt giữa paracetamol và aspirin?
Paracetamol và aspirin có cơ chế tác dụng khác nhau. Công thức paracetamol là gì – C8H9NO2 có tác dụng ức chế tổng hợp prostaglandin ở hệ thần kinh trung ương.
Aspirin (C9H8O4) ức chế enzyme cyclooxygenase (COX) và giảm tổng hợp prostaglandin ngoại vi. Điều này giải thích tại sao aspirin có thêm tác dụng chống viêm mà paracetamol không có.
Paracetamol ít gây kích ứng dạ dày hơn aspirin nên thường được ưu tiên sử dụng cho người bị viêm loét dạ dày. Tương tự như sorbitol là gì, paracetamol cũng được sử dụng rộng rãi trong y học.
Tại sao paracetamol có tác dụng giảm đau?
Paracetamol công thức hóa học tác động lên hệ thống thần kinh trung ương để giảm đau. Thuốc ức chế quá trình tổng hợp prostaglandin – chất trung gian gây đau.
Ngoài ra, paracetamol còn tác động lên các thụ thể cannabinoid và serotonin. Điều này làm tăng ngưỡng chịu đau của cơ thể, tương tự như cơ chế của công thức phân kali.
Paracetamol cũng có khả năng hạ sốt thông qua tác động lên vùng dưới đồi – trung tâm điều hòa thân nhiệt của não bộ.
Liều lượng an toàn của paracetamol?
Liều thông thường cho người lớn là 500-1000mg/lần, cách 4-6 giờ/lần. Tổng liều không quá 4g/ngày để tránh độc tính gan.
Trẻ em cần tính liều theo cân nặng, thường 10-15mg/kg/lần. Không dùng quá 5 lần/ngày và không dùng liên tục quá 5 ngày.
Cần đặc biệt thận trọng ở người có bệnh gan, thận hoặc nghiện rượu. Quá liều paracetamol có thể gây suy gan cấp nguy hiểm.
Kiến thức về công thức paracetamol giúp người học hiểu rõ cấu trúc phân tử và cơ chế hoạt động của loại thuốc giảm đau phổ biến này. Các thành phần cấu tạo đặc trưng như nhóm hydroxyl và acetamid quyết định tính chất hóa học cũng như tác dụng dược lý của paracetamol. Quá trình tổng hợp paracetamol từ nguyên liệu ban đầu đến sản phẩm cuối cùng tuân theo các nguyên tắc hóa học cơ bản và quy trình sản xuất nghiêm ngặt.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

