Nắm kỹ công thức cấu tạo của C4H10 và các đặc điểm cấu trúc butan
Công thức cấu tạo của C4H10 tồn tại dưới hai dạng đồng phân cấu trúc. Butan thẳng và iso-butan có những đặc điểm cấu trúc riêng biệt. Các tính chất hóa học đặc trưng của butan tạo nên nhiều ứng dụng quan trọng trong đời sống. Phương pháp viết công thức cấu tạo giúp phân biệt rõ hai dạng đồng phân này.
Công thức cấu tạo của C4H10 và các đặc điểm cơ bản
C4H10 là một hydrocacbon no thuộc dãy đồng đẳng alkane. Tương tự như công thức cấu tạo của ch4, C4H10 cũng có cấu tạo dạng mạch cacbon liên kết với hydro.
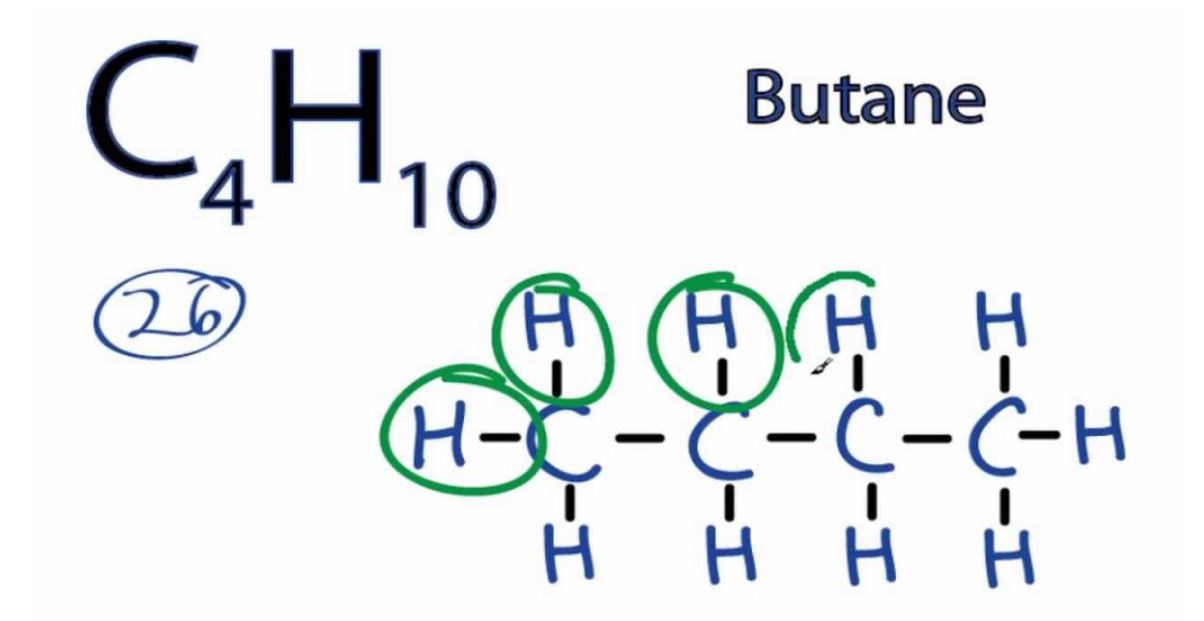
Công thức cấu tạo của C4H10 có 2 dạng đồng phân:
- n-butane (mạch thẳng): CH3-CH2-CH2-CH3
- iso-butane (mạch nhánh): CH3-CH(CH3)-CH3
Trong quá trình giảng dạy, tôi thường giúp học sinh phân biệt 2 dạng này bằng cách vẽ mô hình phân tử. n-butane giống như một chuỗi xích thẳng, còn iso-butane như một cái cây có nhánh.
Các đặc điểm cấu tạo quan trọng của công thức cấu tạo C4H10:
- Mỗi nguyên tử C đều liên kết với 4 liên kết đơn
- Các nguyên tử H bao quanh mạch C chính
- Góc liên kết C-C-C xấp xỉ 109.5°
Cả hai dạng đồng phân đều có cùng công thức phân tử nhưng khác nhau về tính chất vật lý. n-butane có nhiệt độ sôi cao hơn iso-butane do cấu trúc mạch thẳng cho phép các phân tử xếp chặt hơn.
Cấu trúc phân tử và đồng phân của C4H10
C4H10 có hai dạng đồng phân cấu tạo là n-butan và iso-butan. Mỗi dạng đồng phân có cấu tạo phân tử C4H10 đặc trưng và tính chất riêng biệt.
Tương tự như cấu tạo phân tử c3h8, cả hai đồng phân đều có số nguyên tử cacbon và hydro giống nhau nhưng khác nhau về cách sắp xếp trong không gian.
Cấu trúc không gian của n-butan
N-butan có cấu trúc mạch cacbon thẳng với 4 nguyên tử cacbon liên kết đơn. Các nguyên tử cacbon xếp thành một đường thẳng.
Mỗi nguyên tử cacbon đầu mối liên kết với 3 nguyên tử hydro. Hai nguyên tử cacbon giữa liên kết với 2 nguyên tử hydro.
Góc liên kết C-C-C xấp xỉ 109.5° tạo thành hình zigzag. Đây là cấu trúc bền vững nhất của n-butan.
Cấu trúc không gian của iso-butan
Iso-butan có một nguyên tử cacbon trung tâm liên kết với 3 nhóm -CH3. Cấu trúc không gian C4H10 dạng iso có dạng hình tháp tam giác.
Nguyên tử cacbon trung tâm liên kết với một nguyên tử hydro và ba nhóm metyl (-CH3). Ba nhóm metyl tạo thành góc 120° với nhau.
Cấu trúc này làm cho phân tử iso-butan có hình dạng đối xứng hơn so với n-butan.
So sánh hai đồng phân của C4H10
Về nhiệt độ sôi, n-butan sôi ở -0.5°C trong khi iso-butan sôi ở -11.7°C. Sự khác biệt do cấu trúc phân tử khác nhau.
N-butan có lực tương tác van der Waals mạnh hơn do chuỗi cacbon thẳng. Iso-butan có lực tương tác yếu hơn vì cấu trúc phân nhánh.
Về độ tan trong nước, cả hai đồng phân đều không tan. Tuy nhiên, iso-butan tan tốt hơn trong dung môi hữu cơ không phân cực.
Butan và vai trò của nó trong đời sống
Butan là một trong những hợp chất hữu cơ quan trọng thuộc dãy ankane. Chất này đóng vai trò thiết yếu trong nhiều lĩnh vực công nghiệp và đời sống hàng ngày.
Butan là gì và đặc điểm hóa học
Butan là gì? Đây là một hydrocarbon no, có công thức phân tử C4H10, tồn tại ở dạng khí trong điều kiện thường. Butan có hai đồng phân cấu trúc là n-butan và iso-butan.
Tương tự như các đồng đẳng khác trong dãy ankane như công thức cấu tạo của c6h14 hay c5h12 công thức cấu tạo, butan có khả năng tham gia phản ứng thế và cháy.
Butan không màu, không mùi và dễ dàng hóa lỏng dưới áp suất thấp. Nhiệt độ sôi của butan là -0.5°C, điểm nóng chảy -138.3°C.
Ứng dụng của butan trong thực tế
Trong công nghiệp, C4H10 là gì không thể thiếu trong sản xuất nhiên liệu. Butan được sử dụng làm nhiên liệu cho bếp gas mini và bật lửa.
Butan còn là nguyên liệu quan trọng trong ngành công nghiệp hóa dầu. Nó được dùng để sản xuất các hợp chất hữu cơ khác như butadiene.

Theo số liệu từ Hiệp hội Khí đốt Thế giới, butan chiếm khoảng 60% thành phần trong gas dân dụng. Điều này cho thấy tầm quan trọng của nó trong sinh hoạt hàng ngày.
Trong y tế, butan tinh khiết được sử dụng làm chất làm lạnh trong một số thiết bị y tế. Nó cũng là dung môi quan trọng trong ngành công nghiệp dược phẩm.
Cách viết công thức cấu tạo của C4H10
Viết công thức cấu tạo của C4H10 là một kỹ năng quan trọng trong hóa học hữu cơ. C4H10 có hai dạng đồng phân cấu tạo: n-butane và iso-butane.
Để viết chính xác công thức cấu tạo, cần nắm vững các quy tắc cơ bản và thực hiện theo trình tự logic. Kinh nghiệm 20 năm giảng dạy cho thấy nhiều học sinh thường nhầm lẫn giữa hai dạng này.
Quy tắc viết công thức cấu tạo
Nguyên tắc đầu tiên là xác định số liên kết của carbon. Mỗi nguyên tử carbon luôn tạo 4 liên kết hóa học.
Các nguyên tử carbon có thể liên kết với nhau tạo thành mạch thẳng hoặc mạch nhánh. Các nguyên tử hydro sẽ gắn vào các vị trí còn lại của carbon.
Trong công thức phân tử C4H10, tổng số liên kết của carbon phải bằng số nguyên tử hydro có trong phân tử.
Các bước viết công thức cấu tạo C4H10
Bước 1: Viết khung carbon chính gồm 4 nguyên tử C liên kết với nhau.
Bước 2: Điền các nguyên tử H vào các vị trí còn trống của C, đảm bảo mỗi C tạo đủ 4 liên kết.
Bước 3: Kiểm tra lại tổng số nguyên tử H phải đúng bằng 10.
Tương tự như cách viết công thức cấu tạo của c5h10 và công thức cấu tạo của c 4 h 8, việc nắm vững các bước sẽ giúp viết đúng mọi công thức.
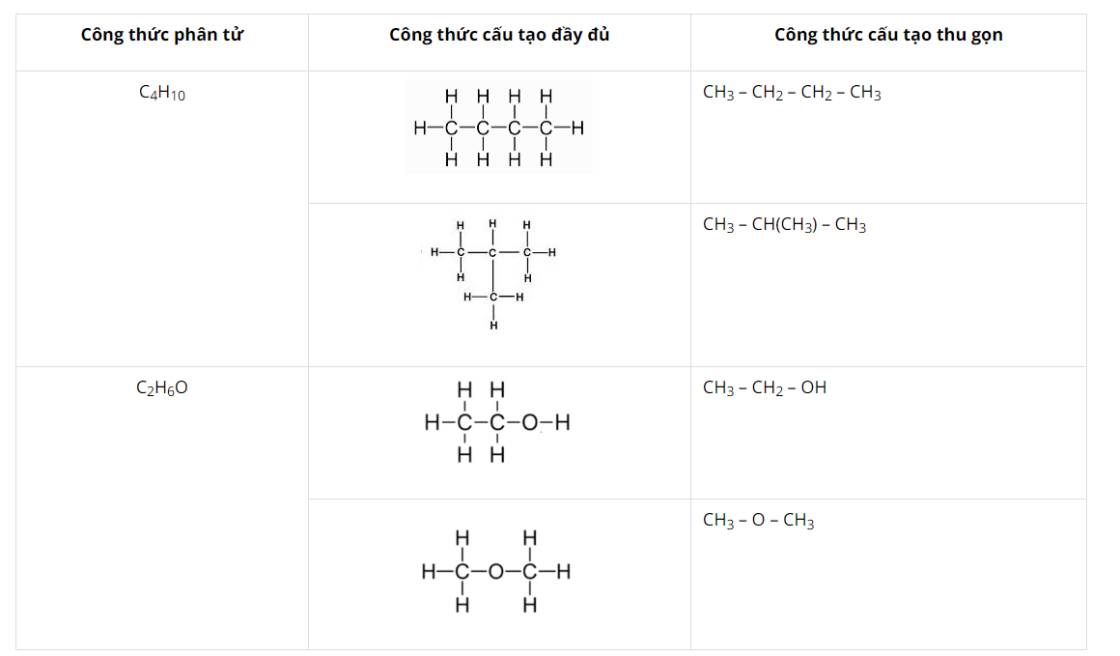
Lưu ý khi viết công thức cấu tạo
Cần phân biệt rõ hai dạng đồng phân của C4H10. N-butane có dạng mạch thẳng, còn iso-butane có một nhánh methyl.
Khi viết công thức cấu tạo thu gọn, có thể bỏ bớt các nguyên tử H nhưng phải giữ nguyên bộ khung carbon.
Một sai lầm phổ biến là viết thiếu hoặc thừa số liên kết của carbon. Tôi thường nhắc học sinh kiểm tra kỹ điểm này.
FAQ: Câu hỏi thường gặp về C4H10
C4H10 là một hydrocacbon no thuộc dãy đồng đẳng của metan. Đây là một chất khí phổ biến trong công nghiệp và đời sống. Tôi sẽ giải đáp các thắc mắc thường gặp về hợp chất này.
Sự khác biệt giữa công thức phân tử và công thức cấu tạo của C4H10
Công thức cấu tạo của C4H10 có 2 dạng đồng phân chính. Đồng phân thứ nhất là n-butan với cấu trúc mạch thẳng CH3-CH2-CH2-CH3. Đồng phân thứ hai là iso-butan với cấu trúc mạch nhánh (CH3)3CH.
Trong quá trình giảng dạy, tôi thường so sánh cấu trúc này với công thức cấu tạo n2h4 để học sinh dễ hiểu hơn về khái niệm đồng phân.
Tính chất vật lý và hóa học của C4H10
C4H10 là chất khí không màu, không mùi ở điều kiện thường. Nhiệt độ sôi của n-butan là -0,5°C và của iso-butan là -11,7°C.
Về tính chất hóa học, C4H10 tham gia phản ứng cháy tạo CO2 và H2O. Tương tự như C6H12 có bao nhiêu đồng phân, C4H10 cũng tham gia phản ứng thế với halogen.
Cách nhận biết C4H10 trong phòng thí nghiệm
C4H10 có thể được nhận biết qua phản ứng cháy với ngọn lửa màu xanh. Khí này nặng hơn không khí nên tích tụ ở đáy bình.
Một phương pháp khác là sử dụng dung dịch KMnO4. Tương tự như cách xác định công thức licopen, C4H10 không làm mất màu dung dịch KMnO4.
Trong phòng thí nghiệm, tôi thường hướng dẫn sinh viên dùng phương pháp đo khối lượng riêng để nhận biết C4H10 một cách chính xác và an toàn.
Kiến thức về công thức cấu tạo của C4H10 giúp học sinh nắm vững cấu trúc phân tử butan với hai dạng đồng phân. Butan là hydrocarbon quan trọng trong công nghiệp và đời sống. Việc thành thạo cách viết công thức cấu tạo, phân biệt đồng phân và tính chất của C4H10 tạo nền tảng cho học sinh tiếp thu tốt các kiến thức hóa học hữu cơ nâng cao.
Bài viết liên quan

Tìm hiểu carbohydrate công thức hóa học và phản ứng đặc trưng
Tìm hiểu carbohydrate công thức hóa học qua cấu tạo, phân loại và phản ứng đặc trưng. Khám phá cấu trúc glucozơ, saccarozơ cùng các phương pháp nhận biết đường đơn, đường đôi trong phòng thí nghiệm.

Nắm rõ công thức hóa học của dầu diesel và tính chất quan trọng
Tìm hiểu chi tiết công thức hóa học của dầu diesel, cấu tạo phân tử và thành phần hydrocarbon C10-C22. Khám phá tính chất vật lý, độ cháy, độc tính và ứng dụng trong đời sống.
Kiến thức về natri propionat công thức và ứng dụng trong thực phẩm
Tìm hiểu chi tiết về natri propionat công thức cấu tạo, phương pháp điều chế, tính chất và ứng dụng làm chất bảo quản thực phẩm an toàn, được giải thích đơn giản dễ hiểu.
Nắm kỹ axit lactic công thức và ứng dụng trong đời sống hàng ngày
Tìm hiểu về axit lactic công thức cấu tạo, tính chất hóa học đặc trưng và vai trò quan trọng trong cơ thể. Khám phá ứng dụng trong sản xuất thực phẩm, mỹ phẩm và công nghiệp.
Tổng quan về phenyl acrylat công thức và ứng dụng trong hóa học
Tìm hiểu chi tiết về phenyl acrylat công thức cấu tạo, phương pháp tổng hợp, tính chất vật lý, hóa học và ứng dụng trong công nghiệp polymer. Hướng dẫn điều chế an toàn.
Phân tích công thức cấu tạo C3H6O3 và vai trò của axit lactic trong cơ thể
Tìm hiểu chi tiết công thức cấu tạo C3H6O3 và các dạng đồng phân, đặc biệt là axit lactic phổ biến trong sữa chua và cơ thể. Khám phá tính chất, ứng dụng và vai trò sinh học quan trọng.

