Công thức cấu tạo C2H2 và tính chất cơ bản
C2H2 là hợp chất hóa học thuộc nhóm hydrocacbon không no có ứng dụng đa dạng trong cuộc sống. Để hiểu rõ hơn về công thức cấu tạo C2H2 cũng như tính chất, ứng dụng và cách điều chế, bạn theo dõi ngay bài viết sau.
Công thức cấu tạo C2H2 là gì?
C2H2 là công thức hóa học của axetilen – một hydrocacbon không no nằm trong dãy đồng đẳng ankin. Công thức cấu tạo C2H2 là H – C ≡ C – H, bao gồm 2 nguyên tử cacbon và 2 nguyên tử hydro.
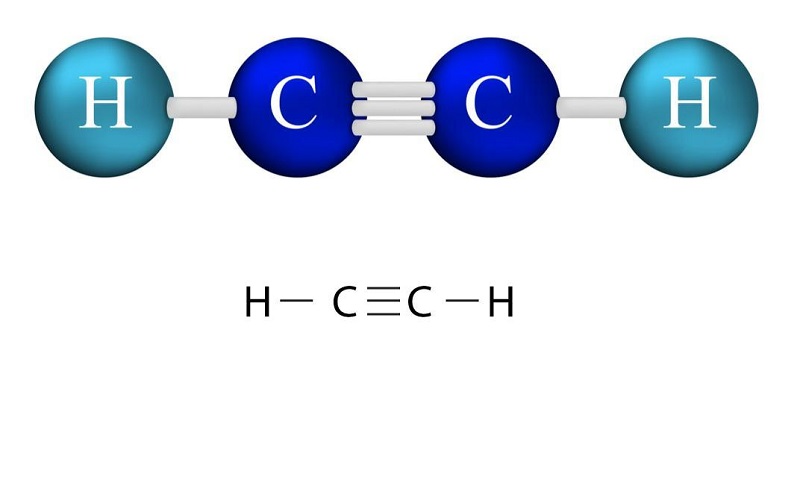
Tính chất vật lý của C2H2
Một số tính chất vật lý cơ bản của Axetilen:
- C2H2 là chất khí không màu, không mùi, dễ cháy và ít tan trong nước nhưng tan tốt trong acetone, benzen.
- Axetilen có trọng lượng riêng d = 26 nhẹ hơn không khí.
- Khối lượng riêng của khí C2H2 là 1.097 kg m-3.
- Axetilen nóng chảy ở nhiệt độ -80.8 độ C và sôi ở -84 độ C.
Tính chất hóa học của C2H2
C2H2 có tính chất hóa học đặc trưng là các phản ứng cộng, oxi hóa và đime hóa – trime hóa. Các tính chất hóa học quan trọng của axetilen thể hiện như sau:
Phản ứng cộng
Axetilen phản ứng cộng với brom, hidro, hidro clorua và nước tạo ra một phân tử khác lớn hơn. Sau đây là các phản ứng cộng của C2H2:
- C2H2 phản ứng với brom làm mất màu dung dịch brom và tạo ra dẫn xuất halogen.
HC≡CH + Br2 → CHBr=CHBr
HC≡CH + 2Br2 → CHBr2-CHBr2
- C2H2 phản ứng cộng với hidro trong trong điều kiện có chất xúc tác niken hoặc Pb/PbCo3 tạo thành etilen hoặc etan.
HC≡CH + H2 → CH2=CH2 (xúc tác Pb/PbCo3)
HC≡CH + 2H2 → CH3-CH3 (xúc tác Ni)
- C2H2 phản ứng cộng với hidro clorua trong điều kiện nhiệt độ cao và có xúc tác HgCl2 tạo thành đicloetan.
HC≡CH + HCl → CH2=CH-Cl
CH2=CH-Cl + HCl → CH3-CHCl2
- C2H2 phản ứng cộng với H2O với xúc tác HgSO4, H2SO4 tạo thành andehit axetic.
HC≡CH + H2O → CH2=CHOH → CH3CHO
Phản ứng đime hóa và trime hóa của C2H2
Khi tác dụng hai phân tử axetilen ở nhiệt độ thích hợp và có chất xúc tác sẽ tạo thành hợp chất vinylaxetilen. Phương trình phản ứng đime hóa và trime hóa của C2H2 như sau:
- 2HC≡CH → CH2=CH-C≡CH

Phản ứng oxy hóa
C2H2 là hợp chất dễ cháy, khi bị đốt sẽ tạo thành khí cacbon dioxit và nước. Phản ứng cháy của axetilen tỏa nhiều nhiệt với ngọn lửa sáng.
Phương trình phản ứng oxy hóa của C2H2:
- 2C₂H₂ + 5O₂ → 4CO₂ + 2H₂O
Cách điều chế C2H2 trong công nghiệp và phòng thí nghiệm
Axetilen được điều chế trong phòng thí nghiệm hoặc trong công nghiệp với các phương pháp khác nhau. Nhìn chung, phương pháp điều chế công nghiệp tạo ra C2H2 tinh khiết với số lượng lớn hơn.
Điều chế trong phòng thí nghiệm
Bạn cho một mẫu nhỏ canxi cacbua vào trong ống nghiệm có chứa 1ml nước rồi đậy kín ống nghiệm có đường dẫn khí. Bạn đốt khí sinh ra ở đầu ống dẫn sẽ thu được C2H2.
Phương trình phản ứng:
- CaC2 + H2O → C2H2 + Ca(OH)2
Điều chế trong công nghiệp
Sau đây là một số cách điều chế C2H2 phổ biến trong công nghiệp kèm theo phương trình phản ứng:
Điều chế bằng metan
Phương pháp điều chế axetilen phổ biến, hiệu quả và giá rẻ nhất là nhiệt phân metan ở nhiệt độ 15000 độ C tạo khí C2H2 và H2. Sau đó, tách riêng hai khí trong hỗn hợp bạn sẽ thu được C2H2.
Phương trình phản ứng:
- 2 CH4→ C2H2 + 3 H2
Điều chế bằng cacbon
Khi cho cacbon tiếp xúc với khí hidro có hồ quang điện, bạn thu được khí C2H2 tinh khiết. Phương trình phản ứng của cacbon và hidro để điều chế C2H2:
- 2C + H2(hồ quang điện) → C2H2
Điều chế bằng Ag2C
Cách điều chế axetilen bằng Ag2C không được ứng dụng phổ biến do có lẫn tạp chất, không thu được khí tinh khiết. Phương trình phản ứng:
- 2HCl + Ag2C → 2AgCl + C2H2
Ứng dụng khí C2H2 trong cuộc sống
Với tính chất hóa học đa dạng cùng cách điều chế đơn giản, axetilen được ứng dụng trong nhiều lĩnh vực như:
- C2H2 được dùng để làm khí hàn vì nhiệt độ sản sinh ra có thể lên đến 3500 độ C.
- Axetilen là nguyên liệu sản xuất một số hóa chất quan trọng như axit axetic và vinyl clorua.
- C2H2 ứng dụng để sản xuất một số dược phẩm như aspirin, acetaminophen,…
- C2H2 là một chất quan trọng dùng trong sản xuất thuốc trừ sâu như DDT, Malathion, Chlordane, Dieldrin, Endrin,…

Axetilen có độc không và cách xử trí khi tiếp xúc
Axetilen có độc hay không còn tùy thuộc vào nồng độ và thời gian tiếp xúc. Nếu bạn tiếp xúc với khí C2H2 nồng độ quá 2.5% với thời gian quá 1 giờ sẽ gây ra một số vấn đề nguy hại cho sức khỏe.
Ví dụ như: buồn nôn, choáng váng, đau tức ngực, khó thở, nhức đầu thậm chí là hôn mê. Khí C2H2 nồng độ cao tiếp xúc trực tiếp với da sẽ gây phát ban, nổi mẩn đỏ.
Cách xử trí khi ngộ độc khí C2H2 là hãy đưa người bệnh đến nơi thoáng đãng, tránh xa nguồn khí. Nếu tình trạng trở nặng, người bệnh cần được đưa đến cơ sở y tế để được thăm khám và điều trị.
Kết luận
Thông qua những thông tin trên, chắc hẳn bạn đọc đã biết được công thức cấu tạo C2H2 cũng như tính chất, ứng dụng và cách điều chế khí. Hy vọng bài viết trên sẽ cung cấp cho bạn những kiến thức hóa học bổ ích để ứng dụng vào công việc và cuộc sống.
Bài viết liên quan
Hiểu rõ axit nitrơ công thức và tính chất hóa học cơ bản
Tìm hiểu chi tiết về axit nitrơ công thức HNO2, cấu tạo phân tử và tính chất hóa học. Khám phá các phản ứng với bazơ, muối, kim loại cùng ứng dụng trong công nghiệp.

Hiểu sâu nước brom công thức và ứng dụng trong thí nghiệm hóa học
Tìm hiểu chi tiết về nước brom công thức, cấu tạo phân tử và tính chất đặc trưng. Hướng dẫn điều chế, phản ứng hóa học quan trọng cùng các biện pháp an toàn khi sử dụng trong phòng thí nghiệm.

Tổng quan natri carbonat công thức và ứng dụng trong đời sống
Tìm hiểu chi tiết về natri carbonat công thức Na2CO3, cấu tạo phân tử, tính chất hóa học đặc trưng và quy trình sản xuất trong công nghiệp. Khám phá ứng dụng thực tiễn của muối cacbonat.

Học thuộc công thức hóa học của lưu huỳnh và các hợp chất quan trọng
Tìm hiểu chi tiết công thức hóa học của lưu huỳnh, cấu tạo phân tử và các dạng tồn tại. Khám phá tính chất, phản ứng đặc trưng cùng ứng dụng quan trọng của nguyên tố này trong đời sống.

Điểm qua oleum công thức và cách tính nồng độ trong hóa học
Tìm hiểu chi tiết về oleum công thức, cấu tạo và tính chất hóa học. Hướng dẫn cách tính nồng độ, pha chế an toàn kèm bài tập có lời giải chi tiết cho học sinh phổ thông.

Tìm hiểu công thức DAP và cách sử dụng phân bón DAP hiệu quả cho cây trồng
Tìm hiểu công thức DAP và hướng dẫn chi tiết về cách pha, tỉ lệ bón phân DAP cho từng loại cây trồng. Giải thích thành phần hóa học và kỹ thuật sử dụng phân bón DAP hiệu quả.

